Элементы, окрашенные в различные цвета, являются неотъемлемой частью нашей повседневной жизни. Мы видим их во многих предметах, таких как мебель, посуда, автомобили и многое другое. Но знание того, какие именно металлы окисляются и обретают свои характерные цвета, может быть интересно для любознательных умов.
Одним из таких металлов является медь. В своем чистом состоянии медь имеет характерный красновато-желтый цвет. Однако, когда медь подвергается воздействию кислорода из воздуха и влаги, она окрашивается в зеленовато-голубой цвет. Это объясняется образованием на поверхности меди оксида меди, который обладает именно таким оттенком.
Другим цветным металлом является алюминий. В своем чистом состоянии алюминий имеет серебристый цвет. Однако, он очень реактивен и быстро покрывается оксидной пленкой при контакте с кислородом. Эта пленка защищает алюминий от дальнейшей окисления, но при этом придает ему белый цвет.
Еще одним примером цветного металла, окисление которого приводит к изменению его цвета, является свинец. Свинец имеет серый цвет, но при воздействии атмосферного кислорода его поверхность покрывается слоем оксида свинца, который придает свинцу белый цвет.
Металлы, которые подвержены окислению

Окисление — процесс, при котором атомы металлов соединяются с кислородом, образуя окислы. В результате окисления металлы теряют свои химические и физические свойства, изменяется их цвет, появляется коррозия и ржавчина. Некоторые металлы особенно подвержены окислению.
Алюминий – один из наиболее распространенных металлов, подверженных окислению. Когда алюминий вступает в реакцию с кислородом, он образует тонкую пленку оксида алюминия на своей поверхности. Эта пленка защищает металл от дальнейшего окисления, но при повреждении она быстро вновь образуется и процесс окисления продолжается.
Железо – еще один металл, склонный к окислению. Когда железо вступает в реакцию с кислородом и влагой, образуется ржавчина. Ржавчина обладает коричневатым цветом и характерной текстурой. Она сильно снижает прочность и эстетическое качество железных предметов и конструкций.
Медь – еще один цветной металл, поддающийся окислению. Когда медь окисляется, она образует известную всем зеленоватую пленку, известную как патина. Патина образуется на медных изделиях и покрывает их поверхность, придавая им особый внешний вид. В больших количествах патина может оказывать негативное влияние на медь и вызывать коррозию.
Серебро – еще один металл, который подвергается окислению. Когда серебро вступает в реакцию с кислородом и сероводородом в воздухе, образуется черная серная пленка. Эта пленка негативно сказывается на блеске и внешнем виде серебряных изделий, поэтому требуется ее регулярная полировка.
Важно помнить, что окисление неизбежно для большинства металлов, особенно в присутствии кислорода и влаги. Однако с помощью правильного ухода и защиты металлы можно сохранять в исходном состоянии на протяжении длительного времени.
Окисление металлов: причины и последствия

Окисление металлов - это процесс, в результате которого металлы соединяются с кислородом. Данный процесс происходит под воздействием различных факторов, таких как влажность, температура, наличие кислорода и других окисляющих агентов.
Окисление металлов является естественным процессом и может привести к различным последствиям. Во-первых, он может привести к образованию окисной пленки на поверхности металла, которая может быть как защитной, так и разрушительной. Защитная пленка обычно образуется на поверхности алюминия, нержавеющей стали и других металлов, что позволяет им сохранять свои свойства и устойчивость к коррозии. Однако, если пленка нарушается или металл находится в агрессивной среде, может начаться разрушение металла.
Более того, окисление металлов может привести к образованию ржавчины, что является одним из наиболее распространенных видов коррозии. Ржавчина образуется на поверхности железа и его сплавов под воздействием влаги и кислорода, что приводит к разрушению металлической структуры.
Кроме того, окисление металлов может привести к потере их эстетического вида. Например, окисление меди приводит к образованию зеленого налета, известного как патина, который может изменить внешний вид изделия и его характеристики.
Для предотвращения окисления металлов могут применяться различные способы, например, использование защитных покрытий, таких как лаки или эмали, или применение специальных антикоррозийных средств. Кроме того, можно контролировать условия окружающей среды и избегать контакта металла с влагой и кислородом, что поможет уменьшить процесс окисления металлов и сохранить их долговечность и внешний вид.
Какие металлы при контакте с воздухом окисляются

Окисление – это процесс, при котором металлы соединяются с кислородом, образуя оксиды. Многие металлы способны подвергаться окислению при контакте с воздухом, но некоторые из них более склонны к окислению, чем другие.
Алюминий является одним из наиболее распространенных металлов, подверженных окислению. Как только алюминий подвергается воздействию кислорода, на его поверхности образуется тонкая пленка оксида, которая придает металлу характерный серебристо-серый цвет. Эта пленка служит защитой от дальнейшего окисления, поскольку предотвращает проникновение воздуха к металлу. Однако, при механическом воздействии или при наличии агрессивных веществ пленка может расколоться и воздействовать на более глубокие слои алюминия.
Железо также легко подвергается окислению при контакте с воздухом. При окислении железа образуется ржавчина – соединение железа с кислородом и водой, обладающее коричневым цветом. Ржавчина может проникать глубже в металл, вызывая его разрушение и образование дырок, особенно при наличии влаги или повышенной влажности воздуха.
Медь также подвержена окислению при контакте с воздухом. При этом процессе образуется патина – зеленоватая или синеватая пленка, состоящая из оксидов и сульфатов меди. Патина является защитным слоем от дальнейшего окисления, но может быть удалена для восстановления блеска меди.
Свинец при длительном контакте с воздухом также подвергается окислению. При этом образуется тонкая пленка оксида свинца, которая медленно темнеет и может в конечном итоге обрести черный цвет. Окисление свинца может привести к разрушению его поверхности и потере блеска.
Это лишь некоторые из металлов, которые при контакте с воздухом подвергаются окислению. Все они нуждаются в особой заботе и защите от воздействия окислительных процессов для продления их срока службы и сохранения внешнего вида.
Реакция металла с кислородом: основные позиции в периодической системе
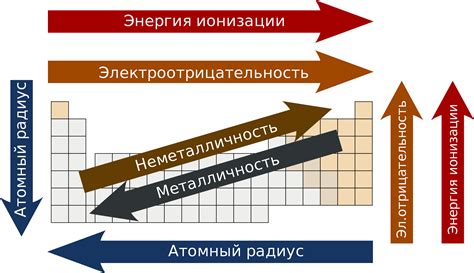
Реакция металла с кислородом – это процесс, в результате которого металл соединяется с кислородом и образует оксид. Оксиды металлов могут иметь различные свойства, в зависимости от положения металла в периодической системе.
Наиболее активные металлы, такие, как щелочные и щелочноземельные металлы, быстро окисляются на воздухе. Например, натрий (Na) при взаимодействии с кислородом образует оксид натрия (Na2O), а кальций (Ca) образует оксид кальция (CaO).
Некоторые металлы, такие как алюминий (Al) и магний (Mg), образуют защитную пленку оксида на своей поверхности, которая предотвращает дальнейшую реакцию металла с кислородом. Это делает их устойчивыми к окислению. Например, алюминий образует оксид алюминия (Al2O3), а магний – оксид магния (MgO).
Некоторые металлы, такие как железо (Fe) и медь (Cu), могут образовывать несколько оксидов в зависимости от условий реакции. Например, железо образует оксид железа (II) FeO и оксид железа (III) Fe2O3. Медь может образовывать оксид меди (I) Cu2O и оксид меди (II) CuO.
Некоторые металлы, такие как серебро (Ag) и золото (Au), очень мало взаимодействуют с кислородом и почти не окисляются при обычных условиях. Они являются химически инертными металлами и обладают высокой коррозионной стойкостью.
Таким образом, реакция металла с кислородом зависит от его положения в периодической системе и может быть использована для предсказания его химического поведения.
Окисленные металлы: свойства и применение
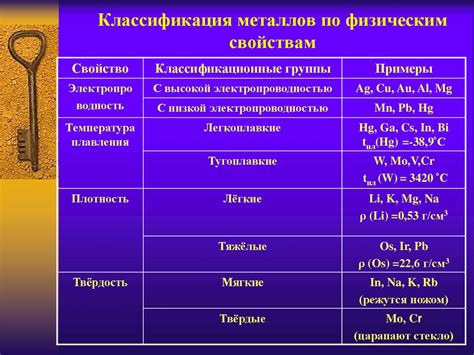
Металлы являются одним из основных классов химических элементов. Они обладают высокой электропроводностью, благодаря свободным электронам в своей валентной оболочке. Однако металлы подвержены процессу окисления при взаимодействии с окружающей средой, особенно с кислородом. При окислении металлы образуют оксиды, которые могут иметь разные свойства и применение.
Окисленные металлы часто обладают новыми свойствами и применяются в различных отраслях промышленности и науке. Например, оксиды цветных металлов используются в качестве пигментов для окрашивания керамики, стекла и красок. Известными примерами таких оксидов являются оксид железа (красная и желтая охра), оксид кобальта (синий пигмент), оксид меди (зелёный пигмент).
Окисленные металлы также проявляют свойства, которые делают их полезными в различных технических областях. Например, оксид алюминия известен своей высокой термической стойкостью и используется в производстве огнеупорных материалов, а оксид кремния широко применяется в производстве стекла и полупроводников.
Важно отметить, что окисленные металлы обычно менее реактивны и коррозионностойкие, чем исходные металлы. Они могут быть менее прочными и подвержены разрушению на воздухе или влажной среде. Поэтому, для защиты окисленных металлов от дальнейшего окисления и коррозии, их часто покрывают защитными покрытиями, такими как лаки, эмали или специальные покрытия, чтобы сохранить их свойства и продлить срок их эксплуатации.
Покрытия, предотвращающие окисление металлов

Во избежание окисления металлов, которое приводит к их коррозии и потере своих свойств, используются различные покрытия. Они создают надежную защитную пленку на поверхности металла, препятствуя проникновению кислорода и влаги.
Одним из самых распространенных покрытий, предотвращающих окисление, является гальваническое покрытие. Оно осуществляется путем погружения металлического изделия в электролитную ванну и нанесения на его поверхность тонкого слоя другого металла. Такая защитная пленка способна активно реагировать с окружающей средой, предотвращая окисление и коррозию.
Другим вариантом покрытия, способствующего защите от окисления, является нанесение органических покрытий. Такие пленки образуются в результате нанесения на поверхность металла специальных лаков, эмалей или красок. Они не только предотвращают проникновение влаги и кислорода, но и улучшают эстетический вид изделия.
Также для защиты металлов от окисления используются горячее оцинкование и анодирование. Горячее оцинкование представляет собой покрытие поверхности металла слоем цинка, который служит барьером для кислорода и влаги. Анодирование применяется для алюминия. В процессе анодирования на поверхности алюминиевого изделия образуется оксидная пленка, способная предотвращать окисление металла.
Все эти покрытия играют важную роль в защите металлов от окисления. Они увеличивают срок службы изделий, сохраняют их эстетический вид и свойства, а также обеспечивают стабильность работы металлических компонентов и конструкций.
Методы защиты от окисления металлов

Защитные покрытия. Один из наиболее распространенных методов защиты металлов от окисления - нанесение защитных покрытий. Это могут быть различные смолы, эмали или краски. Покрытия предотвращают проникновение кислорода и влаги на поверхность металла, благодаря чему его окисление замедляется.
Ингибиторы коррозии. Другой метод защиты металлов от окисления - применение ингибиторов коррозии. Это вещества, которые добавляются в состав материала, чтобы предотвратить его окисление. Ингибиторы коррозии образуют на поверхности металла защитную пленку, которая замедляет процесс окисления.
Гальваническая защита. Гальваническая защита является электрохимическим методом защиты металлов от окисления. Она основана на принципе гальванической пары, когда два металла разного электрохимического потенциала вместе подвергаются коррозии, но один из них окисляется более активно. Таким образом, один металл служит жертвенным, защищая другой металл от окисления.
Управление окружающей средой. Один из способов защиты металлов от окисления - контроль окружающей среды. Уменьшение содержания кислорода, влаги и агрессивных химических веществ в окружающей среде может существенно замедлить процесс окисления металлов. Регулярное проветривание помещений, использование уплотнительных материалов и специальных покрытий для предотвращения проникновения влаги и кислорода, а также удаление агрессивных веществ - все это способы защиты металлов от окисления.
Специальные сплавы. Разработка и использование специальных сплавов - еще один метод защиты металлов от окисления. В специальных сплавах добавлены примеси, которые предотвращают окисление. Эти сплавы обладают высокой стойкостью к коррозии и служат для изготовления конструкций и деталей, которые подвержены агрессивным средам и высокой влажности.
Пассивация. Некоторые металлы могут быть пассивированы, то есть образовать пленку оксида на поверхности, которая предотвращает дальнейшее окисление. Например, нержавеющая сталь образует на своей поверхности пассивную пленку хромового оксида, которая защищает металл от коррозии. Для достижения пассивации чаще всего используются оксидирующие средства или электрохимические методы.
Окисление металлов в природе и быту

Окисление металлов является естественным процессом, который протекает постоянно в природе. Многие металлы, вступая в реакцию с кислородом, образуют оксиды, получающиеся в результате окисления. Некоторые из таких металлов, такие как алюминий и железо, обладают высокой коррозионной стойкостью благодаря образованию защитной пленки оксида на поверхности, которая предотвращает дальнейшее окисление.
Одеяние окислительной реакцией могут также покрытия из металлов, которые используются в быту. Например, медные предметы со временем приобретают зеленоватую патину, которая образуется в результате окисления меди. Это является естественным процессом и не влияет на структурную прочность металла.
Другой пример – серебро. Серебряные украшения со временем теряют свой блеск, так как серебро вступает в реакцию с воздухом, образуя серебряную серу. Чтобы предотвратить окисление серебра, украшения могут покрываться специальным слоем лака или храниться в специальных плотно закрытых контейнерах.
В природе также можно наблюдать окисление разных металлов. Например, пирит (железная сера) окисляется влажным воздухом и трансформируется в серную кислоту. Благодаря этому процессу образуются красивые золотистые кристаллы.
В целом, окисление металлов встречается повсеместно и играет важную роль в различных сферах нашей жизни – от природных процессов до бытовых применений металлических изделий.
Вопрос-ответ

Какие из цветных металлов подвержены окислению?
Окисление может происходить у таких цветных металлов, как медь, алюминий, олово, кобальт, марганец и др.
Почему цветные металлы окисляются?
Окисление металлов происходит из-за взаимодействия металла с кислородом из воздуха. При этом на поверхности металла образуется слой оксида или других окислов, что приводит к изменению его цвета.
