Атомная кристаллическая решетка - это способ, с помощью которого атомы упорядочиваются в трехмерном пространстве, образуя кристаллы. Кристаллическая решетка может быть образована различными элементами, в том числе и металлами.
Однако, не все металлы могут образовывать атомную кристаллическую решетку. В металлах атомы располагаются в ионной решетке с положительно заряженными ионами ядра и свободными электронами, которые движутся между ионами. Это позволяет металлам быть проводниками электричества и тепла.
Основные металлы, которые образуют атомную кристаллическую решетку, - это щелочные металлы, щелочноземельные металлы и некоторые переходные металлы. Например, натрий, калий, магний и алюминий образуют атомную кристаллическую решетку.
В итоге, атомная кристаллическая решетка в металлах играет важную роль в их свойствах и поведении. Она определяет прочность, пластичность и другие механические свойства металла, а также влияет на его проводимость и теплопроводность.
Металлы с атомной кристаллической решеткой:
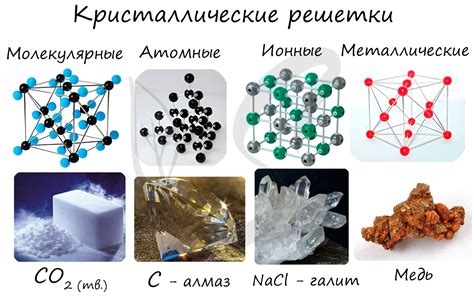
Атомная кристаллическая решетка - это особая структура, которую образуют атомы в металле. Здесь каждый атом занимает свое строго определенное место, образуя регулярную трехмерную сетку.
Одним из примеров металлов с атомной кристаллической решеткой являются железо и его сплавы. Железо имеет кубическую решетку со структурой body-centered cubic (BCC), что означает, что каждый атом железа расположен в центре своего кубического ячейки, а также связан с восьмерью соседних атомов.
Другим примером металлов с атомной кристаллической решеткой является алюминий. Алюминий имеет кубическую решетку, но с другой структурой, называемой face-centered cubic (FCC). В этой структуре каждый атом располагается в вершинах куба и на поверхности каждой грани куба.
Также стоит упомянуть металлы с гексагональной решеткой, такие как магний и цирконий. В гексагональной решетке каждый атом располагается в центре шестиугольных ячеек, образующих трехмерную сетку.
Описанные примеры лишь небольшая часть металлов с атомной кристаллической решеткой. Всего существует множество различных структур, которые образуют атомы металлов, и каждая из них имеет свои особенности и свойства.
Железо:

Железо – это металл, у которого атомная кристаллическая решетка имеет простую кубическую структуру. В каждом узле кристаллической решетки находится атом железа, окруженный восемью ближайшими соседями. Эта структура делает железо твердым и прочным материалом.
Ферромагнитные свойства железа также связаны с его кристаллической решеткой. Ниже температуры Кюри (770 °C) железо обладает спонтанной магнитной намагниченностью, которая сохраняется даже после удаления внешнего магнитного поля. Это объясняется ориентацией магнитных моментов атомов железа в одном направлении благодаря согласованной структуре кристаллической решетки.
В кристаллической решетке железа также происходит фазовое превращение при нагревании и охлаждении. При температуре Т1 происходит превращение гамма-железа (гранецентрированная кубическая решетка) в аустенит. При дальнейшем нагревании при температуре Т2 происходит превращение аустенита в альфа-железо (простая кубическая решетка).
Из-за простой кубической структуры кристаллической решетки железо имеет ряд особенностей. Например, оно образует кристаллы, плоскости которых расположены параллельно поверхности раздела с другими материалами. Это позволяет использовать железо для создания предметов с резкими краями и гранями, таких как ножи, инструменты и строительные конструкции.
Алюминий:

Алюминий является одним из самых распространенных металлов в земной коре. Он обладает атомной кристаллической решеткой, что означает, что его атомы организуются в упорядоченную двумерную или трехмерную структуру.
Атомы алюминия образуют кристаллическую решетку, состоящую из слоев, в которых каждый атом окружен шестью ближайшими соседями. Эти слои располагаются регулярно и создают структуру, которая обеспечивает прочность и стабильность металла.
Алюминий также отличается высокой проводимостью тепла и электричества. Это свойство обусловлено его атомной решеткой, которая позволяет электронам свободно передвигаться внутри металла. Благодаря этому алюминий является важным материалом для производства электрических проводов и теплообменников.
Кроме того, алюминий обладает хорошей коррозионной стойкостью благодаря образованию на его поверхности защитной оксидной пленки. Эта пленка образуется благодаря реакции алюминия с воздухом и предотвращает дальнейшую окислительную реакцию.
Медь:

Медь - это химический элемент, который имеет атомный номер 29 и символ Cu. Он принадлежит к группе переходных металлов и является одним из самых важных металлов в промышленности.
Медь характеризуется атомной кристаллической решеткой, которая образуется благодаря регулярному расположению атомов меди в пространстве. В этой решетке атомы меди соединяются друг с другом через свои электроны, образуя кристаллическую структуру. Эта структура обладает высокой устойчивостью и силой, делая медь прочным и прочным материалом.
Медь имеет высокую теплопроводность и электропроводность, что является одной из его главных причин использования в различных электрических и энергетических системах. Кроме того, медь имеет низкую склонность к окислению и коррозии, что делает его идеальным материалом для производства труб, проводов и различных электронных компонентов.
Медь также широко используется в производстве ювелирных изделий и украшений. Его прочность, блеск и способность сохранять свою форму делают его популярным материалом для создания украшений различных стилей и дизайнов.
В целом, медь является одним из наиболее важных металлов в современной промышленности, благодаря своим уникальным свойствам и атомной кристаллической решетке, которая обеспечивает его прочность и стойкость ко многим факторам внешней среды.
Свинец:

Свинец – химический элемент из группы постпереходных металлов, обозначенный символом Pb и имеющий атомный номер 82. Он является одним из наиболее плотных и тяжелых известных элементов.
Атомная кристаллическая решетка свинца имеет кубическую структуру. В каждом узле этой структуры находится атом свинца. Свинец образует идеальную кристаллическую решетку, где атомы занимают строго определенные позиции в пространстве.
Свинец является мягким металлом с низкой температурой плавления. При комнатной температуре он обладает гибкостью и может быть легко деформирован. Это связано с особенностями его кристаллической решетки.
Свинец имеет низкую электропроводность и хорошо поглощает рентгеновские лучи. Именно благодаря этим свойствам свинец активно применяется в медицине, в производстве аппаратуры для генерации рентгеновских лучей и защиты от них.
Никель:

Никель - химический элемент с атомным номером 28 в периодической системе, который относится к переходным металлам. У никеля атомная кристаллическая решетка, что делает его одним из металлов с характерным кристаллическим строением.
Атомы никеля образуют компактную решетку, в которой каждый атом имеет окружение из шести ближайших соседей. Это обусловлено тем, что никель имеет кубическую гранцентрированную третичную структуру - каждый атом находится в центре кубической ячейки, а в углах находятся атомы других элементов.
В атомной кристаллической решетке никеля имеются свободные электроны, что объясняет его высокую проводимость электричества и тепла. Никель также обладает высокой механической прочностью и стойкостью к коррозии, что делает его полезным материалом в различных отраслях промышленности.
Никель широко используется в производстве металлургических и химических изделий, в производстве магнитных материалов, в электронике и электротехнике, а также в производстве легированных сталей. Свойства никеля, обусловленные его атомной кристаллической решеткой, делают его одним из важных и востребованных металлов на мировом рынке.
Вопрос-ответ

Какая структура у атомной кристаллической решетки?
Атомная кристаллическая решетка имеет упорядоченную и регулярную структуру, где атомы располагаются в узлах кристаллической решетки.
Какие металлы образуют атомную кристаллическую решетку?
Многие металлы образуют атомную кристаллическую решетку, например, железо, алюминий, медь, свинец, цинк и другие.
Какие свойства имеют металлы с атомной кристаллической решеткой?
Металлы с атомной кристаллической решеткой обладают хорошей проводимостью электричества и тепла, высокой пластичностью и прочностью. Они обычно имеют блестящую поверхность и способность формировать различные сложные формы.
Какая роль атомной кристаллической решетки в свойствах металлов?
Атомная кристаллическая решетка играет важную роль в формировании свойств металлов. Она определяет их структурную упорядоченность, электронную структуру, механические свойства и многие другие характеристики.
