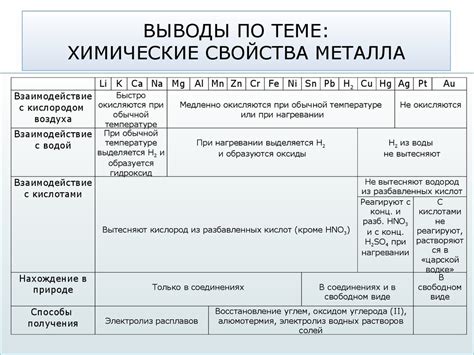
Кислоты – это химические соединения, которые обладают свойством давать водным растворам положительную электрическую реакцию. Они могут оказывать разрушительное воздействие на многие материалы, включая металлы. Однако существуют и такие металлы, которые обладают устойчивостью к воздействию кислотных растворов и могут использоваться в агрессивных химических средах без опасности и разрушения.
Одним из самых устойчивых кислотам металлов является золото. Это благородный металл, который не реагирует с большинством кислотных растворов, включая концентрированную серную, азотную и хлороводородную кислоты. Золото широко используется в химической промышленности и лабораториях, где требуется стойкость к агрессивным средам.
Еще одним металлом, устойчивым к воздействию кислотных растворов, является платина. Этот металл обладает высокой коррозионной стойкостью и способностью не растворяться при взаимодействии с кислотами. Платина широко применяется в химии, электронике, медицине и других отраслях, где требуется материал, устойчивый к химическому воздействию.
Еще одним металлом, способным выдержать воздействие кислотных растворов, является стальная нержавеющая сталь. Она состоит из железа, хрома, никеля и других сплавов, которые придают ей устойчивость к коррозии. Нержавеющая сталь широко используется в пищевой промышленности, химической промышленности и других сферах, где требуется материал с высокой степенью защиты от коррозии.
Определение устойчивости металлов к кислотам

Устойчивость металлов к воздействию кислотных растворов является важным параметром при выборе материала для конкретной задачи. Для определения этой устойчивости проводятся различные испытания и эксперименты.
Одним из методов определения устойчивости металлов к кислотам является измерение электрохимического потенциала материала. По этому показателю можно судить о скорости коррозионных процессов и степени повреждения металла при воздействии кислоты.
Другим методом является измерение массы металла до и после его взаимодействия с кислотным раствором. По изменению массы можно оценить степень коррозии и устойчивость материала к кислотам. Для этого проводятся специальные эксперименты, в которых металл погружается в кислотный раствор и взвешивается до и после воздействия.
Также существуют стандартные методы испытания, устанавливающие нормы устойчивости металлов к кислотам. Например, такие параметры, как pH-значение кислотного раствора, время воздействия и температура, могут быть установлены в соответствии с требованиями стандарта.
Полученные при проведении экспериментов данные о показателях устойчивости металлов к кислотам могут быть представлены в виде таблицы с указанием соответствующих значений для каждого материала. Такой подход позволяет сравнить различные металлы и выбрать наиболее подходящий для конкретной задачи.
Влияние кислотных растворов на металлы

Металлы, устойчивые к воздействию кислотных растворов, играют важную роль в различных отраслях промышленности. Это связано с их способностью выдерживать агрессивные условия и сохранять свои характеристики в контакте с кислотами.
Реакция металлов на воздействие кислотных растворов зависит от их химической природы. Некоторые металлы проявляют сильную реакцию с кислотами, в то время как другие металлы мало подвержены коррозии.
Кислотные растворы могут вызывать различные процессы взаимодействия с металлами. Например, в результате коррозии могут образовываться соединения, которые препятствуют дальнейшему распространению коррозионного процесса. Также некоторые металлы могут образовывать защитные покрытия на поверхности при взаимодействии с кислотами.
Одним из примеров металлов, устойчивых к воздействию кислотных растворов, является нержавеющая сталь. Она обладает высокой стойкостью к различным видам кислот, таким как соляная, серная и многие другие. Это делает нержавеющую сталь широко применяемым материалом в химической промышленности, медицине и других отраслях.
Ссылки между металлами и их стойкостью к кислотам

Металлы обладают различной степенью устойчивости к воздействию кислотных растворов. Это связано с их химическими свойствами и структурой кристаллической решетки. Некоторые металлы проявляют высокую устойчивость к кислотам и могут использоваться для хранения и транспортировки агрессивных химических веществ.
Коррозионная стойкость металлов обусловлена их способностью образовывать защитные оксидные пленки, которые предотвращают проникновение кислоты в металлическую структуру. Например, нержавеющие стали содержат хром, который образует плотную и прочную оксидную пленку на поверхности, предотвращающую дальнейшую коррозию.
Однако не все металлы обладают стойкостью к кислотам. Некоторые металлы, такие как железо или цинк, могут подвергаться активной коррозии при контакте с кислотными растворами. Это связано с тем, что такие растворы могут разрушать защитную пленку на поверхности металла и активировать его коррозию.
Таблица ниже представляет некоторые металлы и их стойкость к различным кислотам:
| Металл | Соляная кислота (HCl) | Азотная кислота (HNO3) | Серная кислота (H2SO4) |
|---|---|---|---|
| Золото | устойчив | устойчив | устойчив |
| Платина | устойчив | устойчив | устойчив |
| Алюминий | разрушение оксидной пленки | разрушение оксидной пленки | разрушение оксидной пленки |
| Железо | коррозия | коррозия | коррозия |
Из таблицы видно, что золото и платина проявляют высокую устойчивость к различным кислотам, в то время как алюминий, железо и другие металлы могут быть подвержены коррозии при их воздействии. Это важно учитывать при выборе материала для конкретной задачи, связанной с контактом с кислотами.
В заключение, стойкость металлов к кислотам зависит от их химических свойств и способности образовывать защитные оксидные пленки. Правильный выбор материала может обеспечить долговечность и безопасность при работе с кислотными растворами.
Коррозия металлов под воздействием кислотных растворов

Коррозия металлов под воздействием кислотных растворов является распространенным и серьезным процессом разрушения материалов. Кислотные растворы могут оказывать агрессивное воздействие на различные металлы, вызывая их коррозию и постепенное разрушение.
Факторы, влияющие на коррозию металлов в кислотных средах, включают концентрацию и pH раствора, тип кислоты, температуру и наличие других химических соединений. Высокая концентрация кислоты обычно усиливает коррозионные процессы, а низкое pH может привести к активной диссоциации воды, образованию ионов водорода и ускорению реакции коррозии.
Одним из наиболее устойчивых к кислотной коррозии металлов является нержавеющая сталь. Благодаря высокому содержанию хрома, она образует пассивную оксидную пленку, которая защищает металл от дальнейшей коррозии. Также к этой группе относятся медные сплавы, в которых на поверхности образуется оксидная пленка, препятствующая контакту металла с кислотным раствором.
Однако некоторые металлы, такие как алюминий и цинк, довольно чувствительны к кислотной коррозии. Под воздействием кислот они могут разрушаться с образованием пузырей и трещин на поверхности. Для защиты таких металлов часто применяют покрытия и пленки, которые призваны предотвратить их контакт с кислотной средой.
Ионная реакция между металлом и кислотным раствором

Металлы, устойчивые к воздействию кислотных растворов, проявляют специфическую реакцию при контакте с кислотным окружением. Эта реакция основана на обмене ионами между металлом и кислотой, что приводит к образованию соответствующих солей.
При взаимодействии металла с кислотой происходит растворение его поверхности, при этом происходит образование ионов металла и протонов H+. Ионы металла, имея положительный заряд, становятся растворимыми в кислотном растворе, образуя соответствующую металлическую соль.
Ионная реакция между металлом и кислотным раствором может быть представлена следующим уравнением:
M + HX → MX + H₂
Где M - металл, HX - кислота, MX - металлическая соль.
Примерами таких реакций могут служить реакции цинка (Zn) и соляной кислоты (HCl), алюминия (Al) и серной кислоты (H₂SO₄), железа (Fe) и азотной кислоты (HNO₃). В результате этих реакций образуются соответствующие соли: хлорид цинка (ZnCl₂), сульфат алюминия (Al₂(SO₄)₃) и нитрат железа (Fe(NO₃)₃).
Таким образом, ионная реакция между металлом и кислотным раствором представляет собой важный процесс, который имеет множество практических применений, включая производство различных соединений, электрохимические процессы и другие области науки и техники.
Отличительные свойства металлов, устойчивых к кислотам
1. Резистентность к коррозии: Металлы, устойчивые к кислотам, обладают высокой степенью резистентности к коррозии. Они не окисляются и не теряют своих механических свойств под воздействием кислотных растворов, что делает их незаменимыми для использования в агрессивных средах.
2. Устойчивость к высоким температурам: Металлы, устойчивые к кислотам, отличаются способностью сохранять свои свойства и прочность даже при высоких температурах. Это связано с тем, что они обладают высокой температурной стабильностью и не подвержены деформациям или плавлению при воздействии кислотных растворов.
3. Химическая инертность: Металлы, устойчивые к кислотам, обладают высокой степенью химической инертности, что означает их небольшую реакционную способность с кислотами. Это делает их стабильными и надежными материалами для использования в различных промышленных процессах, где требуется контакт с кислотными средами.
4. Долговечность: Металлы, устойчивые к кислотам, обладают высокой степенью долговечности и стойкости к воздействию кислотных растворов. Они не подвержены коррозии, ржавлению или другим видам разрушения, что делает их идеальным выбором для использования во многих отраслях промышленности, таких как химическая, нефтегазовая, а также в производстве емкостей и трубопроводов для кислотных сред.
Окислительная способность кислотных растворов и ее влияние на металлы
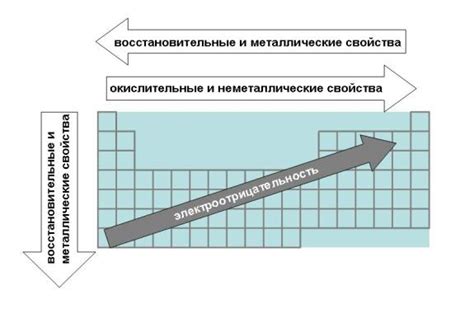
Окислительная способность кислотных растворов является важным фактором, определяющим степень воздействия этих растворов на металлы. Окислительные свойства кислотных растворов связаны с их способностью принимать электроны от веществ, вступающих в реакцию с ними.
Металлы могут быть различных степеней устойчивости к окислительной способности кислотных растворов. Некоторые металлы, такие как золото и платина, не подвергаются окислению при взаимодействии с большинством кислотных растворов. Они обладают высокой степенью стабильности и устойчивости к окислительному воздействию.
Другие металлы, такие как железо и алюминий, более подвержены окислению в кислотных растворах. Это происходит из-за их низкой степени стабильности и способности отдавать электроны окислителю в виде кислоты. При взаимодействии с кислотным раствором эти металлы подвергаются окислительной реакции, которая может привести к образованию оксидов или солей.
Уровень окислительной способности кислотных растворов может быть оценен при помощи потенциала окислительно-восстановительного электрода. Этот показатель позволяет сравнивать величину окислительных свойств различных кислотных растворов и предсказывать их влияние на металлы.
Важно учитывать окислительные свойства кислотных растворов при выборе материала для конкретного приложения. При использовании металла в условиях, когда он будет подвержен воздействию кислотных растворов, необходимо выбирать металлы с высокой степенью устойчивости к окислению. Использование неподходящего металла может привести к его коррозии и образованию нестабильных соединений, что может негативно сказаться на работоспособности и долговечности изделия.
Примеры металлов, устойчивых к воздействию кислотных растворов:
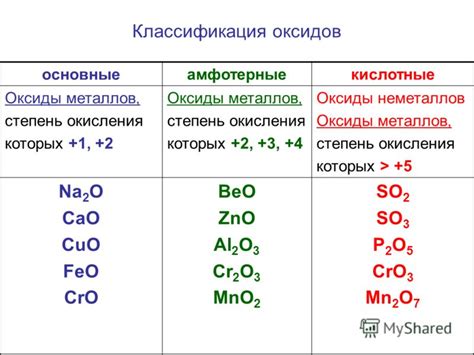
1. Золото
Золото является одним из наиболее устойчивых металлов к воздействию кислотных растворов. Оно не реагирует с сильными кислотами, такими как серная или соляная кислота. Благодаря этой химической устойчивости, золото широко используется в ювелирных изделиях и электронике.
2. Платина
Платина также отличается высокой устойчивостью к кислотам. Подобно золоту, она не реагирует с сильными кислотами, что делает ее ценным и востребованным материалом в различных отраслях, включая производство автомобилей и химическую промышленность.
3. Серебро
Серебро обладает химической устойчивостью к некоторым кислотам, особенно к слабым кислотам, таким как уксусная кислота. Однако сильные кислоты, например, соляная кислота, могут вызвать коррозию серебра. Эта особенность применяется в различных промышленных процессах, включая фотографию и электротехнику.
4. Нержавеющая сталь
Нержавеющая сталь обладает химической устойчивостью к кислотам благодаря примеси хрома, который образует защитную пленку на поверхности металла. Этот материал широко используется в промышленности, строительстве и производстве кухонных приборов.
5. Титан
Титан является металлом с высокой химической устойчивостью, включая устойчивость к кислотам. Он не реагирует с большинством кислот, таких как серная или соляная кислота. Из-за этой устойчивости, а также его легкости и прочности, титан широко используется в авиационной и аэрокосмической промышленности, а также в медицинских имплантатах.
Таким образом, существует несколько металлов, которые проявляют высокую устойчивость к воздействию кислотных растворов. Золото, платина, серебро, нержавеющая сталь и титан являются примерами таких металлов и находят широкое применение в различных отраслях промышленности и технологии.
Нержавеющая сталь

Нержавеющая сталь – это сплав железа с хромом, никелем и другими элементами, обладающий высокой устойчивостью к коррозии в кислотных растворах и окружающей среде. Основными составляющими нержавеющей стали являются хром и никель, которые способствуют формированию плотной и прочной оксидной пленки на поверхности материала.
Преимущества нержавеющей стали заключаются в ее долговечности, стойкости к коррозии и возможности применения в различных условиях эксплуатации. Этот материал широко используется в разных отраслях, включая пищевую, фармацевтическую, химическую и энергетическую промышленности, а также в производстве сантехники и бытовой техники.
Нержавеющая сталь обладает высокой устойчивостью к кислотным растворам различной концентрации и температуры. Она способна выдерживать воздействие таких кислот, как серная, соляная, азотная, фосфорная и многих других. Такая стойкость позволяет использовать нержавеющую сталь для изготовления емкостей, трубопроводов и других элементов, которые будут контактировать с кислотами в процессе хранения и транспортировки.
Важно отметить, что нержавеющая сталь имеет разные марки, каждая из которых имеет свои особенности. Например, марка 304, или 18/8, содержит 18% хрома и 8% никеля, что обеспечивает хорошую устойчивость к коррозии и хорошую свариваемость. Марка 316L, или медицинская сталь, содержит 16-18% хрома, 10-14% никеля и 2-3% молибдена, что придает ей еще большую устойчивость к коррозии и улучшенные механические свойства.
- Нержавеющая сталь – универсальный материал для различных отраслей промышленности.
- Она обладает высокой устойчивостью к воздействию кислотных растворов различной концентрации и температуры.
- Марки нержавеющей стали имеют разные химические составы, что позволяет выбрать оптимальный вариант для конкретных условий эксплуатации.
Вопрос-ответ

Какие металлы устойчивы к кислотным растворам?
Металлы, устойчивые к кислотным растворам, включают такие элементы, как золото, платина, свинец, нержавеющая сталь, алюминий и титан. Они проявляют высокую устойчивость к коррозии и не подвергаются разрушению при контакте с кислотами.
Для чего нужны металлы, устойчивые к кислотным растворам?
Металлы, устойчивые к кислотным растворам, широко применяются в различных областях, где требуется контакт с кислотами. Например, они используются в производстве химической и пищевой промышленности, в лабораторных испытаниях и исследованиях, а также в производстве лекарств и косметики.
Почему металлы, устойчивые к кислотам, не подвергаются коррозии?
Металлы, устойчивые к кислотным растворам, обладают особой структурой и химической стойкостью, которая защищает их от коррозии. Например, золото и платина не реагируют с большинством кислот, так как они химически инертны. Нержавеющая сталь содержит хром, который образует защитную оксидную пленку на поверхности металла, предотвращающую его разрушение.
Какие кислоты могут повредить металлы?
Хотя металлы, устойчивые к кислотным растворам, обладают высокой химической стойкостью, некоторые кислоты все же могут вызвать коррозию или повредить их поверхность. Например, концентрированные серная кислота и азотная кислота могут атаковать свинец и алюминий. Однако, в большинстве случаев, устойчивые металлы показывают минимальную реакцию при контакте с кислотами.
