Металлы - это особый класс веществ, обладающих рядом уникальных свойств, одно из которых заключается в особенности связи между атомами. Атомы металлов в кристаллической решетке устанавливают неординарные связи, приводящие к формированию особой структуры, которая придает металлам их характерные физические и химические свойства. Особенности связи между атомами являются главным фактором, определяющим поведение металлов в различных условиях и их взаимодействие с окружающей средой.
Главным элементом в структуре металлов является кристаллическая решетка, которая состоит из слоев атомов, расположенных регулярно и симметрично друг относительно друга. Образование такой решетки обусловлено особенностями связи между атомами в металлах. В отличие от других веществ, металлы обладают так называемыми "свободными" электронами, которые перемещаются между атомами и образуют облако электронов внутри металлической структуры.
Эти свободные электроны осуществляют связь между атомами в металлах и придают им характерные свойства. Они обеспечивают электропроводность металлов, их теплопроводность, пластичность и другие ключевые характеристики. Свободные электроны также ответственны за способность металлов к формированию металлических связей с другими элементами и соединениями. Благодаря связи между атомами в металлах, эти вещества обладают высокой прочностью и долговечностью, что делает их незаменимыми для множества промышленных и технических приложений.
Изучение особенностей связи между атомами в металлах имеет огромное значение для развития материаловедения и создания новых веществ с уникальными свойствами. Понимание связи между атомами позволяет не только улучшить характеристики и прочность металлов, но и разрабатывать новые материалы с определенными электронными, магнитными и каталитическими свойствами. В будущем, изучение связи между атомами в металлах увеличит наши возможности в области технологий, энергетики, микроэлектроники и других отраслях науки и промышленности.
Металлы: связь между атомами
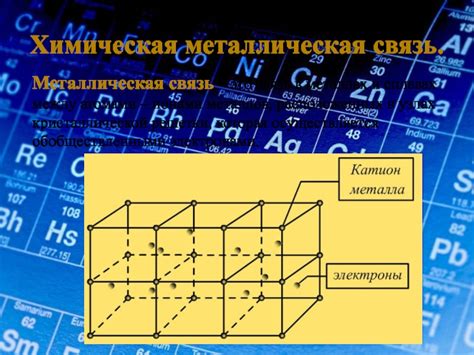
Металлы являются одним из основных классов элементов, которые обладают особыми свойствами, такими как хорошая электропроводность, теплопроводность, пластичность и стойкость к коррозии. Эти свойства металлы приобретают благодаря своей уникальной структуре и связи между атомами.
Основным типом связи между атомами в металлах является металлическая связь. Это связь, при которой валентные электроны свободно перемещаются по всему кристаллическому решетчатому строению металлов. Именно благодаря этой свободе электронов металлы обладают свойствами электропроводности и теплопроводности.
Металлическая связь обусловлена большим количеством свободных электронов, которые образуют так называемое "море электронов". Этот механизм связи позволяет металлам легко проводить электрический ток и тепло. В то же время, благодаря свободе электронов, металлы обладают пластичностью и способностью подвергаться деформации без разрушения своей структуры.
Связь между атомами в металлах имеет не только физическое, но и химическое значение. Металлическая связь позволяет металлам образовывать разнообразные химические соединения и сплавы. Благодаря этому металлы широко используются в индустрии и строительстве, для создания различных материалов и конструкций. Металлическая связь также является причиной того, что металлы обычно обладают высокой плотностью и тугоплавкостью.
Основные свойства металлов
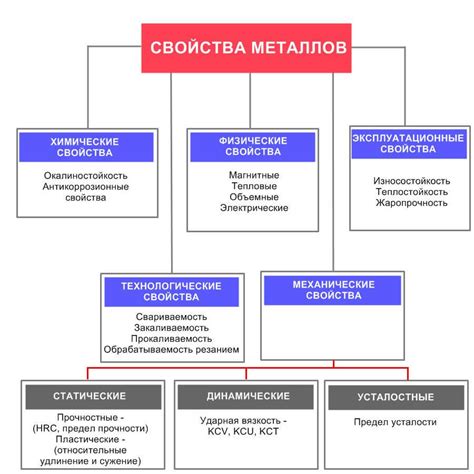
Электропроводность: Одним из основных свойств металлов является их способность проводить электрический ток. Это связано с наличием свободных электронов в их структуре, которые легко перемещаются под воздействием электрического поля.
Теплопроводность: Металлы отличаются высокой теплопроводностью, что означает способность быстро распространять тепло. Это особенно важно для применения металлов в различных технологических процессах, а также для создания материалов с повышенной теплоотдачей.
Пластичность: Металлы обладают высокой пластичностью, то есть способностью подвергаться формоизменению без разрушения. Благодаря этому свойству, металлы могут быть легко прокатаны, вытянуты, выкованы или отлиты в различные формы.
Металлический блеск: Металлы обладают характерным металлическим блеском, который связан с их способностью отражать свет. Это делает металлы привлекательными для использования в ювелирных изделиях и декоративных элементах.
Сильная связь между атомами: Связь между атомами в металлах обладает особыми свойствами. В результате, металлы обладают высокой прочностью и устойчивостью к механическим и химическим воздействиям. Это позволяет использовать металлы в различных областях, где требуется высокая надежность и долговечность материала.
Магнитные свойства: Некоторые металлы, такие как железо, никель и кобальт, обладают магнитными свойствами и могут быть намагничены или притянуты к магниту. Это явление называется ферромагнетизмом и является важным при создании магнитов и электромагнитов.
Строение металлической решетки
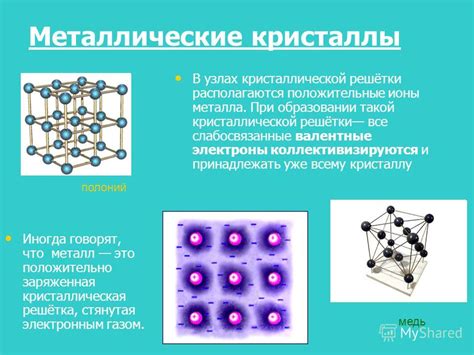
Металлические материалы обладают особыми свойствами, которые объясняются их строением на молекулярном уровне. Основной структурный элемент металлической решетки – это атом металла.
Атомы металла образуют кристаллическую решетку, которая отличается от других типов решеток. В металлической решетке атомы металла организованы в форме кубической или гексагональной сетки. Эти атомы соединены между собой с помощью металлических связей.
Металлические связи являются основой для понимания многих характеристик и свойств металлов. Они обеспечивают высокую электропроводность, теплопроводность, пластичность и прочность металлов. Металлические связи обусловлены способностью атомов металла обмениваться своими электронами с другими атомами.
Благодаря свободному движению электронов, металлы обладают характерными свойствами, такими как блеск, отличная электропроводность и теплопроводность. Отсутствие сильных связей между атомами позволяет металлам сохранять пластичность и принимать различные формы при обработке.
Строение металлической решетки играет ключевую роль в определении свойств и характеристик металлов. Понимание этого строения помогает не только в исследовании и разработке новых металлических материалов, но и в применении существующих металлов в различных отраслях промышленности.
Степень связи между атомами в металлах

Связь между атомами в металлах обладает определенными особенностями, которые отличают ее от связи в других типах веществ. Одной из главных особенностей является металлическая связь - тип связи, характерный исключительно для металлов.
Металлическая связь основана на перекрытии энергетических уровней валентных электронов между атомами металла. При этом электроны становятся общими для всех атомов металла и образуют так называемое "электронное море". Благодаря этой связи, металлы обладают высокой проводимостью электричества и тепла.
Степень связи между атомами в металлах может быть различной и зависит от таких факторов, как размер и форма атомов, наличие дефектов в кристаллической решетке, наличие примесей и т.д. Чем компактнее и регулярнее кристаллическая структура металла, тем сильнее связь между его атомами.
Важно отметить, что связь между атомами в металлах является металлической связью и не подразумевает образования молекул, как это характерно для неметаллов. В металлах атомы связаны между собой не отдельными химическими связями, а большим числом слабых связей между электронами и положительно заряженными ионами атомов.
Влияние связи между атомами на физические свойства металлов
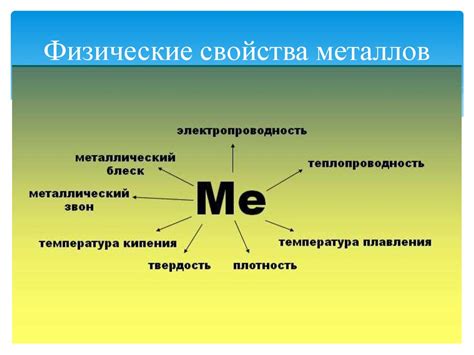
Связь между атомами играет важную роль в формировании физических свойств металлов. Она определяет их структуру и влияет на их механические и электрические характеристики.
Металлы обладают характерной кристаллической структурой, в которой атомы располагаются в регулярном и упорядоченном образе. Это обеспечивает металлам высокую прочность и устойчивость. Связь между атомами в металлах является металлической, что означает, что свободные электроны могут свободно перемещаться между атомами. Это дает металлам хорошую электропроводность и теплопроводность.
Связь между атомами также влияет на пластичность и тугоплавкость металлов. Когда в металле возникает внешнее воздействие, атомы смещаются и переходят в новое положение, что позволяет материалу деформироваться без разрушения. Это объясняет высокую пластичность металлов и их способность быть прокатываемыми или ковкими. Однако, связь между атомами в металлах также приводит к температурной зависимости их свойств, так как при нагреве атомы получают больше энергии и начинают более интенсивные колебания, что может приводить к размягчению и таянию металла.
Итак, взаимодействие и связь между атомами влияют на физические свойства металлов, определяют их механическую прочность, электрическую и тепловую проводимость, пластичность и тугоплавкость. Это делает металлы одними из самых важных и широко используемых материалов в промышленности и строительстве.
Значение связи между атомами для металлургии

Связь между атомами в металлах имеет огромное значение для металлургических процессов и получения качественной металлической продукции. Она обеспечивает прочность и устойчивость материала, а также его физические и химические свойства.
Одной из важнейших особенностей связи между атомами в металлах является их способность образовывать кристаллическую решетку. Это позволяет металлам быть упругими, что особенно важно при производстве строительных конструкций или пружин.
Более того, связь между атомами в металлах обеспечивает возможность проводить электрический ток. Это делает металлы основными материалами для электрической проводки и производства электронной техники.
Специфическая связь между атомами позволяет металлам обладать высокой пластичностью и способностью к деформации без разрушения. Это применяется при обработке металлических деталей – горячей и холодной штамповке, прокатке и литье.
Важным фактором связи между атомами в металлах является их влияние на температуру плавления и кристаллизацию. В зависимости от типа и структуры связей, металлы могут обладать высокой или низкой температурой плавления, что определяет возможность их плавления и использования в различных отраслях промышленности.
Взаимодействие связи между атомами с окружающей средой

Связь между атомами вещества играет важную роль во взаимодействии с окружающей средой. На связь между атомами влияют различные факторы: температура, давление, влажность, а также химические реакции с веществами, с которыми взаимодействует.
Один из основных факторов влияния окружающей среды на связь между атомами - это температура. При повышении температуры атомы начинают колебаться с большей амплитудой, что уменьшает силу связи и способствует распаду вещества. Например, при нагревании металлов их атомы начинают двигаться с большей скоростью, что приводит к повышению их энергии и переходу в состояние плавления или испарения.
Еще одной важной характеристикой взаимодействия связи между атомами с окружающей средой является давление. При высоком давлении атомы могут быть сжаты более плотно, что увеличивает силу связи и делает вещество более устойчивым. Например, при высоком давлении металлы могут образовывать специальные структуры, такие как кристаллические решетки, которые обладают высокой прочностью и твердостью.
Реакции с веществами окружающей среды также оказывают влияние на связь между атомами. Химические реакции могут приводить к образованию новых связей или разрыву существующих. Например, металлы могут реагировать с кислородом воздуха, образуя оксиды, которые имеют различные свойства по сравнению с исходным металлом. Это может привести к изменению механических, электрических и других свойств металла.
Проблемы и перспективы исследования связи между атомами в металлах

Связь между атомами в металлах является одной из ключевых тем в научных исследованиях, так как она определяет множество физических и химических свойств данных материалов. Одной из основных проблем при изучении связи между атомами в металлах является их высокая плотность и сложность структуры.
Для исследования связи между атомами в металлах используются различные методы, такие как рентгеновская дифракция и спектроскопия. Однако, эти методы имеют свои ограничения и не всегда позволяют получить полную информацию о связи между атомами. Также большой проблемой является сложность анализа экспериментальных данных.
В последние годы исследователям удалось достичь значительных успехов в изучении связи между атомами в металлах благодаря использованию современных методов моделирования и компьютерных технологий. Это открыло новые возможности для более глубокого понимания структуры металлов и развития новых материалов с уникальными свойствами.
В перспективе исследование связи между атомами в металлах позволит разработать новые методы синтеза и обработки материалов, что потенциально приведет к созданию более прочных, устойчивых к коррозии и токсичности металлов. Это особенно актуально в свете растущей потребности в разработке экологически чистых и энергоэффективных материалов для различных областей промышленности.
Вопрос-ответ

Какова особенность связи между атомами в металлах?
Металлы имеют особенность в своей связи между атомами, которая называется металлической связью. В металлической связи свободно перемещаются электроны между атомами металла, образуя так называемое "море электронов". Это обеспечивает устойчивость металлов и их некоторые уникальные свойства, такие как высокая электропроводность и теплопроводность.
Каково значение связи между атомами для металлов?
Связь между атомами в металлах имеет огромное значение. Благодаря металлической связи, металлы обладают высокой функциональностью и широким спектром применений. Например, высокая электропроводность и теплопроводность металлов позволяют использовать их в электронике и энергетике. Кроме того, металлы имеют высокую пластичность и прочность, что делает их идеальными материалами для строительства и производства различных изделий.
