Металлы – это материалы, которые активно используются в различных отраслях промышленности и строительства. Однако, под влиянием определенных факторов, металлы могут подвергаться процессу коррозии. Коррозия, или ржавление металла, является нежелательным процессом, который может привести к ухудшению качества и прочности металлических конструкций.
Одним из факторов, способствующих коррозии, является взаимодействие металла с кислотами. Кислоты могут разъедать металл, вызывая его деградацию и образование технических отложений, которые могут привести к потере формы и прочности металлической поверхности.
Существует несколько типов кислот, которые могут вызывать коррозию металла. Например, серная кислота (H2SO4) может разъедать металлы, такие как железо и сталь. Нитридная кислота (HNO3) также способна вызывать коррозию механических сплавов, таких как алюминий и медь. Важно отметить, что различные металлы и сплавы могут иметь разную стойкость к кислотам, что влияет на скорость и степень коррозии.
Сильные и слабые кислоты: различия

Кислоты - это химические соединения, способные отдавать протоны или протонированные ионы в растворе. Они играют важную роль в химических реакциях, включая разъедание металлов. Кислоты можно классифицировать на сильные и слабые в зависимости от их способности отдавать протоны.
Сильные кислоты - это кислоты, которые полностью диссоциируют в водном растворе, отдавая все доступные протоны. Например, серная кислота (H2SO4) и хлорноватистоводородная кислота (HCl) являются сильными кислотами.
Сильные кислоты имеют низкий pH и ярко выраженные кислотные свойства. Они могут причинять повреждение коже и тканям, а также вызывать коррозию металлов при контакте.
Слабые кислоты - это кислоты, которые не полностью диссоциируют в водном растворе и отдают только часть доступных протонов. Например, уксусная кислота (CH3COOH) и угольная кислота (H2CO3) являются слабыми кислотами.
Слабые кислоты имеют более высокий pH и менее выраженные кислотные свойства по сравнению со сильными кислотами. Они могут вызывать разъедание металлов, но требуют более длительного времени для этого процесса.
Важно отметить, что каждая кислота имеет свою уникальную реактивность и разъедающую способность. Некоторые металлы могут быть более подвержены влиянию конкретных кислот, чем другие. Поэтому при работе с кислотами необходимо соблюдать осторожность и использовать соответствующие меры безопасности.
Кислота, разъедающая металл: основные типы
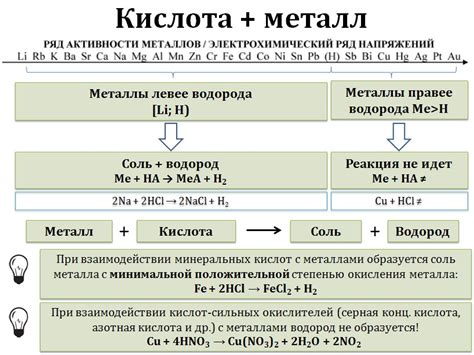
Разъедение металла кислотой - это химический процесс, при котором металлическая поверхность подвергается разрушению из-за реакции с кислотой. Существует несколько типов кислот, имеющих разъедающий эффект на металл.
Серная кислота является одной из самых распространенных кислот, способных разъедать металл. Она часто используется в промышленности и лабораторных условиях для удаления окислов и загрязнений с поверхности металла. Реакция между серной кислотой и металлом происходит с выделением сернистого газа и образованием раствора с солевыми соединениями.
Соляная кислота также обладает разъедающим действием на металлы. Эта кислота отличается высокой активностью и широким спектром применения. Соляная кислота реагирует с металлом, образуя соль и выделяя водород.
Азотная кислота действует на металлы более агрессивно в сравнении с серной и соляной кислотами. Азотная кислота имеет высокую окислительную активность и может разъедать большинство металлов. При взаимодействии с металлами азотная кислота образует нитраты и нитриты, выделяя водород и оксид азота.
Кроме основных типов кислот, разъедающих металл, существуют и другие кислоты, такие как фтороводородная кислота, хлороводородная кислота и другие. Каждая кислота имеет свою химическую активность и специфические свойства, поэтому их выбор зависит от конкретной задачи и типа металла, который необходимо разъедать.
Что происходит при взаимодействии кислоты и металла
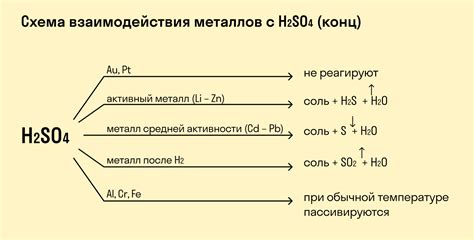
Взаимодействие кислоты и металла является химическим процессом, результатом которого является растворение металла в кислоте. При этом происходят несколько последовательных реакций.
Вначале кислота диссоциирует на ионы водорода и отрицательно заряженные ионы основной части кислоты. В то же время, поверхность металла покрывается окисной пленкой, которая защищает металл от коррозии. Однако, в наличии кислоты окисная пленка разрушается.
При попадании кислоты на металлическую поверхность происходит реакция окисления металла. Кислотные молекулы атакуют поверхность металла и осуществляют обмен ионами, в результате которого ионы металла переходят в раствор. Это приводит к образованию кислотного раствора из ионов металла и ионов кислоты.
Стоит отметить, что разные кислоты взаимодействуют с металлом по-разному. Например, соляная и серная кислоты довольно агрессивны и способны быстро растворять металлы. В то же время, уксусная кислота проявляет более слабое действие и способна растворить только определенные металлы.
В результате взаимодействия кислоты и металла образуется раствор, а металл теряет свои свойства и разрушается. Это явление широко используется в промышленности и научных исследованиях для обработки металлов и получения различных химических соединений.
Как кислота разъедает металл: реакция и образование соли

Кислота имеет способность разъедать металлы в результате химической реакции. При контакте с кислотой на металлической поверхности происходит окислительно-восстановительная реакция, в результате которой образуется соль. Эта реакция является примером химической коррозии металла.
Процесс разъедания металла кислотой начинается с образования ионов металла и водорода. Кислота выступает в роли окислителя, получая электроны от металла и превращая его в ионы. Одновременно водород исключается из кислоты в виде газа.
Реактивность кислот зависит от их свойств и концентрации. Некоторые кислоты, такие как соляная кислота (HCl) и серная кислота (H2SO4), обладают сильной реактивностью и могут разъедать широкий спектр металлов. Другие кислоты, например, уксусная кислота (CH3COOH) и фосфорная кислота (H3PO4), менее реактивны и разъедают только определенные металлы.
Образование соли является последним этапом реакции между кислотой и металлом. Когда ионы металла вступают в реакцию с ионами кислоты, образуются ионы соли. Соль обычно остается в растворе или, в случае коррозии металла, может образовывать твердое отложение на поверхности.
Примеры кислот, разъедающих металл
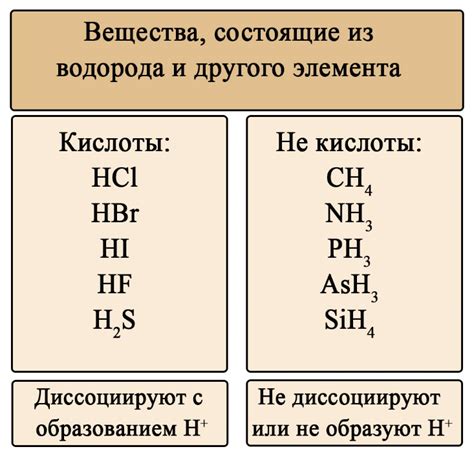
В мире существует множество кислот, способных разъедать металлы и вызывать их коррозию. Одной из таких кислот является серная кислота (H2SO4). Она широко применяется в промышленности и может разъедать большинство металлов, включая железо, медь и алюминий. При взаимодействии с серной кислотой, металлы теряют свою структурную целостность и покрываются слоем коррозии.
Другой кислотой, способной разъедать металл, является соляная кислота (HCl). Она также активно используется в промышленности и может разложить многие металлы, включая цинк, медь и никель. При контакте с соляной кислотой, металлы подвергаются химическим реакциям, в результате чего образуются соли и выделяется водородный газ.
Некоторые другие кислоты, способные разъедать металл, включают нитратную кислоту (HNO3), фтороводородную кислоту (HF) и перхлоровую кислоту (HClO4). Нитратная кислота обладает высокой реактивностью и может разлагать металлы, такие как медь, цинк и свинец. Фтороводородная кислота эффективно разъедает многие металлы, однако ее использование требует особой осторожности из-за ее высокой токсичности. Перхлоровая кислота также может разлагать металлы и обладает высокой степенью окислительности.
Необходимо иметь в виду, что взаимодействие кислот с металлами должно проходить с осторожностью и в соответствии с правилами безопасности, так как это может привести к различным реакциям и выделению опасных газов. Также следует учитывать, что разные металлы могут по-разному реагировать на кислоты, и для каждого случая необходимо учитывать конкретные условия и характеристики реагентов.
Как предотвратить разъедание металла кислотами: защитные меры

Разъедание металла кислотами может вызвать значительные проблемы и повлечь за собой серьезные последствия. Однако, существуют определенные меры, которые можно принять, чтобы предотвратить разрушение металлических конструкций и деталей под воздействием кислот.
1. Использование защитных покрытий: Нанесение на металлическую поверхность специальных защитных покрытий, таких как эмаль, лак, грунтовка и антикоррозийные составы, помогает предотвратить взаимодействие металла с кислотой. Эти покрытия создают защитный барьер, препятствующий проникновению кислоты на поверхность металла.
2. Использование устойчивых сплавов: Выбор правильного типа металла или сплава может значительно повысить его устойчивость к кислотным атмосферным условиям. При выборе материала для конструкции или детали следует обратить внимание на его химическую стойкость и реакцию с кислотами.
3. Контроль окружающей среды: Важно проводить регулярный контроль окружающей среды, в которой находятся металлические конструкции и детали. Предотвращение проникновения влаги и агрессивных кислот в окружающую среду поможет избежать разрушения металла.
4. Правильное использование хранилищ и контейнеров: При хранении кислот необходимо использовать специальные контейнеры из устойчивых к ним материалов, таких как стекло или пластик. Также следует обеспечить правильную вентиляцию и размещение контейнеров в специальных хранилищах, чтобы предотвратить разбрызгивание кислоты на металл.
5. Регулярное обслуживание и очистка: Регулярное обслуживание и очистка металлических поверхностей помогут предотвратить накопление ржавчины и коррозии. При обнаружении повреждений или аномального состояния поверхности металла, следует принять меры по его восстановлению и защите.
Применение этих защитных мер позволит длительное время сохранить металлические конструкции и детали в исходном состоянии, предотвратив их разъедание кислотами и сократив возможность возникновения аварийных ситуаций.
Влияние кислот на окружающую среду и здоровье человека

Кислоты - это химические вещества, обладающие растворяющими свойствами и способностью разрушать материалы. Они широко применяются в промышленности, в быту и науке. Но их использование может иметь негативное влияние на окружающую среду и здоровье человека.
Одно из основных негативных последствий использования кислот - загрязнение окружающей среды. Когда кислоты попадают в водные системы или почву, они могут вызывать кислотные дожди. Кислотные дожди представляют собой осадки, содержащие высокую концентрацию кислот, которые могут причинить вред растениям, животным и экосистемам в целом. Кроме того, кислотные дожди могут загрязнять водные ресурсы, делая их непригодными для питья и использования в сельском хозяйстве и промышленности.
Кроме загрязнения окружающей среды, кислоты могут оказывать и прямое влияние на здоровье человека. При контакте с кислотами, могут возникать ожоги и раздражения кожи, глаз и дыхательных путей. Длительное и частое воздействие кислот на организм может привести к хроническим заболеваниям, таким как бронхит, астма, аллергические реакции и проблемы с дыхательной системой.
Однако, не все кислоты обладают одинаковым уровнем опасности. Некоторые кислоты, такие как соляная кислота и серная кислота, являются ядовитыми и крайне опасными для использования. В то же время, другие кислоты, такие как лимонная кислота или уксусная кислота, безопасны для использования в быту и пищевой промышленности.
В целях безопасности и защиты окружающей среды регулирующие организации устанавливают нормативы и ограничения на использование кислот. Также важно правильно утилизировать отработанные кислоты и следовать предосторожностям при работе с кислотами, чтобы минимизировать риски для окружающей среды и здоровья человека.
Выводы и рекомендации

Исходя из изученных данных, можно сделать следующие выводы:
- Кислоты могут разъедать металлы, образуя соответствующие соли и выделяя водород.
- Способность кислот разъедать металлы зависит от их концентрации и химической природы. Некоторые кислоты, такие как серная и соляная, являются достаточно сильными окислителями и способны разрушить различные металлы.
- Реакция разъедания металла кислотой может протекать с различной интенсивностью в зависимости от условий, таких как температура и наличие примесей.
- В каждом конкретном случае целесообразно проводить предварительное тестирование и анализ, чтобы определить и подобрать наиболее подходящую кислоту для разъедания конкретного металла.
Основываясь на этих выводах, можно дать следующие рекомендации:
- При работе с кислотами, необходимо соблюдать соответствующие меры безопасности, такие как ношение защитной одежды, очков и перчаток, проведение работ в хорошо проветриваемом помещении.
- При выборе кислоты для разъедания металла, рекомендуется обратить внимание на ее концентрацию, химическую природу и специфичные свойства, а также наличие альтернативных методов обработки металла.
- Кроме того, следует учитывать возможные последствия разъедания металла кислотой, такие как образование токсичных газов или загрязнение окружающей среды.
- Проведение тестов на небольших образцах металла перед применением крупномасштабных процессов может позволить установить оптимальные параметры для эффективного разъедания металла кислотой.
Соблюдение указанных рекомендаций поможет уменьшить риск возникновения аварийных ситуаций и повысить эффективность процессов разъедания металла с использованием кислоты.
Вопрос-ответ

Какая кислота разъедает металл?
Разъедающую способность кислоты зависит от ее химического состава и концентрации. Некоторые кислоты, такие как хлороводородная кислота (HCl), серная кислота (H2SO4) и азотная кислота (HNO3), являются агрессивными и могут разъедать различные металлы при взаимодействии с ними.
Как кислота разъедает металл?
Когда кислота взаимодействует с металлом, она может реагировать с поверхностными слоями металла, образуя соли и выделяя газы в результате химической реакции. Например, хлороводородная кислота (HCl) реагирует с железом (Fe) и образует хлорид железа (FeCl2) и водород (H2).
Может ли кислота разъедать все металлы?
Нет, не все металлы разъедаются кислотами. Реакция металла с кислотой зависит от его реакционной способности и электрохимического потенциала. Например, золото (Au) и платина (Pt) являются химически инертными и не растворяются в большинстве кислот, в то время как щелочные металлы, такие как натрий (Na) и калий (K), реагируют с водой при образовании щелочей и выделении водорода.
