Вода является одним из основных растворителей, используемых в химических реакциях и промышленности. Взаимодействие воды с металлами средней активности является одной из важных тем в химии. Это взаимодействие может происходить как в атмосфере, в природных водоемах, так и в промышленных процессах. Результаты этого взаимодействия могут быть различными и зависят от конкретных условий и характеристик металлов.
Когда металлы средней активности взаимодействуют с водой, они могут образовывать различные соединения и реагенты. Некоторые металлы могут образовывать оксиды, гидроксиды или соли, которые могут оказывать влияние на качество воды и ее химический состав. В таких случаях важно учитывать степень активности металлов и условия их взаимодействия с водой.
Другие металлы средней активности могут проявлять свойства катализаторов и играть важную роль в различных процессах окисления и восстановления. Они могут активировать молекулярный кислород и способствовать разложению органических соединений в воде. Такие реакции имеют большое значение для экологии и промышленных процессов.
Изучение взаимодействия воды с металлами средней активности является важной задачей современной науки. Оно позволяет понять и предсказать последствия таких взаимодействий, а также разработать эффективные методы очистки и обезвреживания воды. Это важно не только с точки зрения охраны окружающей среды, но и для обеспечения безопасности и качества питьевой воды.
Роль воды при взаимодействии с металлами средней активности

Вода играет важную роль при взаимодействии с металлами средней активности. Она может быть как реагентом в химических реакциях, так и средой, в которой происходят эти реакции.
При реакции металлов с водой образуется гидроксид соответствующего металла и молекула воды. Это происходит в результате окислительно-восстановительной реакции, в которой металл отдает электроны, а молекула воды принимает их. Таким образом, вода выполняет функцию окислителя.
Вода также может быть средой, в которой происходят реакции между металлами. Например, при взаимодействии двух металлов в присутствии воды может возникнуть реакция диспропорционирования. В этой реакции один металл окисляется, а другой восстанавливается. Таким образом, вода предоставляет среду, в которой происходят эти процессы.
Кроме того, вода может участвовать в образовании растворов металлов. Металлы могут реагировать с водой, образуя ионы металла и связанные с ними анионы. Эти ионы и анионы вступают во взаимодействие с молекулами воды, образуя гидратированные ионы. Такие растворы металлов являются электролитическими и могут обладать специфическими свойствами.
Таким образом, вода играет важную роль при взаимодействии с металлами средней активности, выполняя функции реагента, среды и образования растворов. Ее взаимодействие с металлами способствует образованию новых соединений и процессам окисления-восстановления. Данное взаимодействие имеет большое значение как в практической химии, так и для понимания основных принципов взаимодействия веществ.
Активность металлов в присутствии воды

Вода взаимодействует с металлами средней активности, вызывая различные химические реакции. Данное взаимодействие может быть как самостоятельным, так и зависеть от условий окружающей среды, в которой происходит реакция.
Металлы средней активности погружаются в воду и начинают проявлять активность в виде реакции. Одним из ярких примеров такой реакции является окисление железа под воздействием кислорода воздуха и воды. Результатом этой реакции является образование ржавчины на поверхности металла.
Кроме ржавчины, вода может вызывать реакцию со многими другими металлами, такими как алюминий, цинк, магний и др. В результате этой реакции может образоваться оксид металла, осадок или газ, в зависимости от условий взаимодействия.
В некоторых случаях активность металлов может привести к созданию сложных соединений с веществами, содержащими воду. Например, некоторые металлы могут образовывать гидроксиды, гидраты или комплексные соединения, что может быть использовано в различных химических процессах и технологиях.
Активность металлов в присутствии воды - это важный фактор, который следует учитывать при выборе материалов для конструкций и технических устройств. Знание особенностей взаимодействия металлов с водой позволяет предотвратить коррозию и повреждение материалов, а также использовать их в различных процессах и промышленных производствах.
Формирование окисных пленок на металлической поверхности

Металлы средней активности, такие как алюминий, цинк или железо, при контакте с водой могут образовывать окисные пленки на своей поверхности. Данное явление является результатом химической реакции металла с кислородом из воды, что приводит к окислению металла.
Окисные пленки являются защитным слоем на поверхности металла и предотвращают дальнейшую реакцию с водой. Эти пленки имеют характерную структуру, состоящую из слоев оксидов металла, которые могут быть различной толщины и состава в зависимости от условий образования.
Кроме того, окисные пленки могут обладать различными свойствами, такими как электропроводность, проницаемость для воды и газов, устойчивость к коррозии и механическим воздействиям. Некоторые окисные пленки могут быть полезными для использования в различных областях промышленности, например, в качестве антикоррозионного покрытия или электропроводных материалов.
Образование окисных пленок на металлической поверхности обусловлено не только взаимодействием металла с водой, но и другими факторами, такими как температура, pH среды, наличие других химических веществ. Эти факторы могут влиять на скорость реакции и структуру образующейся пленки.
Образование гидроксидов при взаимодействии металлов с водой

При взаимодействии металлов с водой может происходить образование гидроксидов – соединений металлов с гидроксильными группами OH-. Гидроксиды образуются в результате диссоциации металлических ионов в воде и их последующей реакции с гидроксильными ионами. Этот процесс является важным аспектом взаимодействия металлов с водой и имеет большое значение в различных областях химии и техники.
Вода является хорошим растворителем, поэтому она способна растворять многие металлы и вызывать их диссоциацию. Поэтому при погружении металла в воду происходит его растворение и образование ионов металла в растворе. Затем ионы металла могут реагировать с гидроксильными ионами, присутствующими в воде, образуя гидроксиды.
Гидроксиды металлов обладают различными свойствами – от щелочных до амфотерных. Они могут образовывать растворимые или нерастворимые соединения в зависимости от их растворимости в воде. Некоторые гидроксиды имеют высокую растворимость и образуют стабильные растворы, в то время как другие образуют нерастворимые осадки, которые могут осаживаться на поверхности металла или на дне реакционной смеси.
Знание образования гидроксидов при взаимодействии металлов с водой позволяет учитывать их реакционные способности и использовать в различных сферах, включая производство материалов, электрохимические процессы, очистку воды и другие.
Коррозия и разрушение металлов под воздействием воды

Коррозия – это процесс взаимодействия металла с окружающей средой, в результате которого происходит разрушение материала. Вода, являясь одной из основных сред, способствующих коррозии, играет важную роль в процессе разрушения металлов.
Вода содержит различные вещества, такие как растворенные газы (например, кислород и углекислый газ), соли и другие химические соединения. Когда металл погружается в воду, между его поверхностью и водой образуется электрохимическая система, где разные участки металла играют роль анодов и катодов.
Коррозия металлов под воздействием воды может происходить по разным механизмам, включая:
- Питание
- Концентрационную полярность
- Межкристаллическую коррозию
- Коррозию под напряжением
- Микробиологическую коррозию
В результате коррозии металлов под воздействием воды происходит разрушение материала. Коррозионные процессы могут привести к образованию трещин, пузырьков, отслаиванию слоев металла, а также к изменению механических свойств материала. Появление коррозии может быть вызвано разными факторами, такими как наличие кислорода в воде, солей, наличие других активных веществ и особенностей микробиологической среды.
Для защиты металлов от коррозии используют различные методы, включая использование защитных покрытий и покрытий, антикоррозионных добавок, а также проведение регулярного технического обслуживания и мониторинга состояния металлических конструкций.
Катодные и анодные реакции в системе "металл-вода"
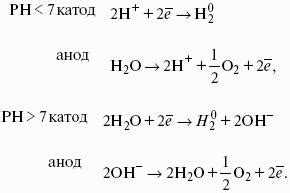
Взаимодействие металлов с водой средней активности происходит посредством катодных и анодных реакций. Катодная реакция представляет собой постепенное выделение водорода на погруженной в воду металлической поверхности.
Электрод потенциального раздела водородного типа является катодом в данной системе и восстанавливается за счет протекающего электролитического процесса. В результате этой реакции металл окисляется до катионного состояния, а протекает электролитический процесс.
С другой стороны, анодная реакция характеризуется окислением воды средней активности до кислорода, который выделяется на поверхности металла. Электрод потенциального раздела кислородного типа является анодом в данной системе.
Под влиянием электролиза и миграции ионов в растворе происходит образование ионосферы, что усиливает рост протекающих катодных и анодных реакций. Также возможно возникновение пассивной пленки на поверхности металла, способной защитить его от дальнейшей коррозии.
В результате взаимодействия воды с металлами средней активности происходит распад молекулы воды на ионы водорода и оксигена. Эти реакции важны для понимания процессов коррозии и защиты металлов от негативного воздействия среды.
Влияние pH воды на химические реакции с металлами
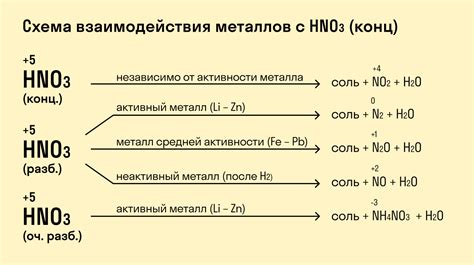
pH воды – это мера кислотности или щелочности раствора, которая определяется концентрацией ионов водорода в растворе. Этот показатель имеет существенное влияние на химические реакции между водой и металлами средней активности.
При нейтральном pH (7), вода обычно обладает нейтральной реакцией с металлами, такими как медь, никель, цинк и алюминий. Это означает, что реакции с металлами происходят медленно или не происходят вообще. Однако, если pH воды изменяется, то эти реакции могут протекать быстрее или вообще измениться.
Если pH воды ниже 7 и становится кислым, то это приводит к активации реакции между кислыми металлами, такими как железо, алюминий и цинк, и водой. В результате образуются соответствующие соляные соединения металла с кислородом и водородом. Это может привести к ускоренной коррозии металлических изделий.
Если pH воды выше 7 и становится щелочным, то реакции между металлами и водой происходят снова медленно или не происходят вообще. В щелочной среде, некоторые металлы, такие как алюминий и цинк, могут покрываться защитной пленкой оксида, что предотвращает дальнейшую реакцию с водой.
Таким образом, pH воды играет важную роль во взаимодействии с металлами средней активности. Знание и контроль pH воды имеют большое значение в различных технических процессах и предотвращают нежелательные химические реакции с металлами.
Биологическое взаимодействие воды с металлами средней активности

Вода является важным компонентом взаимодействия металлов средней активности с биологическими системами. Различные металлы могут быть растворимы в воде и образовывать ионы, которые играют важную роль в жизнедеятельности организмов.
Некоторые металлы, такие как кальций, магний и железо, являются необходимыми микроэлементами для регуляции физиологических процессов. Они участвуют в формировании костей, функции нервной системы и образовании гемоглобина. Вода является средой, в которой происходят процессы растворения и ионизации этих металлов, что обеспечивает их доступность для организма.
С другой стороны, некоторые металлы средней активности, например, свинец и кадмий, могут быть токсичными и вызывать негативные эффекты на организм. Вода может служить источником этих металлов, особенно при недостаточном контроле качества воды потребителями. В результате попадания таких металлов в организмы они могут вызывать отравление и множество заболеваний.
Поэтому контроль качества воды и наличие регламентирующих норм и концентраций металлов средней активности имеют важное значение для обеспечения безопасности питьевой воды и сохранения здоровья людей и животных.
Практическое применение металлов средней активности в связи с водой

Металлы средней активности, такие как цинк, никель, железо и алюминий, имеют широкое практическое применение в различных отраслях, связанных с водой. В первую очередь, эти металлы используются для создания сооружений и оборудования в водоснабжении и водоотведении.
Цинк, благодаря своей стойкости к коррозии, активно применяется для создания трубопроводов, фитингов и насосов в системах водоснабжения. Никель, известный своей устойчивостью к кислородной коррозии и окислительным средам, используется для изготовления теплообменников, труб и арматуры в системах охлаждения и кондиционирования воздуха.
За счет своих антикоррозионных свойств, железо используется для создания ограждений и конструкций, которые подвергаются воздействию воды и атмосферных условий. Этот металл также является основным составляющим материалом для производства водопроводных и канализационных труб, а также насосов и резервуаров.
Алюминий, часто применяется в судостроении и производстве подводных сооружений, благодаря своей легкости и устойчивости к коррозии в соленой воде. Он также используется для создания облицовочных панелей, дверей и оконных рам в зданиях, прибрежных сооружениях и крышах.
Более того, металлы средней активности применяются в процессах очистки воды. Железо используется для удаления железа и марганца, которые могут присутствовать в воде и влиять на ее качество. Алюминий используется для удаления турбидности и органических веществ. Благодаря своим каталитическим свойствам, никель применяется для обработки воды с низким содержанием аммиака.
Таким образом, металлы средней активности играют важную роль в водном секторе, обеспечивая надежность и стабильность систем водоснабжения и водоотведения, а также способствуя обеспечению чистой и безопасной питьевой воды.
Вопрос-ответ

Как вода взаимодействует с металлами средней активности?
Вода может взаимодействовать с металлами средней активности различными способами, включая окисление, образование ионных соединений и гидридов.
Какие металлы относятся к металлам средней активности?
К металлам средней активности относятся, например, цинк, железо и медь. Они не настолько реактивны, как щелочные металлы, но и не настолько стабильны, как благородные металлы.
