Амфотерные металлы представляют собой особую группу веществ, которые обладают способностью взаимодействовать как с кислотами, так и с щелочами. Эта способность делает их уникальными и необычными в мире химии. Благодаря этим свойствам амфотерные металлы широко применяются в различных отраслях промышленности и строительства. Однако, их отличительные характеристики могут быть не всегда очевидны, и их распознавание может потребовать некоторых знаний и опыта. В этой статье мы рассмотрим, как определить амфотерные металлы и чем они отличаются от других веществ.
Важно понимать, что некоторые металлы могут обладать и амфотерными и другими свойствами, в зависимости от условий взаимодействия. Например, алюминий является амфотерным металлом, но при контакте с водой его поверхность окисляется, образуя защитную пленку оксида, что делает его устойчивым к дальнейшему взаимодействию. В таких случаях необходимо учитывать окружающие условия для определения химической реакции металла.
Первым шагом к распознаванию амфотерных металлов является изучение их химических свойств. Амфотерные металлы обычно проявляют способность реагировать как с кислотами, так и с щелочами, что отличает их от других металлов. Для определения реактивности можно провести серию экспериментов с различными разведениями кислот и щелочей и наблюдать изменения, происходящие с металлической поверхностью. Кроме того, амфотерные металлы обычно имеют разнообразные степени окисления, что тоже может являться показателем их амфотерности.
Амфотерные металлы: определение и свойства

Амфотерными металлами называются вещества, которые могут образовывать соединения как с кислотами, так и с щелочами. Такое поведение является особенностью некоторых элементов периодической таблицы.
Свойства амфотерных металлов определяют их способность взаимодействовать как с кислотами, так и с щелочами. Это связано с наличием у них нескольких вариантов окислительных состояний и способностью принять или отдать электроны.
Примерами амфотерных металлов являются алюминий, цинк, свинец и железо. Они способны образовывать различные типы соединений в зависимости от условий окружающей среды. Например, амфотерный металл алюминий может образовывать соли и ионы как с кислотами (например, с хлороводородной кислотой), так и с щелочами (например, с натриевой гидроксидом).
Важно отметить, что свойства амфотерных металлов могут быть использованы в различных областях, включая химическую промышленность и медицину. Например, амфотерные металлы широко применяются в катализе и производстве лекарственных препаратов. Изучение и понимание их химических свойств позволяет разрабатывать новые материалы и технологии.
Что такое амфотерные металлы?
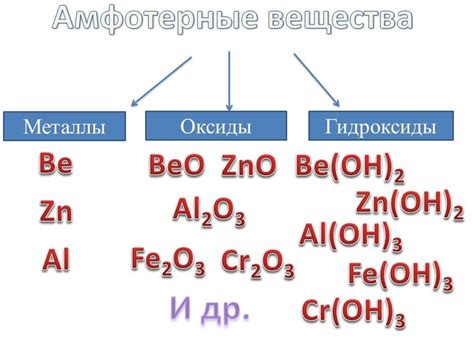
Амфотерные металлы - это класс элементов, которые могут вести себя как основания, проявляя свойства щелочей, и как кислоты, обладая свойствами кислот. Они могут реагировать как с кислотными, так и с щелочными реактивами, проявляя двойную реакционную способность.
Примерами амфотерных металлов являются алюминий (Al), железо (Fe), цинк (Zn), свинец (Pb), медь (Cu) и их соединения. Эти элементы обладают особой электронной структурой, которая позволяет им проявлять амфотерные свойства.
Амфотерные металлы имеют важное значение в химии и промышленности. Они широко применяются в процессах гальванического покрытия, производстве керамики, а также в производстве амфотерных оксидов и гидроксидов. Амфотерные свойства этих металлов позволяют им использоваться в различных областях, включая медицину, электронику и строительство.
Химические свойства амфотерных металлов
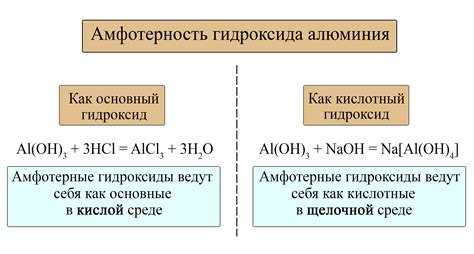
Амфотерные металлы - это класс элементов, которые могут проявлять как кислотные, так и основные свойства в химических реакциях. Они обладают способностью взаимодействовать с кислотами и основаниями, что является характерным для них особенным свойством.
Одним из примеров амфотерных металлов является алюминий. Он реагирует с кислотами, образуя соли, например, с соляной кислотой образуется хлорид алюминия. Алюминий также может реагировать с основаниями, например, образуя гидроксид алюминия в реакции с натрием гидроксидом.
Другим примером амфотерного металла является цинк. Он может образовывать соли с кислотами, например, с соляной кислотой образуется хлорид цинка, а также реагировать с основаниями, образуя гидроксид цинка.
Амфотерные свойства металлов обусловлены наличием свободных электронов и способностью образовывать координационные связи. Кроме алюминия и цинка, к амфотерным металлам относятся также медь, свинец, кадмий и многие другие элементы.
Химические свойства амфотерных металлов имеют важное значение в промышленных и научных приложениях. Например, алюминий используется в производстве лекарств, пищевых добавок, стекла и других материалов. Это связано с его способностью взаимодействовать как с кислотами, так и с основаниями, что позволяет использовать его в различных процессах и реакциях.
Способы распознавания амфотерных металлов
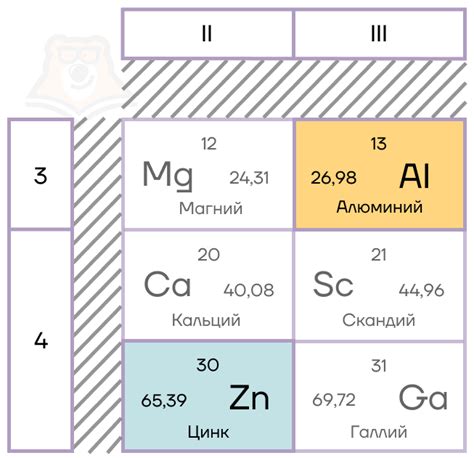
Амфотерные металлы – это элементы периодической системы, которые могут образовывать как катионы, так и анионы, в зависимости от реактивного агента, с которым они взаимодействуют. Они обладают способностью проявлять свойства и характеристики и металлов, и неметаллов. Существует несколько способов распознавания амфотерных металлов.
Определение по реакции с кислотами: амфотерные металлы проявляют кислотные свойства, образуя соляные соединения с кислотами. Однако, они также могут проявлять основные свойства, образуя с кислотами амфотерные соединения.
Определение по реакции с щелочами: амфотерные металлы проявляют щелочные свойства, образуя гидроксиды с щелочами. Однако, они также могут образовывать с щелочами амфотерные соединения.
Определение по реакции с оксидами: амфотерные металлы реагируют с оксидами, проявляя либо кислотные, либо щелочные свойства. Например, сильные оксиды могут образовывать кислотные соединения с амфотерными металлами, а слабые оксиды – щелочные соединения.
Определение по реакции с индикаторами: амфотерные металлы могут изменять цвет индикаторных растворов в зависимости от своих кислотно-щелочных свойств. Они могут проявляться как кислоты, окрашивая индикаторы в кислотные цвета, так и как щелочи, окрашивая индикаторы в щелочные цвета.
Практическое применение амфотерных металлов

Амфотерные металлы, такие как алюминий, цинк, железо и свинец, имеют уникальные свойства, позволяющие им быть использованными в различных отраслях промышленности и научных исследованиях.
Во-первых, амфотерные металлы широко используются в производстве различных материалов. Например, алюминий является основным компонентом для создания легких и прочных сплавов, которые используются в авиационной и автомобильной промышленности. Знание его амфотерных свойств позволяет использовать этот металл для изготовления различных конструкций и деталей с уникальными свойствами.
Во-вторых, амфотерные металлы используются в процессах обработки различных материалов. Например, цинк используется в гальваническом покрытии для защиты металлических поверхностей от коррозии. Его амфотерные свойства позволяют проводить электрохимические процессы, при которых цинк может служить и анодом, и катодом.
Также амфотерные металлы играют важную роль в научных исследованиях. Их свойства могут быть использованы для изучения реакций между металлами и другими веществами. Например, амфотерные свойства железа позволяют использовать его в качестве катализатора в химических реакциях, что облегчает проведение сложных процессов и синтез новых соединений.
В заключении, практическое применение амфотерных металлов открыто множество возможностей для различных отраслей исследований и промышленности. Знание и понимание их уникальных свойств позволяет эффективно использовать эти металлы для создания новых материалов, обработки поверхностей и проведения научных исследований.
Вопрос-ответ

Какие металлы относятся к амфотерным?
К амфотерным металлам относятся алюминий, цинк, кадмий и свинец. Они могут образовывать соли и ионы как с кислотами, так и с щелочами.
Как можно определить, является ли металл амфотерным?
Один из способов определения амфотерности металла - это проведение реакций с разными кислотами и щелочами. Если металл образует соли и ионы как с кислотами, так и с щелочами, то он является амфотерным.
Как амфотерные металлы реагируют с кислотами?
Амфотерные металлы могут реагировать с кислотами, образуя соли. Например, алюминий реагирует с соляной кислотой и образует соль алюминия и водород. Такая реакция называется нейтрализацией.
Как амфотерные металлы реагируют с щелочами?
Амфотерные металлы могут реагировать с щелочами, образуя соли. Например, цинк реагирует с гидроксидом натрия и образует соль цинка и воду. Такая реакция называется гидролизом.
Зачем нужно знать о свойствах амфотерных металлов?
Знание о свойствах амфотерных металлов важно, так как они могут быть использованы в различных химических реакциях и процессах. Например, амфотерные металлы используются в производстве лекарств, катализаторов и различных материалов.
