Ржавчина является одной из наиболее распространенных проблем металлических поверхностей. Она не только портит внешний вид, но и может привести к серьезным повреждениям материала. Многие люди задаются вопросом, как превратить металл в ржавчину и сделать это быстро и эффективно.
Существует несколько способов создания ржавчины на металлической поверхности. Одним из самых популярных методов является использование химических реагентов. Некоторые из них содержат в себе соляную или азотную кислоты, которые обладают силой разъедания металла и приводят к появлению ржавчины. Конечно, использование таких химических веществ требует осторожности и должно выполняться в хорошо проветриваемом помещении или на открытом воздухе.
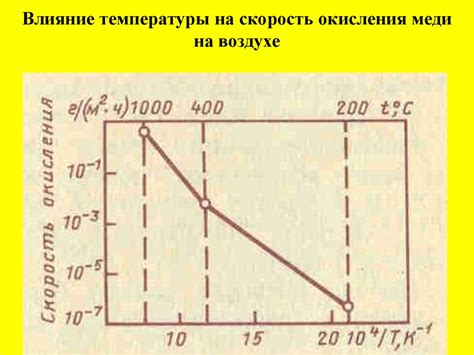
Еще одним способом создания ржавчины на металле является его подвержение действию влаги и кислорода. Примером этого может быть оставление металла на дожде или влажном месте на продолжительное время. Кислород воздуха окисляет металл, что приводит к образованию ржавчины. Важно помнить, что этот процесс занимает время и может занимать от нескольких дней до нескольких месяцев, в зависимости от условий окружающей среды и типа металла.
Что такое ржавчина и как она образуется?

Ржавчина - это процесс окисления металла, который приводит к образованию корки на его поверхности. Образование ржавчины возникает при взаимодействии металла с водой и кислородом, присутствующим в воздухе. Главным "катализатором" ржавчины является вода, которая увеличивает скорость процесса окисления.
Вода воздействует на металл и растворяет его поверхностные слои, открывая доступ воздуха и кислорода к внутренней структуре металла. С этого момента начинается процесс окисления, при котором металл и кислород взаимодействуют и образуют оксиды металла. Оксиды имеют ржаво-коричневый цвет, который и придает ржавчине характерный вид.
Чтобы процесс окисления происходил, металл должен быть способен к реакции с кислородом, а также должны быть наличие влаги и кислорода. Влага увеличивает скорость окисления, поэтому металлы, находящиеся под водой или во влажной среде, подвержены ржавчине в большей степени.
Ржавчина может образовываться на различных металлах, но особенно подвержены этому процессу железо и его сплавы, так как реакция с кислородом у них происходит быстрее. Другие металлы, такие как алюминий или нержавеющая сталь, могут быть устойчивы к ржавчине благодаря образованию защитной пленки на поверхности, которая предотвращает проникновение влаги и кислорода.
body {
font-family: Arial, sans-serif;
line-height: 1.5;
}
table {
border-collapse: collapse;
}
h2 {
font-size: 24px;
font-weight: bold;
margin-bottom: 20px;
}
p {
margin-bottom: 10px;
}
strong {
font-weight: bold;
}
em {
font-style: italic;
}
ul, ol {
margin-bottom: 10px;
}
li {
margin-bottom: 5px;
}
Естественные процессы

В природе существует множество естественных процессов, которые способствуют образованию ржавчины на металлических поверхностях. Один из таких процессов называется окислением. Окисление - это химическая реакция, при которой металл взаимодействует с кислородом из воздуха, образуя оксид металла. Этот оксид является основной составной частью ржавчины.
Кроме окисления, естественные процессы, такие как осадки и влажность, также способствуют образованию ржавчины на металлических поверхностях. Если металл находится под воздействием постоянной влажности, то это может привести к образованию ржавчины. Вода содержит различные элементы, которые могут реагировать с металлом и вызывать окисление.
Еще одним естественным процессом, который способствует образованию ржавчины, является электрохимическая коррозия. Электрохимическая коррозия происходит, когда металлическая поверхность подвергается воздействию влаги и воздуха, что создает электролитическую среду. В такой среде начинает протекать электрохимический процесс, в результате которого металл начинает корродировать и образовывается ржавчина.
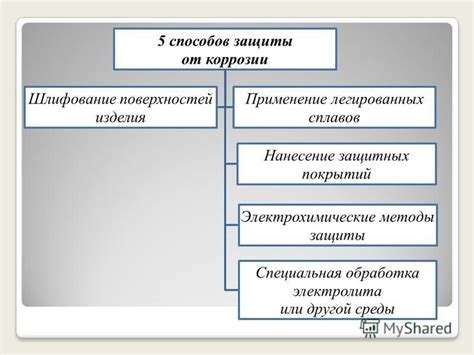
Суммируя вышеизложенное, можно сказать, что естественные процессы, такие как окисление, влажность и электрохимическая коррозия, играют важную роль в образовании ржавчины на металлических поверхностях. Изучение и понимание этих процессов помогут разработать методы и техники, которые могут использоваться для создания или предотвращения ржавчины.
Химические реакции

Химическая реакция – это процесс, в результате которого изменяется химический состав вещества. При химической реакции происходит образование новых химических связей и появление новых веществ с другими свойствами.
Существует несколько основных типов химических реакций, включая окислительно-восстановительные реакции, кислотно-щелочные реакции, восстановительные реакции и ионные реакции.
Окислительно-восстановительные реакции – это реакции, в которых одно вещество окисляется, а другое вещество восстанавливается. В результате происходит обмен электронами между реагентами.
Кислотно-щелочные реакции – это реакции, в которых взаимодействуют кислоты и щелочи. В результате реакции образуются соль и вода. Кислоты передают протоны щелочам, образуя соль, а щелочи передают свободные протоны кислотам.
Восстановительные реакции – это реакции, в результате которых происходит восстановление окисленного вещества или окислительного агента. Восстановление может происходить за счет передачи электронов.
Ионные реакции – это реакции, в которых образуются ионы. При ионной реакции происходит перенос ионов между реагентами.
Химические реакции проявляются во множестве процессов, включая ржавление металла. Ржавчина – это окисляемая пленка на поверхности металла, образующаяся при химической реакции металла с кислородом воздуха.
Виды ржавчины и методы их образования

Ржавчина – это процесс окисления металла, который приводит к образованию характерных коррозионных осадков на поверхности. Существует несколько видов ржавчины, которые образуются в зависимости от условий окружающей среды и состава металла.
Коррозия воздухом. Это наиболее распространенный вид ржавчины. Он образуется при взаимодействии металлической поверхности с кислородом из воздуха. При этом реакции окисления происходят на поверхности металла, образуя ржавчину. Коррозия воздухом может приводить к довольно глубокому разрушению металла.
Контактная коррозия. Этот тип ржавчины возникает при взаимодействии двух разных металлов в присутствии влаги или электролита. Один из металлов становится анодом, а другой – катодом. Поток электронов между ними приводит к реакции окисления и образованию ржавчины.
Коррозия почвы. Когда металл находится в почве, он подвержен воздействию различных химических реакций, которые могут привести к образованию ржавчины. Это происходит из-за наличия в почве различных солей, кислот или же из-за взаимодействия с растениями или микроорганизмами.
Коррозия воды. Вода также способна вызывать процессы окисления металла. Ржавчина может образовываться на металлической поверхности при длительном контакте с водой или ее паром. Особенно это явление характерно для металлических предметов, находящихся в водоемах или погруженных в землю.
Применение и устранение ржавчины

Ржавчина - это окисление металла, которое не только портит его внешний вид, но и может снижать его прочность и функциональность. Несмотря на это, существуют специальные методы и техники, которые позволяют применять ржавчину в различных областях и устранять ее в случае необходимости.
В некоторых случаях, ржавчина может придавать эстетическую привлекательность металлическим изделиям. Например, в интерьерах в стиле лофт или винтаж, металлические поверхности с ржавчиной могут создавать особую атмосферу и придавать помещению уникальный характер. В таких случаях специальные отделочные средства применяются для стабилизации и фиксации ржавчины, чтобы предотвратить ее дальнейшее разрушение и сохранить желаемый эффект.
Однако, в большинстве ситуаций, ржавчина является нежелательным явлением, которое необходимо устранить. Для этого существуют различные методы и химические средства, которые позволяют удалить ржавчину с поверхности металла. Одним из наиболее популярных способов является использование растворителей и средств с высокой концентрацией кислоты. Они эффективно растворяют ржавчину и позволяют очистить металлическую поверхность.
В некоторых случаях, особенно если ржавчина проникла глубоко в металл, может потребоваться применение механических методов удаления. Например, шлифовка, пескоструйная обработка или использование специальных инструментов, таких как стальная щетка или насадка на дрель. При этом необходимо быть аккуратным, чтобы не повредить поверхность металла и не ухудшить его состояние.
Важно понимать, что применение и устранение ржавчины требует знания и опыта. При работе с химическими средствами необходимо соблюдать правила безопасности и использовать защитное снаряжение. При использовании механических методов также важно быть осторожным и внимательным, чтобы не причинить вред себе и окружающим.
Вопрос-ответ

Почему металл ржавеет?
Металл ржавеет из-за химической реакции, называемой окислением, которая происходит в результате взаимодействия металла с кислородом и влагой в воздухе.
Какие факторы способствуют образованию ржавчины на металле?
Образование ржавчины на металле зависит от таких факторов, как содержание влаги в воздухе, наличие солей и кислот в окружающей среде, а также от состава и состояния самого металла.