Азотная кислота (HNO3) является одной из наиболее распространенных кислот, используемых в промышленности и лабораториях. Она обладает сильными окислительными свойствами и может вызывать серьезные повреждения металлических поверхностей. Поэтому необходимо знать методы нейтрализации азотной кислоты на металле, чтобы предотвратить ее разрушительное воздействие.
Одним из наиболее эффективных методов нейтрализации азотной кислоты на металле является использование щелочи, такой как гидроксид натрия или гидроксид калия. Эти вещества реагируют с кислотой, образуя соль и воду. Например, гидроксид натрия реагирует с азотной кислотой по следующей реакции: NaOH + HNO3 → NaNO3 + H2O. При этом образующийся осадок соли можно легко удалить с поверхности металла.
Другим методом нейтрализации азотной кислоты на металле является использование щелочного раствора аммиака. Аммиак реагирует с азотной кислотой, образуя аммонийную соль и воду. Реакция происходит по следующему уравнению: NH3 + HNO3 → NH4NO3. Полученную аммонийную соль можно удалить с поверхности металла путем промывки водой.
Таким образом, для нейтрализации азотной кислоты на металле можно использовать щелочи, такие как гидроксид натрия или гидроксид калия, а также щелочной раствор аммиака. Эти методы позволяют безопасно и эффективно устранить воздействие агрессивной кислоты и предотвратить повреждение металлических поверхностей.
Что такое азотная кислота?
Азотная кислота - это бесцветная или желтоватая жидкость с сильным запахом, химическая формула которой HNO3. Она является одной из самых важных и распространенных кислот в химической промышленности. Азотная кислота обладает высокой реакционной способностью и широко применяется в различных отраслях, включая производство удобрений, взрывчатых веществ, пластиков и красителей.
Азотная кислота образуется при окислении азота воздуха и обладает высокой кислотностью. При контакте с кожей или слизистыми оболочками она может вызвать серьезные ожоги. В чистом виде азотная кислота обычно хранится в стеклянных бутылках, так как агрессивно действует на большинство других материалов.
Азотная кислота является двухатомной кислотой и может отдавать два протона (водородных иона). Ее основные химические свойства связаны с образованием нитратных солей при реакции с металлами. Нитраты обладают высокой растворимостью в воде и, в зависимости от металла, образуют различные соединения с разными свойствами.
Основные свойства и химический состав

Азотная кислота (HNO3) – очень реактивное и коррозионно активное вещество. Она обладает сильной кислотностью и широко используется в различных сферах народного хозяйства, включая промышленность, медицину и сельское хозяйство. Химический состав азотной кислоты включает молекулу одного атома азота (N) и трех атомов кислорода (O).
Азотная кислота обладает мощными окислительными свойствами и может вызывать деструктивные процессы взаимодействия с металлами. В результате, она может разрушить структуру и поверхность металла, вызывая коррозию. Взаимодействие азотной кислоты с металлами происходит посредством окисления атомов металла, образования азотистых соединений и выделения газообразного оксида азота.
Азотная кислота обычно применяется в промышленности для очистки и усиления поверхности металла перед дальнейшей обработкой или покрытием. Высокая кислотность и окислительные свойства способствуют удалению загрязнений и окисленных слоев с поверхности металла, обеспечивая лучшее сцепление с последующими покрытиями. Однако, использование азотной кислоты требует особой осторожности и заботы, так как она может быть опасной для здоровья человека и окружающей среды.
Использование азотной кислоты в промышленности
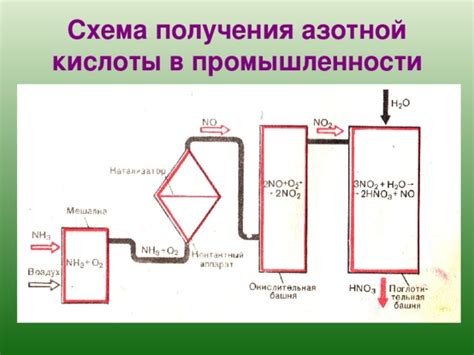
Азотная кислота является одним из наиболее широко используемых химических соединений в промышленности. Она имеет множество применений благодаря своим химическим свойствам, таким как ее высокая реакционная способность и окислительные свойства.
Одним из главных применений азотной кислоты является производство различных видов удобрений, таких как нитраты аммония и нитраты калия. Азотная кислота используется в процессе нитрирования, при котором аммиачное соединение реагирует с кислотой, образуя соответствующий нитрат.
Другим важным применением азотной кислоты является производство взрывчатых веществ, таких как тротил и динамит. Азотная кислота используется как окислитель в реакции с соединениями, содержащими углерод и водород, что позволяет получить высокоэнергетические взрывчатые соединения.
Азотная кислота также используется в процессе обработки металлов. Она используется как часть электролитического раствора при нанесении защитных и декоративных покрытий на поверхность металлов. Азотная кислота обладает высокой степенью растворимости и реакционной способностью, что позволяет ей эффективно взаимодействовать с поверхностью металла, обеспечивая качественное покрытие.
Кроме того, азотная кислота используется в процессе производства различных химических соединений, таких как азотная кислота целлюлозы, азотная кислота ацетата и азотные эфиры. Эти соединения используются в качестве растворителей, веществ для разрыхления и обработки растительных волокон, а также в процессе производства лекарственных препаратов и красителей.
Почему азотная кислота может повредить металл?

Азотная кислота является химическим соединением, которое может представлять опасность для металлических материалов. Ее повреждающие свойства обусловлены высокой агрессивностью, вызванной наличием активного азота и кислорода в ее составе.
Взаимодействие азотной кислоты с металлом может привести к разрушению поверхности материала, образованию коррозии и даже полной потере его работоспособности. Это происходит из-за того, что агрессивные ионы азотной кислоты атакуют структуру металла, разрушают его кристаллическую решетку и вызывают химические реакции, которые приводят к образованию расщепленных участков и поверхностного разрушения.
Особенно восприимчивы к атаке азотной кислоты металлы, которые обладают высокой активностью и электропроводностью, такие как железо, алюминий и медь. Вещества, которые содержат эти металлы, могут подвергаться серьезным повреждениям при взаимодействии с азотной кислотой.
Для предотвращения повреждений металлических поверхностей и их защиты от воздействия азотной кислоты, широко применяются методы нейтрализации. Эти методы предусматривают применение различных химических реагентов, которые способны нейтрализовать агрессивные свойства азотной кислоты и предотвратить ее влияние на металлические материалы.
Основные причины коррозии металла под влиянием азотной кислоты

Азотная кислота (HNO3) является сильным окислителем и может вызывать коррозию металлов под действием различных факторов. Основные причины коррозии металла под влиянием азотной кислоты включают:
- Агрессивность кислоты. Азотная кислота обладает высокой кислотностью и способна реагировать с поверхностью металла, вызывая химическую коррозию. Кислотное окружение способствует образованию активного кислорода и резкому повышению концентрации ионов водорода, что ускоряет процесс коррозии.
- Электрохимическая реакция. Под влиянием азотной кислоты металл может подвергаться электрохимической коррозии. Происходит реакция окисления-восстановления, при которой на поверхности металла образуются окисные пленки, что приводит к разрушению металлической структуры.
- Высокая температура. Повышенная температура изменяет реакционную способность азотной кислоты и увеличивает ее агрессивность. В результате этого ускоряется процесс коррозии металла.
При контакте металла с азотной кислотой необходимо принять меры для нейтрализации этой кислоты и предотвращения коррозии. Нейтрализация может осуществляться с помощью щелочных растворов или специальных химических реагентов, которые реагируют с кислотой и образуют нерастворимые соли.
Как предотвратить повреждение металла азотной кислотой?

Азотная кислота является сильным окислителем и может нанести значительный вред металлическим поверхностям. Однако, существуют методы нейтрализации азотной кислоты на металле, помогающие предотвратить повреждения и сохранить его целостность.
1. Защитные покрытия: Нанесение на металл специальных покрытий, таких как эмали, лаки или защитные пленки, может эффективно предотвратить воздействие азотной кислоты на поверхность металла. Эти покрытия создают барьер, который защищает металл от проникновения кислоты и предотвращает ее окислительное действие.
2. Использование средств с нейтрализующим эффектом: Нейтрализующие средства, содержащие щелочи, такие как гидроксид натрия или гидроксид калия, могут быть использованы для нейтрализации азотной кислоты на металле. Они реагируют с кислотой, образуя нейтральные соли, которые не повреждают металл.
3. Соблюдение правил безопасности: Предотвращение попадания азотной кислоты на металл может быть достигнуто соблюдением правил безопасности при ее хранении и использовании. Рекомендуется хранить кислоту отдельно от металлических предметов и перевозить ее в закрытой упаковке. При работе с кислотой следует использовать специальные средства защиты, такие как перчатки и защитные очки, чтобы предотвратить случайное попадание кислоты на металл.
4. Регулярный уход и обслуживание: Регулярная очистка и обслуживание металлических поверхностей также помогает предотвратить повреждение азотной кислотой. Удаление остатков кислоты с металла с помощью специальных растворителей или моющих средств поможет сохранить его целостность и увеличить срок его службы.
Предотвращение повреждения металла азотной кислотой является важной задачей, которая может быть достигнута путем применения защитных покрытий, использования нейтрализующих средств, соблюдения правил безопасности и регулярного ухода за металлическими поверхностями.
Вопрос-ответ

Какие методы используются для нейтрализации азотной кислоты на металле?
Для нейтрализации азотной кислоты на металле можно использовать несколько методов. Один из них - это обработка поверхности металла щелочным раствором, который реагирует с кислотой и нейтрализует ее. Другой метод - применение специальных химических соединений, таких как аммиак или гидроксид натрия, которые также реагируют с азотной кислотой и превращают ее в соли или более безопасные соединения. Еще один метод - это использование электрохимической коррозии, при которой кислота или ее продукты окисления разлагаются под воздействием электрического тока.
