Атомная масса металла — это средневзвешенная масса атомов данного металла в периодической системе элементов. Рассчитывая атомную массу металла, мы можем определить массовое отношение между атомами различных изотопов этого металла, что имеет важное значение для химических расчетов и исследований.
Для расчета атомной массы металла мы должны знать массовое число каждого изотопа металла и его относительную абундантность. Относительная абундантность показывает, насколько часто встречается данный изотоп в природе. Она измеряется в процентах или в виде десятичной дроби.
Например, рассмотрим массовое число и относительную абундантность двух изотопов металла: изотоп A с массовым числом 40 и относительной абундантностью 60%, и изотоп B с массовым числом 42 и относительной абундантностью 40%. Для расчета атомной массы металла мы умножаем массовое число каждого изотопа на его относительную абундантность, затем складываем полученные произведения.
Таким образом, атомная масса металла = (массовое число изотопа A * относительная абундантность изотопа A) + (массовое число изотопа B * относительная абундантность изотопа B). Получившаяся сумма будет представлять собой атомную массу металла с учетом относительной абундантности каждого изотопа.
Что такое атомная масса металла?
Атомная масса металла представляет собой среднюю массу атомов данного металла, выраженную в атомных единицах (а.е.м.). Другими словами, это количество массы вещества, которое содержится в одном атоме данного металла. Зная атомную массу, можно рассчитать массу определенного количества атомов или молекул металла.
Атомная масса металла вычисляется путем усреднения массы всех изотопов данного металла, пропорционально их относительному содержанию. Изотопы - это атомы одного и того же элемента, но имеющие различное количество нейтронов. Из-за присутствия изотопов атомная масса металла может отличаться от целого числа, так как она учитывает средний вес всех изотопов, участвующих в составе металла.
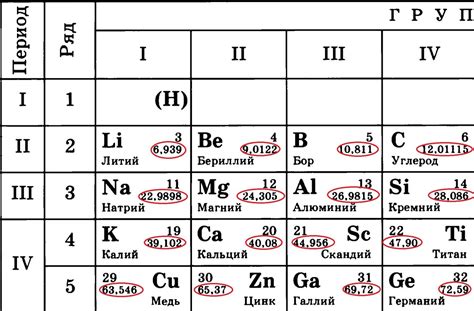
Атомную массу металла можно найти в периодической системе химических элементов, где она указана под именем элемента в таблице. Обычно атомная масса выражается в граммах на моль (г/моль), что позволяет установить массу одного атома вещества и применять ее для химических расчетов и реакций.
Принципы и определения

Рассчет атомной массы металла является важным исследовательским инструментом в химии и физике. Атомная масса металла представляет собой среднюю массу атомов металла в его естественном состоянии и измеряется в атомных единицах (amu).
Атомная масса металла определяется путем учета массы его изотопов и их относительной обилии в природе. Изотопы - это различные формы атомов металла, отличающиеся количеством нейтронов в атомном ядре. Изотопы имеют разные массы, и учет их относительной обилии позволяет рассчитать среднюю атомную массу.
Для рассчета атомной массы металла используется таблица элементов, где указаны массы изотопов и их относительные обилия. Умножение массы каждого изотопа на его относительное обилие и суммирование этих результатов дает среднюю атомную массу металла.
Атомная масса металла имеет большое значение при проведении различных химических расчетов, таких как определение количества вещества и молярной массы. Знание атомной массы металла позволяет уточнить точность расчетов и представить химические процессы на молекулярном уровне.
Как рассчитать атомную массу металла: основные шаги

Атомная масса металла - это средняя масса атомов данного металла, выраженная в атомных единицах (аму). Рассчитывая атомную массу металла, можно определить, сколько граммов данного металла содержится в одной молекуле или одном мольке вещества. Для расчета используется периодическая система химических элементов, где указана атомная масса каждого элемента.
Основные шаги для расчета атомной массы металла:
- Определите химический символ металла, атомную массу которого требуется рассчитать. Химический символ металла указан в периодической системе элементов и обычно состоит из одной или двух букв.
- Найдите атомную массу металла в периодической системе химических элементов. Атомная масса указана под химическим символом каждого элемента в граммах на моль.
- Приведите массу металла к нужным единицам измерения. Обычно атомная масса указывается в граммах на моль, поэтому, если вам нужно выразить атомную массу в граммах на атом или каком-либо другом масштабе, выполните соответствующие преобразования.
Например, рассчитаем атомную массу железа (Fe). В периодической системе элементов атомная масса железа равна примерно 55,85 г/моль. Для преобразования в граммы на атом можно поделить атомную массу на число Авогадро (6,022 × 10^23), получив примерно 9,27 × 10^-23 г/атом.
Таким образом, расчет атомной массы металла является важным шагом для понимания его физических и химических свойств, а также для проведения различных расчетов в области химии и материаловедения.
Формула расчета атомной массы металла

Атомная масса металла - это средняя масса атомов этого металла, выраженная в атомных единицах массы (а.е.м.). Расчет атомной массы металла осуществляется по формуле:
АМ = ∑ (Mi * Ni)
где АМ - атомная масса металла (а.е.м.),
Мi - масса i-го изотопа металла (а.е.м.),
Ni - доля i-го изотопа металла в природе (безразмерная величина).
Для расчета атомной массы металла необходимо знать массы каждого изотопа металла и их доли в природе. Массы изотопов указаны в таблице элементов Менделеева, а доли изотопов можно найти в специальных источниках.
На практике для упрощения расчета атомной массы металла используется средняя атомная масса, которая представляет собой среднее значение массы атомов металла, учитывая доли его изотопов в природе. Средняя атомная масса металла может отличаться от массы каждого отдельного атома металла и зависит от пропорции изотопов в его составе.
Например, для расчета атомной массы железа необходимо учесть, что в природе примерно 5.845% составляет изотоп железа-54 с массой 53.939 а.е.м., 91.754% составляет изотоп железа-56 с массой 55.934 а.е.м., и 2.119% составляет изотоп железа-57 с массой 56.935 а.е.м. Подставив данные в формулу расчета, мы получим среднюю атомную массу железа:
АМ(Fe) = (0.05845 * 53.939) + (0.91754 * 55.934) + (0.02119 * 56.935) = 55.845 а.е.м.
Таким образом, формула позволяет рассчитать атомную массу металла, исходя из массы его изотопов и доли каждого изотопа в природе.
Важные факторы, влияющие на точность расчетов

Расчет атомной массы металла является сложным и многоэтапным процессом, который требует учета нескольких важных факторов для достижения высокой точности и надежности результатов.
Первым важным фактором является выбор исходных данных. Для расчета атомной массы металла необходимо знать молярные массы его атомов. Важно использовать актуальные и достоверные данные о молярных массах, которые можно найти в химических справочниках или базах данных.
Другим важным фактором является учет изотопов. Металлы могут иметь несколько изотопов, имеющих различные массы атомов. При расчете атомной массы, необходимо учитывать относительные процентные содержания каждого изотопа, чтобы получить точные значения.
Также, необходимо учитывать степень чистоты металла. Наличие примесей может оказывать влияние на атомную массу металла. Значительная концентрация примесей может привести к смещению расчетных значений, поэтому важно знать и учеть их содержание при проведении расчетов.
Для достижения максимальной точности в расчетах, необходимо также принимать во внимание факторы округления и приближения. Округление результатов до определенного числа знаков после запятой может привести к незначительным погрешностям, которые необходимо учесть.
Итак, учет этих важных факторов, таких как выбор исходных данных, учет изотопов, степень чистоты металла и факторы округления и приближения, позволяет повысить точность расчетов атомной массы металла и получить надежные результаты.
Вопрос-ответ

Какая формула используется для расчета атомной массы металла?
Для расчета атомной массы металла используется формула, в которой учитывается количество изотопов данного элемента и их относительная атомная масса.
Как найти относительную атомную массу металла?
Относительная атомная масса металла вычисляется как среднее арифметическое массы атомов всех его изотопов, умноженное на их относительные проценты обычного встречания.
Что такое изотопы и как они влияют на расчет атомной массы металла?
Изотопы - это разновидности атомов одного и того же элемента, отличающиеся числом нейтронов в ядре. Изотопы металла имеют разную атомную массу, поэтому для расчета средней атомной массы металла необходимо учитывать их количество и относительную атомную массу.
Какие единицы измерения используются для атомной массы металла?
Атомная масса металла измеряется в атомных единицах массы (аму) или в граммах на моль. Атомная единица массы равна одной двенадцатой части массы атома углерода-12.
Можно ли найти атомную массу металла, зная его химическую формулу?
Нет, атомная масса металла не может быть найдена только по его химической формуле. Для расчета атомной массы металла необходимо знать количество и относительную атомную массу его изотопов.
