Щелочноземельные металлы - это одна из групп химических элементов, которые находятся во второй группе периодической таблицы. В эту группу входят бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Подобно щелочным металлам, щелочноземельные металлы обладают сходными свойствами, но отличаются более высокими плотностью и точкой плавления, а также менее реактивными свойствами. В этой статье мы расскажем, как распознать и определить наличие этих металлов в примерах.
Один из методов, который может помочь в распознавании щелочноземельных металлов, - это использование пламени. Каждый из этих металлов имеет свой характерный оттенок пламени при горении. Например, бериллий дает безцветное пламя, магний - белое светлое пламя, а барий - зеленое пламя. Следует отметить, что этот метод достаточно приблизительный и может быть не всегда надежным.
Второй способ распознавания щелочноземельных металлов - это использование химических реакций с другими веществами. Например, щелочноземельные металлы реагируют с кислотами, образуя соли и выделяя водород. Кроме того, они могут образовывать оксиды и гидроксиды при реакции с кислородом и водой соответственно. Эти химические реакции могут помочь в определении присутствия щелочноземельных металлов в примерах.
Какие элементы относятся к щелочноземельным металлам?
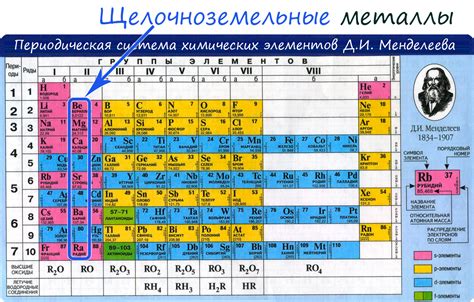
Щелочноземельные металлы - это группа химических элементов, которая расположена во второй группе периодической таблицы Менделеева. Эта группа состоит из шести элементов: бериллия (Be), магния (Mg), кальция (Ca), стронция (Sr), бария (Ba) и радия (Ra).
Бериллий (Be) является первым элементом группы щелочноземельных металлов. Он обладает серебристо-белым цветом и хорошей проводимостью электричества. Бериллий используется в производстве сплавов и конструкционных материалов благодаря своей легкости и прочности.
Магний (Mg) - это легкий, серебристо-белый металл. Он является важным элементом для жизни, так как входит в состав многих биологических молекул. Магний применяется в производстве сплавов, а также в производстве огнестойких материалов и пиротехнических смесей.
Кальций (Ca) - это мягкий серебристо-белый металл, который широко распространен в природе. Он играет важную роль в живых организмах, так как является необходимым элементом для здоровья костной ткани и функционирования нервной системы. Кальций используется в производстве строительных материалов, лекарств и пищевых добавок.
Стронций (Sr) - это мягкий, серебристо-белый металл, который обладает химическими и физическими свойствами, похожими на кальций. Стронций используется в производстве стекла, огнегасителей и ядерных реакторов.
Барий (Ba) - это мягкий, серебристо-белый металл, который имеет высокую плотность. Барий используется в производстве телевизионных и компьютерных экранов, стекла и фармацевтических препаратов.
Радий (Ra) - это редкий и радиоактивный металл. Он обладает высокой токсичностью и опасностью для жизни. Радий используется в научных исследованиях и в медицине для лечения рака.
Щелочноземельные металлы имеют много различных применений и играют важную роль в различных отраслях науки и промышленности.
Физические свойства щелочноземельных металлов

Щелочноземельные металлы - это группа химических элементов, включающая в себя бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). У этих металлов есть несколько общих физических свойств, которые делают их уникальными и полезными для различных применений.
Одним из основных физических свойств щелочноземельных металлов является их металлический блеск. Они обладают достаточно высоким блеском, который проявляется при полировке или обработке поверхности. Это свойство делает щелочноземельные металлы привлекательными для использования в ювелирных изделиях и в других отраслях, где требуется эстетическое качество поверхности.
Другим важным физическим свойством щелочноземельных металлов является их низкая плотность. Они отличаются от других металлов тем, что обладают меньшей плотностью, что делает их легкими и удобными в использовании. Например, магний, который является одним из щелочноземельных металлов, обладает очень низкой плотностью, поэтому используется в авиационной и автомобильной промышленности для создания легких и прочных материалов.
Щелочноземельные металлы также обладают хорошей теплопроводностью. Они могут легко передавать теплоту, что делает их полезными для применений, где требуется эффективное распределение тепла. Например, кальций используется в производстве световых катодов, где его хорошая теплопроводность помогает распределить тепло равномерно и снизить риск перегрева.
Щелочноземельные металлы также обладают высокой электропроводимостью. Они легко проводят электрический ток, что делает их полезными для использования в электронике и электротехнике. Например, бериллий, который является щелочноземельным металлом, используется в производстве контактов и электродов, так как он обладает высокой электропроводимостью и хорошей устойчивостью к коррозии.
В заключение, физические свойства щелочноземельных металлов, такие как металлический блеск, низкая плотность, хорошая теплопроводность и высокая электропроводимость, делают их полезными и востребованными материалами в различных отраслях. Они играют важную роль в промышленности, науке и технологии, и их свойства способствуют развитию новых технологий и материалов.
Химические свойства щелочноземельных металлов

Щелочноземельные металлы - это группа химических элементов, включающая в себя бериллий, магний, кальций, стронций, барий и радий. Они обладают сходными химическими свойствами, которые определяются их электронной структурой.
Основные химические свойства щелочноземельных металлов включают:
- Высокую реактивность: Щелочноземельные металлы активно взаимодействуют с водой, кислородом и другими химическими веществами. Они более реактивны, чем щелочные металлы, но менее реактивны, чем активные металлы, такие как алюминий или натрий.
- Щелочность: Все щелочноземельные металлы составляют щелочную часть периодической таблицы. Они реагируют с водой, образуя гидроксиды и выделяя водород.
- Образование оксидов: Щелочноземельные металлы имеют сильную способность образовывать оксиды при взаимодействии с кислородом. Например, магний образует оксид магния (MgO), который является основным компонентом вещества, известного как магний.
- Высокую температуру плавления: Большинство щелочноземельных металлов обладают высокими температурами плавления, что делает их полезными материалами в различных промышленных процессах и технологиях.
Благодаря своим уникальным свойствам, щелочноземельные металлы находят широкое применение в различных областях, включая металлургию, строительство, медицину и электронику. Они являются важными компонентами сплавов, катализаторов и материалов для производства легких и прочных конструкций.
Реакции щелочноземельных металлов с водой и кислотами

Щелочноземельные металлы в таблице элементов Менделеева находятся во второй группе. К ним относятся бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). У этих металлов характерным свойством является высокая реактивность.
Реакция с водой:
Бериллий не реагирует с обычной водой, но образует оксид BeO при взаимодействии с паром воды. Магний реагирует с водой, выделяя водород и образуя гидроксид магния Mg(OH)2. Кальций, стронций и барий также реагируют с водой, образуя соответствующие гидроксиды (Ca(OH)2, Sr(OH)2, Ba(OH)2).
Реакция с кислотами:
Взаимодействие щелочноземельных металлов с кислотами приводит к образованию солей и выделению водорода. Например, реакция магния с соляной кислотой HCl приводит к образованию хлорида магния MgCl2 и выделению водорода. Такие реакции характерны для всех щелочноземельных металлов.
Реакции щелочноземельных металлов с водой и кислотами позволяют определить их присутствие в различных веществах и соединениях. Эти реакции являются основой для методов анализа и выделения данных металлов в химических исследованиях.
Примеры распознавания щелочноземельных металлов в лаборатории

Щелочноземельные металлы - это группа элементов периодической таблицы химических элементов, которые имеют сходные физические и химические свойства. К ним относятся бериллий, магний, кальций, стронций, барий и радий.
В лаборатории для распознавания щелочноземельных металлов используются различные методы и реакции. Одним из таких методов является ионно-экранировочная хроматография. С помощью этого метода можно определить присутствие и концентрацию щелочноземельных металлов в образце.
Другим методом является спектральный анализ. Спектральный анализ позволяет исследовать поглощение и испускание электромагнитной радиации материалом. Каждый щелочноземельный металл имеет свой характерный спектральный отпечаток, который можно использовать для его распознавания.
Также для определения щелочноземельных металлов может применяться метод гравиметрического анализа. При этом методе происходит выпадение осадка из раствора и последующее его взвешивание. В результате можно получить точные значения содержания щелочноземельных металлов в образце.
Кроме того, в лаборатории можно использовать химические реакции для распознавания щелочноземельных металлов. Например, реакция с оксалатом аммония или сульфатом аммония может привести к образованию осадков, которые могут быть отнесены к конкретному щелочноземельному металлу.
В современных лабораториях широко применяются автоматические анализаторы, которые позволяют быстро и точно определить содержание щелочноземельных металлов в образцах. Эти анализаторы основаны на различных методах и технологиях, таких как атомно-абсорбционная спектрометрия, флюоресцентная спектрометрия и другие.
Примеры использования щелочноземельных металлов в промышленности

Щелочноземельные металлы, такие как магний, кальций и барий, являются важными материалами для различных отраслей промышленности. Их уникальные свойства делают их незаменимыми в ряде процессов и производств.
Примеры использования щелочноземельных металлов в промышленности:
- Авиационная промышленность: Магний широко используется в производстве легких и прочных сплавов для изготовления компонентов авиационной техники, таких как корпуса самолетов, двигатели и шасси. Благодаря своей легкости и прочности, магниевые сплавы помогают снизить вес и повысить эффективность авиационных конструкций.
- Автомобильная промышленность: Кальций используется в производстве сплавов для литья деталей автомобилей. Он улучшает качество и прочность металла, уменьшает его плотность и снижает температуру плавления. Кальций также используется в процессе дегазации стали, что позволяет убрать из нее вредные примеси.
- Строительная промышленность: Барий, в виде своих соединений, используется в производстве бетона, глинозема и стекла. Он повышает плотность и прочность материалов, а также обеспечивает им устойчивость к истиранию и коррозии.
- Фармацевтическая промышленность: Магний и кальций используются в производстве лекарственных препаратов, включая витамины и минеральные добавки. Эти металлы играют важную роль в поддержании здоровья костей, мышц и нервной системы человека.
- Энергетическая промышленность: Барий использовался в прошлом для получения рентгеновского излучения в медицинских и промышленных рентгеновских установках. Сегодня щелочноземельные металлы также используются в производстве энергоэффективных батарей.
Это лишь некоторые примеры использования щелочноземельных металлов в промышленности. Эти металлы продолжают находить новые области применения и играть важную роль в различных отраслях производства и технологий.
Как обнаружить щелочноземельные металлы в повседневной жизни
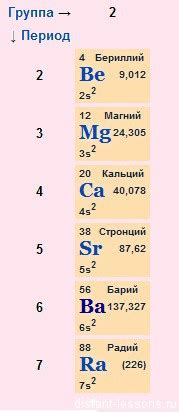
Щелочноземельные металлы - это группа химических элементов, которые могут быть найдены в различных предметах и материалах, которые мы используем в повседневной жизни. Определить присутствие этих металлов можно с помощью нескольких простых методов и наблюдений.
1. Смотри на цвет и блеск: Щелочноземельные металлы, такие как магний, кальций и стронций, обладают характерным блеском и ярким цветом. Например, магний имеет серебристо-белый цвет, а стронций - красновато-желтый. Если предмет имеет подобный цвет и блеск, то есть вероятность, что он содержит щелочноземельные металлы.
2. Проверь наличие реактивности: Щелочноземельные металлы обладают высокой химической реактивностью, особенно кислороду и воде. Если предмет реагирует с водой, выделяет газ или изменяет свою структуру под воздействием влаги или кислорода, то есть большая вероятность, что он содержит щелочноземельные металлы.
3. Используй химические тесты: Существуют специальные химические тесты, которые позволяют определить наличие щелочноземельных металлов в пробе. Такие тесты можно приобрести в химической лаборатории или онлайн. Их использование может быть полезно, если вам требуется точное определение щелочноземельных металлов в материалах или предметах.
Важно помнить, что определение присутствия щелочноземельных металлов требует опыта и знаний в области химии. Без достаточного опыта, самостоятельное определение щелочноземельных металлов может быть затруднительным и ненадежным.
Итак, при наличии яркого цвета, блеска, реактивности или с помощью химических тестов, можно обнаружить щелочноземельные металлы в повседневной жизни. Однако, для точного определения рекомендуется обратиться к специалисту или использовать специализированные химические тесты.
Вопрос-ответ

Какие металлы относятся к щелочноземельным?
К щелочноземельным металлам относятся бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Как можно определить щелочноземельные металлы в примерах?
Определить щелочноземельные металлы можно по нескольким признакам: они имеют от двух до шести электронов на внешней энергетической оболочке, образуют оксиды с щелочной реакцией, образуют двухзарядные ионы и обладают подобными физическими и химическими свойствами.
