Коррозия – это процесс разрушения металла под влиянием окружающей среды, такой как влажность, кислоты или соли. Коррозия может серьезно повлиять на структурную целостность металлических изделий и привести к их непригодности для использования. Одним из наиболее распространенных способов защиты металла от коррозии является покраска. Однако существуют и другие эффективные методы, которые не требуют применения краски.
Один из таких способов – гальваническая защита. Она основана на создании анодной и катодной зон на поверхности металла. Металлический анод, как правило, представляет собой пластину или гальваническую анодную систему, которая погружается в электролитический раствор. При этом он расходуется, защищая основной металл от коррозии. Катодная зона может быть создана путем подключения второго металла, который будет служить как катод, или с использованием катодной защитной системы.
Еще одним способом защиты металла от коррозии является нанесение покрытий или покрытий без использования краски. Нанесение покрытий может быть выполнено путем горячего цинкования, алюминизации или оксидирования. Горячее цинкование – это процесс, в ходе которого металлическая поверхность погружается в расплавленный цинк. При контакте с металлом цинк реагирует с ним, образуя защитное цинковое покрытие. Алюминизация – это процесс нанесения алюминиевого покрытия на поверхность металла. Оксидирование – это создание защитного оксидного покрытия на металле путем обработки его в кислотной или щелочной среде.
Все эти способы защиты металла от коррозии без покраски являются эффективными и могут быть использованы в зависимости от конкретных условий и требований. Они позволяют сохранить металлические изделия в рабочем и безопасном состоянии на протяжении длительного времени.
Что такое коррозия металла?

Коррозия металла - это процесс разрушения и повреждения металлических предметов в результате химических реакций со средой. Она может быть вызвана воздействием влаги, кислот, солей, газов и других веществ на поверхность металла.
Вследствие коррозии металла могут образовываться окислы и гидроксиды, которые снижают прочность и долговечность материала. Коррозия может привести к появлению трещин, отслоения покрытия, утрате эстетического вида и даже к полной потере функциональности предмета.
Процесс коррозии металла является естественным и неизбежным, поскольку находится взаимодействии между металлом и окружающей средой. Однако существуют различные способы защиты металла от коррозии без покраски, которые могут помочь предотвратить или замедлить этот процесс.
Почему покраска не всегда эффективна?

Покраска является одним из самых распространенных способов защиты металла от коррозии. Однако, не во всех случаях покраска может быть эффективным решением. Во-первых, покраска требует определенной подготовки поверхности и нанесения краски в несколько слоев. Если этот процесс выполнен некачественно или пропущены какие-либо этапы, то металлическая поверхность останется уязвимой для коррозии.
Во-вторых, покраска может быть неэффективна в условиях эксплуатации, когда металл подвергается агрессивным химическим воздействиям, контактам с водой или влажными средами. Даже при наличии качественного покрытия, коррозия может произойти из-за механических повреждений, царапин или сколов краски.
Кроме того, покраска может стать временным решением, требующим периодического обслуживания и актуализации. Краска со временем может выцветать, трескаться или отслаиваться, что снижает ее защитные свойства и может привести к образованию очагов коррозии. Удачным сочетанием между покраской и другими способами защиты можно добиться наилучшей эффективности в борьбе с коррозией металла.
Гальваническая защита

Гальваническая защита - один из эффективных способов защиты металла от коррозии без покраски. Она основана на явлении электрической коррозии, при которой металлы, находящиеся в электролите, под воздействием электрохимического процесса, могут образовывать гальванические элементы и создавать токовую цепь.
Этот метод заключается в использовании металла с большей электрохимической активностью (самого активного металла) в качестве анода и металла с меньшей активностью (менее активного металла) в качестве катода. Таким образом, активный металл будет жертвоваться коррозии вместо менее активного металла.
Гальваническая защита может быть реализована с помощью различных методов, включая использование анодов из цинка, алюминия или магния, а также применение специальных анодов, таких как аноды смешанного металла. Эти аноды должны быть правильно подключены к металлическому объекту, чтобы обеспечить эффективную защиту.
Преимуществами гальванической защиты являются ее простота и низкая стоимость в сравнении с другими методами защиты от коррозии. Она также может быть эффективной даже при небольшом количестве защитных материалов. Однако этот метод имеет свои ограничения и может быть неэффективным в некоторых условиях, таких как высокая температура, высокая концентрация электролита или наличие сильных кислот или щелочей.
Катодная защита

Катодная защита является одним из эффективных методов предотвращения коррозии металлов без использования покрытий. Она основана на электрохимическом принципе, который позволяет сохранить металл в неизменном состоянии за счет изменения потенциала поверхности.
Основным принципом катодной защиты является создание электрической цепи, включающей металлическую конструкцию, аноды из неразрушаемого материала, источник постоянного или переменного тока, а также электролит. Процесс защиты осуществляется путем подачи постоянного или переменного тока на аноды из неразрушаемого материала, в результате чего металл становится катодом, а аноды – анодами.
В процессе катодной защиты происходит уменьшение скорости коррозии металла за счет передачи электронов с анодов на катоды. Катодная защита эффективна для большого количества конструкций, так как она позволяет защищать металлы с различными геометрическими формами и сложной конфигурацией.
Катодная защита может использоваться для защиты таких объектов, как подводные сооружения, трубопроводы, судовые конструкции, танкеры и другие металлические конструкции, находящиеся в агрессивных средах. Она применяется в различных отраслях промышленности, таких как нефтегазовая, химическая, энергетическая, судостроительная и др.
Ингибиторы коррозии

Ингибиторы коррозии - это химические вещества, которые помогают предотвратить или замедлить процесс коррозии металла.
Они действуют, образуя на поверхности металла защитную пленку, которая препятствует контакту металла с окружающей средой. Эта пленка может быть механической или химической.
Ингибиторы коррозии классифицируются по различным признакам, например по их действию на разные типы коррозии или по применению в определенных условиях.
Одним из примеров ингибиторов коррозии являются азотсодержащие соединения. Они образуют на поверхности металла защитную пленку из оксида, которая предотвращает контакт с окружающей атмосферой и влагой.
Другими примерами ингибиторов коррозии являются соединения, содержащие фосфор или фтор. Они также образуют непроницаемую пленку на поверхности металла, которая предотвращает реакцию с окружающей средой.
Ингибиторы коррозии широко применяются в различных отраслях промышленности, особенно в нефтегазовой, химической и строительной промышленности. Они помогают увеличить срок службы металлических конструкций и оборудования, а также снизить затраты на их покраску и ремонт.
Полимерные покрытия

Способы защиты металла от коррозии без покраски включают использование полимерных покрытий. Полимеры - это молекулярные соединения, состоящие из длинных цепей повторяющихся единиц - мономеров. Они могут быть нанесены на поверхность металла в виде пленки, покрывая его и предотвращая проникновение влаги и кислорода.
Полимерные покрытия обладают высокой адгезией к поверхности металла, что обеспечивает прочное соединение между покрытием и металлом. Они также имеют хорошую устойчивость к атмосферным воздействиям, ультрафиолетовому излучению и химическим веществам, что позволяет им сохранять свои защитные свойства в течение длительного времени.
К полимерным покрытиям относятся различные типы полимеров, такие как эпоксидные, полиуретановые и полиэфирные. Каждый из них обладает своими особенностями и применяется в различных условиях, в зависимости от требований защиты и эксплуатационных характеристик металла.
Полимерные покрытия могут быть нанесены на поверхность металла различными способами, такими как нанесение в виде жидкой эмульсии, нанесение покрытия в порошке и последующая термическая обработка, либо методом электростатического нанесения. Это позволяет достичь равномерного и прочного слоя, который обеспечивает надежную защиту металла от коррозии.
Полимерные покрытия являются одним из наиболее эффективных способов защиты металла от коррозии без покраски. Они обладают высокой стойкостью к воздействию окружающей среды и механическим повреждениям, что делает их идеальными для использования в различных отраслях промышленности.
Электрохимическая защита
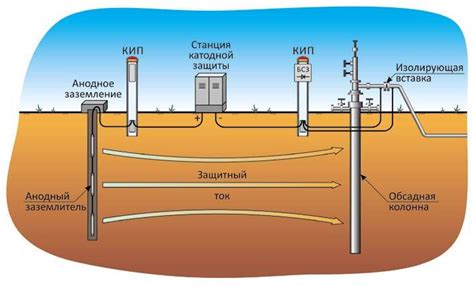
Электрохимическая защита является эффективным и долговечным способом защиты металла от коррозии без необходимости покраски. Основной принцип этого метода заключается в создании электрической связи между металлом, который нужно защитить (который называется анодом), и более активным металлом (который называется катодом).
Процесс электрохимической защиты основан на использовании гальванической пары, в которой катодом выступает активный металл, обычно цинк или алюминий, а анодом – защищаемый металл. При этом, катод больше по площади, чем анод. Таким образом, создается электрическая цепь, через которую идет ток, что способствует сохранению металла от коррозии.
Для эффективной электрохимической защиты металла от коррозии необходимо правильно подобрать катодный материал и обеспечить надлежащий контакт между анодом и катодом. Для этого часто используют специальные анодные комплекты или покрытия, состоящие из гальванической пары между металлом и цинком или алюминием. Также возможно использование пассивных анодов, которые создают защитный слой на поверхности металла и предотвращают его окисление.
При правильном применении электрохимической защиты можно значительно увеличить срок службы металлических конструкций и снизить расходы на их обслуживание и ремонт. Однако, следует учитывать, что электрохимическая защита не является универсальным решением и требует профессиональной экспертизы для подбора оптимальных параметров и компонентов системы защиты.
Вопрос-ответ

Какие способы можно использовать для защиты металла от коррозии без покраски?
Для защиты металла от коррозии без покраски можно использовать различные методы. Один из них - антикоррозийное покрытие, которое предотвращает проникновение влаги и кислорода на поверхность металла. Другим способом может быть применение антикоррозийных пленок или антикоррозийной ленты. Ещё одним вариантом является гальваническая защита, при которой металл, который находится в более высоком электрохимическом ряду, служит анодом для защиты более благородных металлов.
Как работает антикоррозийное покрытие?
Антикоррозийное покрытие создаёт защитный слой на металлической поверхности, который предотвращает контакт металла с воздухом и влагой. В результате этого, металл не окисляется и не образуется коррозия. Антикоррозийные покрытия могут быть различными по составу и способу нанесения, например, это может быть эпоксидная смола, полиуретановый клей или специальные антикоррозийные краски.
Что такое антикоррозионные пленки?
Антикоррозионные пленки - это специальные самоклеящиеся покрытия, которые накладывают на поверхность металла. Они служат защитой от воздействия влаги, газов и других агрессивных веществ. Антикоррозионные пленки можно использовать как временную меру защиты металла, например, при транспортировке или хранении, либо, как постоянную защиту, если не планируется нанесение покрытий или покраска металла.
Каким образом осуществляется гальваническая защита металла?
Гальваническая защита металла происходит благодаря созданию гальванической пары с использованием более благородного металла. Более благородный металл, который находится в более высоком электрохимическом ряду, называется анодом, а защищаемый металл - катодом. Анод и катод соединяют между собой источником электрического тока (батареей или аккумулятором) таким образом, что анод будет расходоваться, а катод будет защищаться от коррозии.
