Формулы металлов являются важным компонентом науки о материалах и широко применяются в различных областях, начиная от металлургии и электроэнергетики, и заканчивая промышленными процессами и технологиями строительства. Правильное написание формул металлов имеет большое значение, так как оно позволяет четко и точно обозначить состав материала и его свойства.
Особенностью формул металлов является то, что они позволяют описать атомную структуру материала. В основе формул металлов лежат химические символы элементов, из которых состоит металл. Для каждого элемента используется отдельный символ, который записывается с большой буквы. Элементы связываются между собой специальными знаками и прямыми линиями, которые указывают на наличие химической связи.
Правила написания формул металлов включают в себя определенные соглашения, которых необходимо придерживаться. Во-первых, элементы записываются в формуле в том порядке, в котором они расположены в веществе. Во-вторых, если атомы одного элемента повторяются несколько раз, то их количество записывается в виде индекса после символа элемента. Кроме того, в формулах металлов используются знаки «+» и «-», которые указывают на положительный или отрицательный заряд атомов.
Правильное написание формул металлов является важным навыком для специалистов в области материаловедения и обеспечивает точность и ясность в передаче информации о составе и свойствах материалов. Основные правила и соглашения помогают сделать формулы металлов понятными и удобочитаемыми, что упрощает их использование в различных областях науки и промышленности.
Правильное написание формулы металла

При написании формулы металла необходимо учесть некоторые особенности и следовать определенным правилам. Формула металла указывает на его химический состав и вещественный состав, что имеет большое значение при производстве металлургических изделий.
Первым этапом в написании формулы металла является указание его химического элемента, краткое обозначение которого записывается в верхнем индексе. Например, Fe - железо, Cu - медь, Al - алюминий.
Далее следует указать вещественный состав металла, который записывается в виде десятичной дроби. Вещественный состав указывает процентное содержание примесей и легирующих элементов в металле. Например, для указания массовой доли нужно использовать символы "м.д.", а для указания объемной доли - символы "о.д.". Например, Fe85Cr15 означает, что металл содержит 85% железа и 15% хрома.
При написании формулы металла также необходимо учитывать возможное наличие полиграфических знаков, которые указывают на отличия от обычного химического элемента. Такие знаки могут быть добавлены перед формулой элемента или после нее. Например, Fe* - железо с повышенной стойкостью или FeLi - железо с добавкой лития.
Важно помнить, что формула металла должна быть четко и однозначно описана, чтобы исключить возможные ошибки в процессе производства и использования металлургических изделий. Правильное написание формулы металла позволяет более точно контролировать его свойства и качество, что важно для различных отраслей промышленности.
Особенности и правила

Правильное написание формулы металла является важным аспектом в области химии и материаловедения. Для точного определения состава и свойств металла необходимо правильно представить его формулу, которая обычно состоит из символов химических элементов и их количества.
Одной из особенностей написания формулы металла является правило задания заряда элементов. Обычно заряд указывается в верхнем правом углу символа элемента. Для положительных зарядов используется знак "+", а для отрицательных - знак "-". Это помогает установить ионный состав металла и его способность образовывать соединения с другими веществами.
Кроме того, следует учитывать правила приоритетности ионов в формуле металла. Например, если в составе металла присутствуют ионы с разным зарядом, то ионы с меньшим зарядом указываются в формуле первыми, а с большим - вторыми. Это позволяет сравнивать и анализировать формулы металлов и предсказывать их свойства.
Также важным правилом написания формулы металла является указание количества атомов каждого элемента. Обычно количества атомов элементов указываются с помощью цифр, например, Fe2O3 - формула ржавчины, в которой указано, что на каждый атом железа приходится два атома кислорода.
В заключение, правильное написание формулы металла играет важную роль в определении его химических и физических свойств. Знание особенностей и правил составления формулы позволяет более точно анализировать и понимать свойства металла, а также способствует эффективному взаимодействию с другими веществами.
Компоненты формулы металла

Формула металла состоит из нескольких компонентов, каждый из которых вносит свой вклад в общую картину. Вот основные компоненты, которые следует учитывать при написании формулы:
- Химический символ: наиболее распространенный и узнаваемый компонент формулы металла. Он обозначает конкретный металл и записывается заглавными буквами. Например, Fe для железа или Cu для меди.
- Атомный номер: указывает порядковый номер металла в периодической системе элементов и является уникальным для каждого металла. Он записывается нижним индексом справа от химического символа. Например, Fe26 или Cu29.
- Молярная масса: определяет массу одного моля металла и записывается в граммах. Она указывается вверху химического символа, перед индексом атомного номера. Например, Fe55.845 или Cu63.546.
- Степень окисления: выводится в виде римских цифр и указывает на заряд и валентность металла. Она записывается в верхнем индексе справа от химического символа. Например, FeIII или CuII.
Эти компоненты вместе образуют полную формулу металла, которая точно идентифицирует конкретное вещество и описывает его химические свойства. Важно соблюдать правила и порядок написания этих компонентов, чтобы избежать недоразумений и понятно передать информацию о металле.
Ионное состояние элементов и их заряды

Ионное состояние элементов - это форма существования атомов, в которой они образуют ионы, то есть заряженные элементарные частицы. Заряд ионов может быть положительным или отрицательным, и он определяется количеством потерянных или полученных электронов.
Ионы с положительным зарядом называются катионами. Они образуются тогда, когда атом теряет один или несколько электронов. Обычно катионы имеют заряд, равный числу потерянных электронов. Например, ион натрия Na+ образуется путем потери одного электрона.
Ионы с отрицательным зарядом называются анионами. Они образуются тогда, когда атом получает один или несколько электронов. Обычно анионы имеют заряд, равный числу полученных электронов. Например, ион кислорода O2- образуется путем получения двух электронов.
Ионное состояние и заряд элементов можно определить по их электронной конфигурации. В таблице Менделеева указано ионное состояние некоторых химических элементов.
| Элемент | Ионное состояние |
|---|---|
| Калий (K) | K+ |
| Хлор (Cl) | Cl- |
| Магний (Mg) | Mg2+ |
| Фосфор (P) | P3- |
Знание ионного состояния элементов и их зарядов позволяет правильно записывать химические формулы, а также понимать как происходят химические реакции и взаимодействия элементов.
Важно: Ионное состояние элементов и их заряды могут меняться в зависимости от условий реакции или соединения с другими веществами.
Правила записи ионных формул
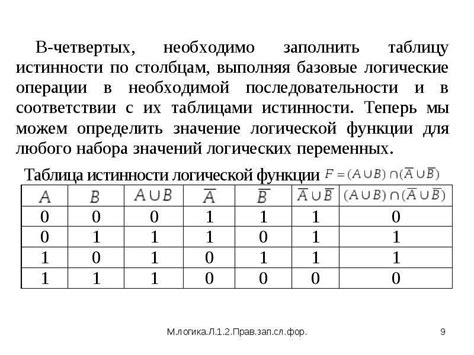
Ионные формулы представляют собой запись состава ионных соединений. Они показывают, какие ионы присутствуют в соединении и в каком количестве. Важно правильно записывать ионные формулы, чтобы передать информацию о составе соединения и его заряде.
Основное правило при записи ионных формул - записывать сначала положительные ионы (катионы), а затем отрицательные ионы (анионы). Например, в формуле для хлорида натрия - NaCl, сначала идет ион натрия (Na+), а затем ион хлорида (Cl-).
Для указания количества ионов в формуле используют цифры. Если количество ионов одного вида равно 1, то цифру указывать не обязательно. Например, в формуле для хлорида натрия (NaCl) цифра 1 не пишется. Если количество ионов различно, цифру указывают после химического символа иона. Например, в формуле для сульфата магния - MgSO4, цифра 4 указывает, что в соединении присутствует 4 иона кислорода (O2-).
Приведенным выше правилам следуют при записи ионных формул, однако есть ряд исключений. Например, у некоторых металлов может быть несколько зарядов, их указывают в римских цифрах после химического символа металла. Также в формуле для многоатомных ионов используются скобки и цифры для показа их количества.
Знание правил записи ионных формул является важным при изучении химии. При правильной записи формул можно получить полную информацию о составе и свойствах ионного соединения. Следование правилам позволяет создавать более точные и удобочитаемые записи, облегчающие изучение и анализ химических соединений.
Ионные радиусы и их влияние на формулу

Ионные радиусы являются важными параметрами, которые влияют на формулу металла. Они определяют размер ионов в решетке металла и влияют на его химические и физические свойства.
Расчет ионных радиусов проводится на основе экспериментальных данных и включает в себя измерение расстояния между ионами и определение их размеров. Ионный радиус определяется как половина расстояния между ионами в кристаллической решетке.
Ионные радиусы могут быть положительными или отрицательными, что зависит от заряда иона. Положительно заряженные ионы называются катионами, а отрицательно заряженные – анионами. Размеры катионов и анионов могут различаться, что влияет на формулу металла.
Ионные радиусы определяются в таблице ионных радиусов и могут быть различными для разных элементов. Например, в межметаллическом соединении NaCl размер натриевого иона (Na+) будет меньше, чем размер хлоридного иона (Cl-), что отражается в формуле NaCl.
Знание ионных радиусов является важным для правильного написания формулы металла, так как размер ионов вещества будет влиять на его структуру и свойства. Поэтому при составлении формулы необходимо учитывать ионные радиусы, чтобы правильно определить соотношение элементов в соединении.
Особенности записи координационных формул

Координационные формулы являются специальным способом записи соединений металлов с другими элементами. Их особенностью является использование сложных структур, которые передают информацию о взаимодействии атомов в подсоединениях.
В координационных формулах важно правильно указать основной металл, к которому присоединяется другой элемент. Для этого используется знак "+" или обозначение "Me", которое означает металл. Например, формула комплексного соединения меди и аммиака будет выглядеть как Cu(NH3)42+.
Также в координационной формуле важно указывать координационное число металла, то есть количество атомов, к которым присоединены другие элементы. Если все атомы аммиака присоединены к одному атому меди, то указывается число "4" внизу справа от знака "+" или "Me".
Для удобства чтения координационных формул используются парные скобки "[" и "]", которые обозначают комплекс соединения. Например, формула комплекса меди и цианида будет записываться как [Cu(CN)2]2-.
Важным элементом записи координационных формул является использование правил номенклатуры. Координационное соединение получает название от основного металла с указанием его окислительного состояния. Например, [Cu(NH3)4]+2 - это тетрааммин(II) ион меди.
В заключение следует отметить, что запись координационных формул представляет собой важный элемент изучения химии комплексных соединений. Правильное оформление формул позволяет более точно передавать информацию об атомных взаимодействиях и имеет большое значение в научных и практических исследованиях.
Центральный атом и лиганды

Центральный атом в химической формуле металла играет важную роль, так как он определяет химические свойства и реакционную способность металла.
Лиганды — это атомы или молекулы, которые приходят в контакт с центральным атомом и образуют комплексы. Они могут быть трех- или четырехзубыми, взаимодействуя с центральным атомом через свои валентность.
Лиганды прикрепляются к центральному атому металла через координационную связь, где один из атомов молекулы лиганда делится своей электронной оболочкой с центральным атомом. Это создает особый тип химической связи, называемый координационной связью.
В составе молекул металлов можно выделить различные позиции для разных лигандов. Наиболее распространенными являются позиции октаэдра и куба. В октаэдральной структуре центральный атом металла окружен шестью лигандами на постоянном расстоянии друг от друга. В кубической структуре центральный атом окружен восемью лигандами, расположенными на кубической сетке.
Расположение лигандов вокруг центрального атома определяет степень сферичности и симметрии комплекса. Это в свою очередь влияет на его структуру, свойства и возможные реакции. Правильное написание формулы металла с учетом центрального атома и лигандов значительно влияет на понимание его химических свойств и реакционной активности.
Многозарядные ионы в формулах
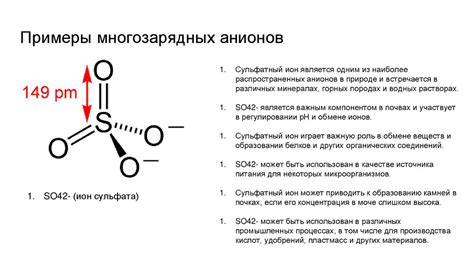
Формулы металлов представляют собой составление химического символа металла и указания заряда. Заряд металла обозначается в виде верхнего индекса справа от символа металла. Однако, иногда металлы образуют ионы с разными зарядами, называемыми многозарядными ионами.
Многозарядные ионы образуются из металлов, у которых есть несколько степеней окисления. Например, медь может образовывать ионы Cu+ и Cu2+, железо может образовывать ионы Fe2+ и Fe3+. Для указания заряда многозарядного иона в формуле металла, после символа металла ставят знак соответствующего заряда и затем указывают число, обозначающее количество данных ионов.
При записи формулы, многозарядный ион указывается в скобках и после него указывается число, обозначающее количество данных ионов в соединении. Например, формула для сульфата железа(II) будет иметь вид Fe(SO4)2.
Важно учитывать, что в сульфате железа(II) содержится два иона железа с зарядами 2+. Поэтому, запись формулы с использованием скобок позволяет точно указать наличие многозарядного иона в соединении и избежать путаницы.
Вопрос-ответ

Какие особенности и правила нужно знать для правильного написания формулы металла?
Для правильного написания формулы металла необходимо знать его название, заряд и числовую величину заряда. Название металла записывается с заглавной буквы, а заряд указывается с помощью римских цифр в верхнем индексе после названия металла. Если у металла только один возможный заряд, то указывать его необязательно. В случае, если металл имеет несколько возможных зарядов, необходимо указать числовую величину заряда, добавив в нижний индекс арабские цифры. Например, формула для железа Fe может быть Fe2+ или Fe3+, в зависимости от заряда.
Как я могу узнать заряд и числовую величину заряда металла?
Заряд и числовую величину заряда металла можно узнать из таблицы Менделеева, где указаны все химические элементы и их характеристики. В таблице указаны также возможные заряды для каждого металла. Если указано только одно значение заряда, значит у металла только один возможный заряд. Если указано несколько значений, то в нижний индекс записывается числовая величина заряда.
Могут ли у металла быть разные заряды и как это влияет на его формулу?
Да, у металла могут быть разные заряды. Если металл имеет только один возможный заряд, то его формула записывается просто с названием металла. Например, медь - Cu. Если у металла есть несколько возможных зарядов, то числовую величину заряда указывают в виде арабских цифр в нижнем индексе после названия металла. Например, железо - Fe2+ или Fe3+. Таким образом, заряд металла влияет на его формулу и указывается с помощью римских цифр для одного заряда и арабских цифр для нескольких зарядов.
