Щелочные металлы являются важной группой элементов, которые встречаются в природе и широко используются в различных областях. Распознать щелочной металл несложно, если вы знаете их основные признаки и свойства. Они включают в себя шесть элементов периодической таблицы: литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Основной признак щелочных металлов – их активность. Они являются очень реактивными и легко реагируют с другими элементами, особенно с кислородом и водой. При контакте с водой они образуют щелоочистительные растворы, поэтому и получили своё название. Кроме того, щелочные металлы отличаются низкой плотностью, низкой температурой плавления и высокой электропроводностью.
Важно отметить, что щелочные металлы обладают уникальными свойствами, которые делают их полезными в промышленности и технологии. Они используются для производства щелочных батарей, сплавов для лёгких конструкций, косметических продуктов и даже в ядерной энергетике. При их использовании необходимо быть осторожными, так как они могут быть ядовитыми и опасными при неправильном обращении.
В заключение, распознать щелочной металл несложно, учитывая их основные признаки и свойства. Активность, низкая плотность, низкая температура плавления и высокая электропроводность – все это характеристики щелочных металлов. Их уникальные свойства сделали их важными и используемыми элементами в различных отраслях, от промышленности до медицины. Но помните, что обращение с щелочными металлами требует осторожности и соблюдения особых мер предосторожности.
Щелочные металлы: общая информация

Щелочные металлы – это группа элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они обладают низкой плотностью и низкой температурой плавления. Часто встречаются в природе в виде солей, оксидов и гидроксидов.
Основные свойства щелочных металлов: они обладают высокой химической реакционностью, способностью образовывать оксиды и гидроксиды, растворимые в воде. Они также хорошие проводники электричества и тепла.
Щелочные металлы являются сильными щелочами, они реагируют с кислотами, образуя соли. Они также обладают способностью образовывать амфотерные соединения, способные проявлять кислотные и основные свойства в зависимости от условий.
Щелочные металлы находят широкое применение в различных отраслях промышленности и научных исследованиях. Например, они используются для производства щелочных батарей, сплавов для литейных целей, в процессе синтеза органических соединений и многом другом.
На сегодняшний день изучение и применение щелочных металлов является одной из актуальных задач в химической и материаловедческой науке. Эти элементы имеют широкий спектр свойств, что открывает возможности для создания новых материалов и технологий.
Основные признаки щелочных металлов
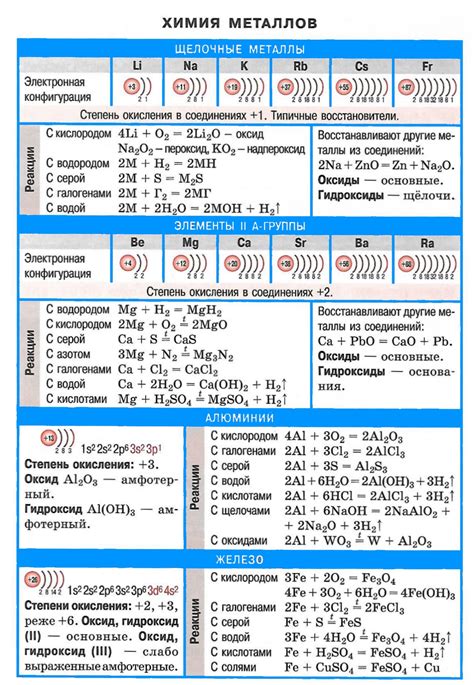
Щелочные металлы – это группа элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они обладают рядом характерных признаков, отличающих их от других элементов.
Первый основной признак щелочных металлов – это низкая плотность. В сравнении с другими металлами, щелочные металлы имеют очень низкую плотность, что делает их легкими и мягкими веществами.
Вторым основным признаком щелочных металлов является их высокая активность. Они являются самыми реактивными металлами в периодической системе элементов. Они легко реагируют с водой и воздухом, образуя горючие вещества и выделяя газы.
Третий признак – это низкая температура плавления и кипения щелочных металлов. Они плавятся и кипят при очень низких температурах, что делает их прекрасными материалами для использования в высокотемпературных процессах.
Четвертым признаком щелочных металлов является их способность образовывать оксиды. Эти оксиды обладают щелочными свойствами и растворяются в воде, образуя щелочные растворы.
Пятый признак – это химическая реакция щелочных металлов с кислородом. Щелочные металлы активно реагируют с кислородом, образуя оксиды металлов.
Особенности и свойства щелочных металлов

Щелочные металлы – это элементы химической группы I периодической системы Менделеева. Включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они обладают рядом уникальных свойств, отличающих их от других элементов.
Во-первых, щелочные металлы являются самыми реакционными металлами. Они легко образуют соединения с другими элементами, особенно с кислородом и водой. При контакте с водой они мгновенно реагируют, образуя щелочные растворы и выделяя водород. Это делает их опасными в обращении.
Во-вторых, щелочные металлы обладают низкими температурами плавления и кипения. Они являются мягкими и легкими металлами, которые могут быть разрезаны ножом. Некоторые щелочные металлы, такие как литий и калий, могут быть легко растрясти пальцами.
В-третьих, щелочные металлы обладают высокой электроотрицательностью. Они проявляют способность к образованию ионов с положительным зарядом и взаимодействуют с отрицательно заряженными ионами и молекулами. Это делает их полезными в различных химических реакциях и применениях, включая производство щелочных батарей, сплавы и стекла.
В-четвертых, щелочные металлы обладают высокой проводимостью электричества и тепла. Их атомы легко сдвигаются, позволяя электронам свободно передвигаться, что делает их хорошими проводниками электричества и тепла. Эта особенность делает щелочные металлы важными компонентами в различных электрических устройствах и технологиях.
В-пятых, щелочные металлы обладают высокими степенями окисления. Они способны образовывать соединения с положительными зарядами, что отражается в химических реакциях и их способности образовывать ионы.
В заключении следует отметить, что особенности и свойства щелочных металлов делают их уникальными и важными в различных областях жизни, включая промышленность, электронику и химию.
Вопрос-ответ

Какие основные признаки щелочного металла?
Основными признаками щелочных металлов являются: низкая плотность, низкая температура плавления, мягкость, большая реакционная способность с водой и кислородом.
Какие свойства характерны для щелочных металлов?
У щелочных металлов характерны следующие свойства: низкая твердость, жидкость при комнатной температуре, чтобы их перевести в твердое состояние, необходимо очень низкую температуру и высокое давление.
В чем заключается реакционная способность щелочных металлов?
Реакционная способность щелочных металлов проявляется в их способности активно вступать в реакцию с водой и кислородом. При реакции с водой они выделяют большое количество теплоты и образуют гидроксиды, а с кислородом образуют оксиды. Это делает щелочные металлы опасными в хранении и использовании.
