Щелочные металлы – это элементы периодической системы, которые характеризуются высокой активностью икомбинативными свойствами. На сегодняшний день существует несколько способов получения щелочных металлов, одним из которых является электролиз водных растворов их солей. Этот метод позволяет получать щелочные металлы с высокой степенью чистоты и в больших количествах.
Процесс электролиза водных растворов солей щелочных металлов основан на разложении электролита под действием электрического тока. Для проведения электролиза необходимо использовать специальное устройство – электролизер, состоящий из двух электродов, анода и катода, погруженных в электролит. При подключении к электрическому току на аноде происходят окислительные реакции, а на катоде – восстановительные.
Одной из особенностей электролиза щелочных металлов является высокая степень их ионизации. Это связано с тем, что вода может образовывать гидроксидные ионные комплексы с щелочными металлами, которые затем диссоциируют на ионы. В результате электролиза водяного раствора солей щелочных металлов на катоде выделяется соответствующий металл, а на аноде образуется кислород или хлор.
Методы получения щелочных металлов электролизом
Щелочные металлы, такие как натрий и калий, могут быть получены электролизом водных растворов их солей. Этот метод является одним из наиболее широко используемых при производстве щелочных металлов.
В процессе электролиза водных растворов солей щелочных металлов, таких как хлориды или гидроксиды, происходит разложение электролита под действием постоянного электрического тока. Этот процесс происходит в электролитической ячейке, состоящей из анода и катода, разделенных электролитом.
Анодом в электролизе водных растворов солей щелочных металлов обычно служит платиновый или кислородный электрод, который окисляет воду и образует кислород. При этом на катоде осуществляется восстановление металла, прилипающий в виде металлического осадка.
Электролизаторы для производства щелочных металлов имеют высокую эффективность, так как наличие воды в растворе позволяет проводить электролиз при низкой температуре и поддерживать стабильность процесса. Кроме того, электролизаторы могут быть масштабированы для производства необходимого количества металла.
Итак, метод получения щелочных металлов электролизом водных растворов их солей является эффективным и широко используемым при производстве этих металлов. Он позволяет получать чистые и высококачественные изделия без применения сложных или дорогостоящих процессов.
Электролиз водных растворов солей

Электролиз водных растворов солей является эффективным методом получения щелочных металлов. Он основан на использовании электрического тока для разложения солей на ионы в растворе. Этот процесс позволяет извлечь щелочные металлы из их соединений и получить их в чистом виде.
Для электролиза водных растворов солей требуется основное оборудование, такое как электролитическая ячейка и источник постоянного тока. В процессе электролиза в ячейке размещаются два электрода - катод и анод. Катодом является отрицательно заряженный электрод, а анод - положительно заряженный.
Катод привлекает положительно заряженные ионы металла из раствора, в то время как анод привлекает отрицательно заряженные ионы. Как только ионы достигают электродов, они получают или отдают электроны, претерпевая реакцию окисления или восстановления, и соответственно переходя в раствор или осаждаясь на электроде.
Электролиз позволяет получить щелочные металлы в высокой степени чистоты, поскольку избыточные примеси остаются в растворе. Кроме того, этот метод позволяет контролировать процесс получения металла, изменяя условия электролиза, такие как ток, время и концентрация раствора. Электролиз водных растворов солей является важным и широко применяемым методом получения щелочных металлов в промышленности.
Методы получения щелочных металлов из расплавов
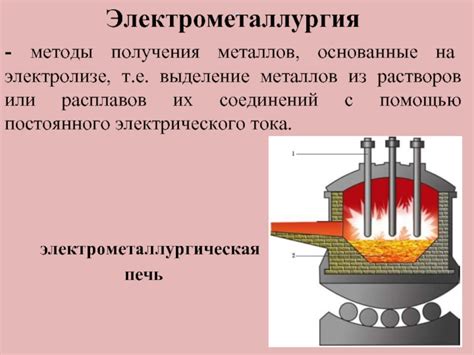
Щелочные металлы, такие как литий, натрий, калий и др., могут быть получены из их расплавов при помощи различных методов.
Один из методов - это электролиз расплава. В этом случае, вода или другие субстанции добавляются к расплаву, которые помогают проводить электрический ток через него. Через электролиз щелочные металлы извлекаются в виде катионов из расплава и осаждается на отрицательном электроде. Этот метод является одним из наиболее эффективных способов получения щелочных металлов из расплавов.
Другой метод - это химическое восстановление. При этом, растворимые соединения щелочных металлов подвергаются химическим реакциям, в результате которых образуются осадки или отвердевающие массы. Эти массы затем подвергаются различным процессам очистки и выделения щелочных металлов. Химическое восстановление широко применяется в промышленности для получения значительных объемов щелочных металлов.
Еще один метод - это экстракция. При экстракции используют растворители, которые способны выделять щелочные металлы из расплавов. Растворитель погружается в расплав и абсорбирует металлы, а затем происходит процесс разделения, где щелочные металлы извлекаются из растворителя.
Методы получения щелочных металлов из расплавов имеют широкое применение в различных отраслях промышленности, таких как производство батарей, лужение металлов и многих других.
Пониженные температуры электролиза
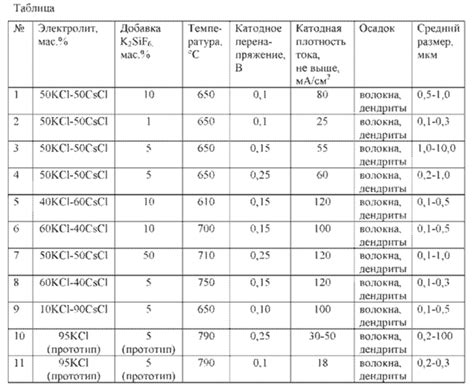
При электролизе водных растворов солей щелочных металлов возможна работа при пониженных температурах. Это связано с тем, что электролиз водных растворов солей щелочных металлов обычно проводится в высокотемпературных условиях.
Однако при использовании особого типа электролизных ячеек, называемых "томическими электролизерами", можно добиться эффективного электролиза при пониженных температурах. Эти ячейки состоят из твердых электролитов, которые обеспечивают быструю передачу ионов внутри ячейки.
Электролиз при пониженных температурах имеет ряд преимуществ. Во-первых, он позволяет экономить энергию, так как не требует нагревания раствора. Во-вторых, он уменьшает риск возникновения нежелательных побочных реакций, так как при пониженной температуре скорость химических реакций существенно снижается.
Однако электролиз при пониженных температурах требует использования специального оборудования и методов. Также он может быть менее эффективным, чем электролиз при высоких температурах, из-за более низкой проводимости электролита и меньшей скорости передачи ионов.
Подготовка электролита для электролиза
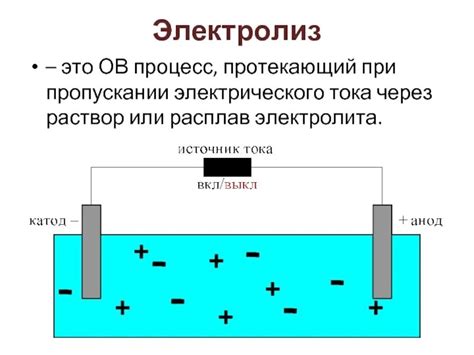
Электролит для электролиза представляет собой водный раствор соли щелочного металла, который играет роль проводника электрического тока и источника ионов металла для процесса электролиза. Подготовка электролита является важным этапом в получении щелочных металлов электролизом.
Первоначально необходимо подобрать подходящую соль щелочного металла, учитывая ее растворимость, стабильность и электрохимические свойства. Чаще всего для электролиза используются хлориды, гидроксиды или карбонаты щелочных металлов.
Затем следует провести растворение выбранной соли в дистиллированной воде. Важно учесть пропорции, чтобы достичь оптимальной концентрации электролита. Далее раствор может быть дополнительно очищен или фильтрован для удаления примесей и сортировки частиц.
Если требуется получить чистый металл, то после подготовки электролита возможно применение дополнительных методов очистки, таких как электроосаждение или дистилляция, для удаления из раствора примесей и получения чистого продукта.
Важно строго соблюдать меры безопасности при подготовке электролита, так как некоторые соли щелочных металлов являются токсичными и опасными веществами. Перед началом работы необходимо ознакомиться с инструкциями по безопасности и использовать соответствующую защитную экипировку.
Особенности электролита для получения щелочных металлов

Для электролиза водных растворов солей щелочных металлов необходимо выбрать подходящий электролит, который обеспечит эффективность процесса и высокую чистоту получаемых металлов. В качестве электролита чаще всего используют растворы гидроксидов или карбонатов щелочных металлов.
Важной особенностью электролита является его концентрация, которая должна быть достаточной для обеспечения достаточной проводимости раствора. Однако слишком высокая концентрация может привести к возникновению побочных реакций или сложностей при дальнейшей обработке полученных продуктов.
Еще одной важной характеристикой электролита является его pH-значение. Для получения щелочных металлов оптимальным является нейтральное pH-значение, которое достигается при добавлении кислоты или щелочи в зависимости от среды.
Также следует обратить внимание на примеси, содержащиеся в электролите. Они могут влиять на качество получаемых металлов, поэтому перед проведением электролиза рекомендуется очистить и обезвожить электролит от нежелательных примесей.
- Эффективность процесса электролиза
- Высокая чистота получаемых металлов
- Растворы гидроксидов или карбонатов щелочных металлов
- Оптимальное pH-значение
Таким образом, выбор и подготовка электролита играют важную роль в процессе получения щелочных металлов электролизом водных растворов их солей.
Вопрос-ответ

Каким образом можно получить щелочные металлы электролизом?
Щелочные металлы могут быть получены электролизом водных растворов их солей. Для этого необходимо использовать специальные установки и аппараты, которые позволяют проводить электролиз с высокой эффективностью и выходом продукта.
Какое оборудование необходимо для проведения электролиза водных растворов солей щелочных металлов?
Для электролиза водных растворов солей щелочных металлов необходимы электролизеры или электролизные ячейки, которые обычно представляют собой две пластины из металла, разделенные мембраной или перегородкой. В эти ячейки помещается раствор соли и проводятся электролизные процессы.
Как происходит электролиз водных растворов солей?
При электролизе водных растворов солей щелочных металлов происходит разложение воды на кислород и водород. Кислород осаждается на аноде, а водород на катоде. Щелочные металлы находятся в виде катионов в растворе и также могут осаждаться на катоде.
Какие факторы могут влиять на эффективность электролиза водных растворов солей?
Факторы, которые могут влиять на эффективность электролиза водных растворов солей, включают концентрацию и свойства соли, температуру раствора, напряжение и ток электролиза, время проведения электролиза и прочие параметры процесса.
Каковы преимущества метода электролиза для получения щелочных металлов?
Метод электролиза водных растворов солей щелочных металлов имеет несколько преимуществ. Во-первых, он позволяет получить высокочистые продукты без примесей, благодаря чему в полученных металлах отсутствуют примеси и превосходные электрические и физические свойства. Во-вторых, метод электролиза является относительно простым и доступным, не требует сложного оборудования и может быть использован в промышленных масштабах.
