Металлы – это химические элементы, которые обладают особыми свойствами: проводят ток, имеют блестящую поверхность и способны образовывать сплавы. Исследование металлов является важным вопросом химии, так как они находят широкое применение в различных отраслях промышленности. Для решения химических задач, связанных с металлами, необходимо знать их возможные степени окисления.
Степень окисления металла – это число, характеризующее относительную потерю или получение электронов металлом в химической реакции. Определение степени окисления металла является неотъемлемой частью решения химических задач. В зависимости от степени окисления металла, он может образовывать различные соединения, что имеет большое значение для понимания и изучения его химических свойств.
Определение возможных степеней окисления металла может быть проведено на основе ряда правил. В некоторых случаях они могут быть предсказаны на основе положения металла в периодической системе элементов. Однако, в других случаях, степень окисления металла необходимо определять экспериментально или с помощью специальных методов, например, осаждением или изменением окружающей среды.
Окисление и степень окисления

Окисление — это химическая реакция, при которой атом либо молекула теряет электроны и повышает свою степень окисления. Степень окисления определяет количество электронов, которые атом получил или потерял при окислении.
Для металлов степень окисления показывает, сколько положительных зарядов носит их ион. Металлы могут иметь различные степени окисления и образовывать ионы с разными зарядами. Например, железо может иметь степень окисления +2 или +3, а медь - +1 или +2.
Определение возможных степеней окисления металла может проводиться с помощью систематического анализа его соединений. Методами химического анализа можно выявить, какие соединения данного металла существуют и какие степени окисления они имеют.
Также можно использовать таблицы степеней окисления для определенных классов металлов. Эти таблицы содержат информацию о возможных степенях окисления каждого металла и могут быть полезными инструментами для определения степени окисления металла в конкретном соединении.
Понимание степени окисления металла важно для понимания его химической активности и свойств. Степень окисления может определять, насколько металл легко отдает или принимает электроны, что влияет на его реактивность и способность образовывать соединения.
Определение степени окисления металла

Степень окисления металла – это числовое значение, которое указывает, сколько электронов металл отдал или принял в ходе окислительно-восстановительных реакций. Определение степени окисления металла имеет большое значение при изучении химических реакций и составления химических уравнений.
Существует несколько методов определения степени окисления металла. Один из них основывается на заряде ионов металла и составлении таблицы, где указываются возможные степени окисления. Например, для металла меди (Cu) возможны степени окисления +1 и +2. При составлении химического уравнения с участием иона меди, необходимо учесть его степень окисления с помощью соответствующего знака.
Другой метод определения степени окисления металла заключается в анализе его окружающей среды и окислительно-восстановительных свойств. В данном случае необходимо изучить химические свойства металла, его реакцию с различными веществами и определить возможные степени окисления на основе полученных данных.
Определение степени окисления металла является важным этапом в изучении его свойств и взаимодействий с другими веществами. Использование различных методов позволяет точно определить степень окисления металла и составить корректные химические уравнения, что необходимо при решении различных химических задач и при проведении научных исследований.
Методы определения степени окисления

Для определения степени окисления металла существуют различные методы, которые основаны на химических и физических свойствах вещества. Эти методы позволяют получить информацию о количестве электронов, которые металл может отдать или принять при взаимодействии с другими веществами.
Одним из самых распространенных методов является использование химических реакций с известными соединениями металла. При этом проводится ряд экспериментов, в результате которых определяется количество электронов, участвующих в реакции и соответственно степень окисления металла.
Другим методом является применение спектроскопических методов, которые позволяют анализировать спектры поглощения или испускания электромагнитного излучения металла. Эти спектры зависят от энергетических уровней электронов и позволяют определить возможные степени окисления.
Еще одним методом является анализ реакций металла с различными реагентами. Путем образования соединений с разными степенями окисления металла можно определить его возможные степени окисления.
Иногда для определения степени окисления металла применяют электрохимические методы, например, использование вольтамперометрии или потенциометрии. Эти методы позволяют измерить потенциал электродов и определить степень окисления металла.
Таким образом, существует несколько методов определения степени окисления металла, каждый из которых имеет свои преимущества и недостатки и выбор метода зависит от конкретной задачи и доступных инструментов.
Химические реакции для определения степени окисления
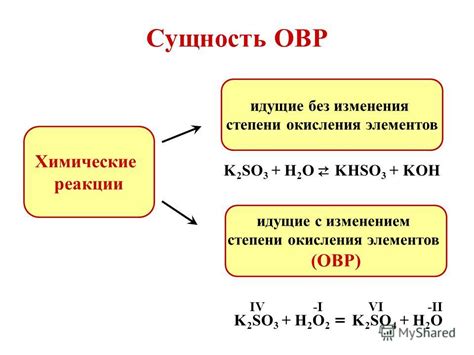
Определение степени окисления металла может быть выполнено при помощи химических реакций, которые основаны на изменении окислительных способностей самого металла или его ионов.
Одним из стандартных методов определения степени окисления металла является использование различных окислительных и восстановительных реакций. Например, восстановление металлов может быть проведено путем взаимодействия с кислородом из воздуха или окиси водорода в водной среде. Реакции восстановления помогают определить, в каком состоянии находится металл - с положительной или отрицательной степенью окисления.
Другим способом определения степени окисления металла является взаимодействие его ионов с различными окислителями или восстановителями. Например, в реакции с хлоридом водорода металлический ион может быть окислен, а его степень окисления определена по количеству выделяющегося хлора. Также можно использовать взаимодействие металлических ионов с растворами аммиака или оксида азота, что также позволяет определить степень окисления.
Для определения степени окисления металла можно также использовать титрование. При этом, известное количество вещества, содержащего металл с неизвестной степенью окисления, реагирует с раствором окислителя или восстановителя. Результаты титрования могут быть использованы для определения степени окисления металла в исходном веществе.
Практическое применение определения степени окисления

Определение степени окисления металла имеет широкое практическое применение в различных областях науки и промышленности. В химическом анализе и синтезе, а также в процессе производства многих химических соединений, знание степени окисления позволяет контролировать и управлять реакциями.
Одним из основных практических применений определения степени окисления является расчет электронного баланса в химических реакциях. Это позволяет точно определить количество электронов, участвующих в реакции, и составить уравнение реакции с учетом баланса зарядов.
Определение степени окисления металла также необходимо для определения его химических свойств и способности взаимодействовать с другими веществами. Знание степени окисления металла позволяет предсказывать его реакционную активность и использовать его в различных процессах и технологиях.
Другим практическим применением определения степени окисления металла является разработка и исследование различных легированных сплавов с заданными свойствами. Определение степени окисления металла помогает выбирать оптимальные пропорции компонентов для получения желаемых характеристик сплава, таких как прочность, твердость, коррозионная стойкость и другие.
Также степень окисления металла может быть полезна в металлургической промышленности для контроля качества металлических изделий. При изготовлении и обработке металлов часто используется окисление и восстановление, а знание степени окисления позволяет контролировать данные процессы и получать продукцию с заданными свойствами.
Таким образом, определение степени окисления металла имеет широкое практическое применение и является важным инструментом для изучения и использования химических реакций с участием металлов.
Вопрос-ответ

Какие методы можно использовать для определения возможных степеней окисления металла?
Для определения возможных степеней окисления металла можно использовать различные методы, включая анализ химических свойств металла, физических свойств, сравнительный анализ соединений металла с известными степенями окисления и использование специальных методов, таких как электрохимический анализ.
Какие химические свойства металла могут помочь определить его возможные степени окисления?
Химические свойства металла, такие как его реакционная способность с кислотами и щелочами, способность образовывать соли с разными анионами, способность образовывать комплексные соединения и взаимодействовать с другими элементами, могут помочь определить возможные степени окисления металла.
Как сравнительный анализ соединений металла может помочь в определении его возможных степеней окисления?
Сравнительный анализ соединений металла с известными степенями окисления может помочь определить возможные степени окисления металла путем сравнения их химических свойств, степени реакционной способности и способности образовывать соли и комплексные соединения. Например, если металл образует соль с известной степенью окисления и не образует соль с другой степенью окисления, это может указывать на возможную степень окисления металла.
Какой метод наиболее точно позволяет определить возможные степени окисления металла?
Наиболее точным методом определения возможных степеней окисления металла является электрохимический анализ. Этот метод позволяет измерить потенциал окислительно-восстановительных реакций металла и его соединений и определить возможные степени окисления в зависимости от изменения потенциала. Однако он требует специализированных инструментов и навыков, поэтому может быть использован только в специализированных лабораториях.
