Химическая связь между атомами играет важную роль в химии и имеет различные типы. Одним из таких типов связей является химическая связь между металлами. Понимание и определение типа связи между металлами является важной задачей для изучения и практического применения металлургии и материаловедения.
Существует несколько способов определения типа химической связи металлов. Один из них - анализ электронной структуры атомов металла. Металлы имеют особую электронную структуру, которая предполагает наличие свободных электронов в их внешних оболочках. Это делает металлы идеальными проводниками электричества и тепла. Если у металла есть большое количество свободных электронов, то связь между металлами будет являться металлической связью.
Другим способом определения типа связи между металлами является анализ сил притяжения между атомами. Металлы часто образуют между собой ионные связи, когда один металл отдает электроны, становясь положительным ионом, а другой металл принимает эти электроны, становясь отрицательным ионом. Электростатическая сила притяжения между ионами образует ионную связь.
Кроме того, химическая связь между металлами может быть и координационной связью. В этом типе связи один металл предоставляет электроны для образования координационной связи с другим металлом или молекулой. Такая связь образуется из-за различия в электроотрицательности между металлами, которое создает дипольный момент и притяжение между атомами.
Определение химической связи
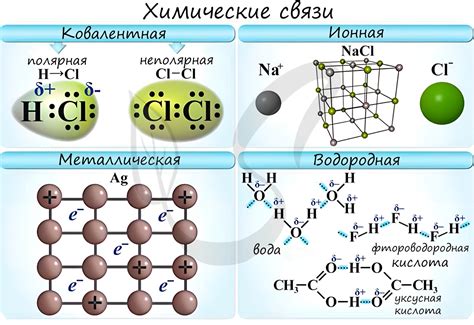
Химическая связь – это физическое явление, связывающее атомы или ионы в молекулах или кристаллах. Химическая связь обеспечивает устойчивость и силу взаимодействия между атомами или ионами в веществе. Определение типа химической связи между металлами имеет большое значение при изучении их химических свойств и реакций.
Взаимодействие между металлами может происходить по различным типам связей:
- Ковалентная связь – это тип химической связи, в котором элементы обменивают электроны между собой. В случае металлов, ковалентная связь может существовать между атомами металлов при образовании их соединений.
- Металлическая связь – это тип химической связи, характерный для металлов. Она основывается на свободном движении электронов в металлической решетке, что обеспечивает соединение атомов металла в единый кристаллический решетчатый образец металла.
- Ионная связь – это тип химической связи между атомами металлов и неметаллов. Основание этого типа связи заключается во взаимном притяжении противоположно заряженных ионов.
Для определения типа химической связи между металлами необходимо изучить их электронную структуру. Химические эксперименты, такие как измерение длины и силы связи, проведение химических реакций и анализ полученных соединений, позволяют более точно определить тип связи и свойства металлов.
Понятие металлической связи

Металлическая связь – это особый тип химической связи, характерный для металлов. Она возникает между положительно заряженными атомами металлов, называемыми катионами, и облаком свободно движущихся электронов, называемых металлическими электронами. В результате металлической связи атомы металлов образуют кристаллическую решётку, в которой катионы расположены в регулярном порядке и окружены электронами.
Особенностью металлической связи является то, что она обладает металлическими свойствами, такими как теплопроводность, электропроводность и пластичность. Электроны, участвующие в металлической связи, могут свободно перемещаться по кристаллической решётке металла, обеспечивая электропроводность. Под влиянием приложенного электрического поля они направляются к положительным зарядам, что объясняет высокую электропроводность металлов.
Металлическая связь также отвечает за другие свойства металлов, такие как пластичность и теплопроводность. Гибкость и пластичность металлов обусловлены способностью слоев катионов металла сдвигаться друг относительно друга без нарушения связи между атомами. Теплопроводность металлов обусловлена способностью электронов передавать энергию при нагревании.
Металлы и их свойства

Металлы являются одним из основных классов химических элементов, которые обладают рядом характерных свойств. Во-первых, металлы хорошие проводники электричества и тепла. Это связано с наличием свободных электронов в их валентной оболочке, которые способны легко передвигаться по металлической структуре. Во-вторых, металлы обладают высокой пластичностью и прочностью. Они могут быть легко вытянуты, изгибаны и прокатаны в различные формы без разрушения. В-третьих, металлы имеют блестящую поверхность, способную отражать свет. Их светоотражающие свойства объясняются наличием свободных электронов, которые могут свободно взаимодействовать с фотонами света.
В таблице Менделеева металлы обычно располагаются в левой части - они занимают около 75% всех химических элементов. Все металлы относятся ко
Химическая связь между металлами и неметаллами

Химическая связь между металлами и неметаллами представляет собой процесс, в результате которого образуется соединение из атомов различных химических элементов. Эти соединения являются основой для создания многочисленных веществ и материалов, таких как соли, окислы и металлические сплавы.
Химическое взаимодействие между металлами и неметаллами основано на передаче электронов от металла к неметаллу. Металлы, обладая низкой электроотрицательностью, обладают свободными электронами в валентной оболочке. Неметаллы, напротив, имеют высокую электроотрицательность, необходимую им для привлечения электронов и создания связи с металлом.
Такое взаимодействие между металлами и неметаллами может приводить к образованию различных типов связей. Одним из таких типов является ионная связь, при которой происходит обмен электронами между атомами металла и атомами неметалла. В результате образуются ионы с противоположными зарядами, которые притягиваются друг к другу и образуют кристаллическую решетку вещества.
Еще одним типом связи между металлами и неметаллами может быть ковалентная связь. В этом случае электроны, необходимые для связи атомов, делятся между атомами металла и неметалла. Такая связь обычно имеет место при образовании молекулных соединений между металлами и неметаллами.
Таким образом, химическая связь между металлами и неметаллами играет важную роль в химии и материаловедении. Она позволяет создавать разнообразные вещества с уникальными свойствами и открывает возможности для разработки новых материалов и технологий.
Как определить химическую связь между металлами
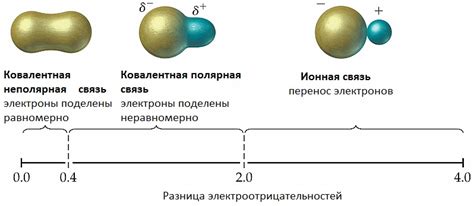
Химические связи между металлами могут быть различными и зависят от ряда факторов, таких как электроотрицательность, размер и структура атомов металлов. Определение типа химической связи между металлами может помочь понять их реакционную способность и свойства.
Одним из основных методов определения типа химической связи между металлами является анализ их электроотрицательности. Если разность электроотрицательностей между металлами невелика, то связь между ними является неполярной ковалентной. В этом случае электроны общие между атомами металлов и образуют область общей электронной плотности.
Если же разность электроотрицательностей между металлами велика, то их связь будет ионной. В ионной связи электроны полностью передаются от одного атома металла к другому, образуя ионы с разными зарядами.
Еще одним способом определения типа химической связи между металлами является исследование структуры кристаллической решетки. В случае ковалентной связи между металлами атомы могут быть связаны ковалентными связями внутри кристаллической решетки. При ионной связи же атомы металлов образуют регулярную кристаллическую решетку с ионами разной полярности.
Также можно использовать методы, основанные на энергии и длине связи между металлами. Ковалентная связь обычно характеризуется более короткой связью и большей связывающей энергией, в то время как ионная связь имеет более длинную связь и меньшую связывающую энергию.
Все эти методы могут быть использованы для определения типа химической связи между металлами. Понимание типа связи между металлами является важным фактором при изучении их химических свойств и реакционной способности.
Примеры химической связи металлов
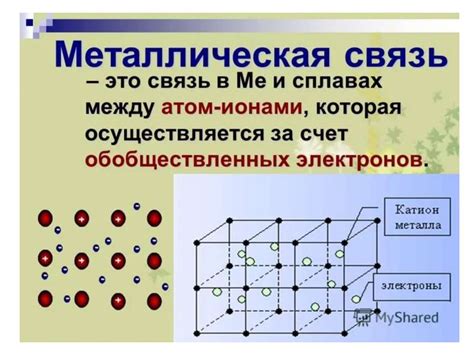
Химическая связь металлов может проявляться в разных формах, в зависимости от их валентности и свойств. Рассмотрим некоторые примеры такой связи:
Ионная связь - одна из наиболее распространенных форм химической связи между металлами и неметаллами. Примером такой связи может служить соединение хлорида натрия (NaCl). В этом соединении натрий (Na) отдает один электрон, становясь положительным ионом (Na+), а хлор (Cl) принимает этот электрон, образуя отрицательный ион хлорида (Cl-). Таким образом, между ними образуется притяжение на основе противоположных зарядов, что и обуславливает силу ионной связи.
Металлическая связь - характерна для чистых металлов или сплавов. В этом типе связи между атомами металла образуется "море" свободных электронов, которые связывают атомы вместе. Примером такой связи может служить металлическое соединение меди (Cu), где атомы меди вписываются в кристаллическую решетку и обмен электронами.
Ковалентная связь - тип связи, который образуется между атомами неметаллов или между атомами металлов с неметаллами при обмене электронами. Некоторые металлы, например, алюминий (Al), образуют соединения с ковалентной связью. Примером такой связи может служить алюминиевый оксид (Al2O3), где атомы алюминия и кислорода образуют связи между собой, обмениваясь электронами.
Каждый из примеров химической связи между металлами имеет свои особенности и определяется взаимодействием между атомами металла и другими элементами. Это самый общий подход к определению типа химической связи, однако в реальности может наблюдаться их совместное влияние и промежуточные формы связи.
Вопрос-ответ

Какие методы можно использовать для определения типа химической связи металлов?
Для определения типа химической связи металлов можно использовать различные методы, такие как рентгеноструктурный анализ, спектроскопия, электронная микроскопия и др. Рентгеноструктурный анализ позволяет определить расстояние между атомами и их угловые параметры, что позволяет сделать выводы о типе связи. Спектроскопические методы, такие как инфракрасная и ядерно-магнитная резонансная спектроскопия, позволяют исследовать особенности электронной структуры металла и его связей. Электронная микроскопия позволяет непосредственно наблюдать структуру металлического соединения и его связей.
Как можно определить, есть ли ионная химическая связь между металлами?
Для определения наличия ионной химической связи между металлами можно использовать несколько методов. Один из них - рентгеноструктурный анализ, который позволяет определить тип связи, исходя из значений расстояний между атомами и угловых параметров. Если расстояние между атомами значительно меньше, чем сумма радиусов атомных окружностей, то это может указывать на наличие ионной связи. Также можно обратить внимание на разность электроотрицательностей металлов: если она достаточно большая, то скорее всего между ними есть ионная связь.
