Оксиды – это химические соединения, которые образуются в результате реакции металла или неметалла с кислородом. В зависимости от типа элемента, содержащегося в оксиде, они могут быть классифицированы как металлические и неметаллические оксиды. Распознать, является ли оксид металлическим или неметаллическим, можно с помощью нескольких химических и физических характеристик.
Первый способ – оксиды металлов обычно обладают металлическим блеском. Это связано с тем, что металлы, входящие в состав оксидов, отражают свет и придают им блестящую поверхность. В то же время, неметаллические оксиды, поскольку не содержат металлов, обычно являются матовыми.
Второй способ – проверка проводимости оксидов. Металлические оксиды являются хорошими проводниками электричества. Это можно проверить, поместив оксид между двумя проводниками и подключив их к источнику тока. Если оксид проводит электрический ток, то он металлический. В свою очередь, неметаллические оксиды обладают низкой проводимостью и не пропускают электрический ток.
Третий способ – реакция оксидов с кислотами. Металлические оксиды обычно реагируют с кислотами, выделяя соответствующую соль – основание. Например, оксид цинка при взаимодействии с соляной кислотой образует хлорид цинка и воду. В то же время, неметаллические оксиды не реагируют с кислотами, поскольку не обладают свойствами оснований.
Важно отметить, что эти методы не являются абсолютными и требуют дополнительной проверки. В химической лаборатории существуют более точные методы определения типа оксида, такие как спектральный анализ или химические тесты. Если у вас есть сомнения, лучше обратиться к специалисту, чтобы получить точный результат.
Что такое металлический оксид и неметаллический оксид?
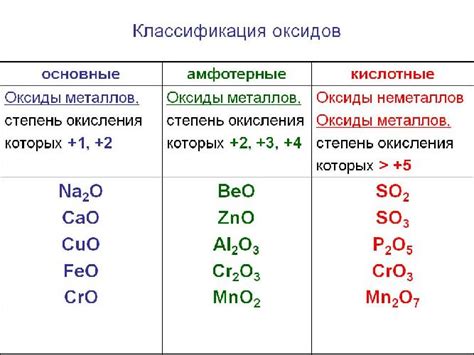
Металлический оксид - это химическое соединение между металлом и кислородом. Оксиды металлов обычно являются твердыми веществами и обладают металлическим блеском. Они образуются в результате окисления металлов, когда металлы вступают в реакцию с кислородом воздуха или растворятся в кислых средах. Металлические оксиды имеют различные физические и химические свойства в зависимости от специфики металла и взаимодействия с кислородом.
Неметаллический оксид - это химическое соединение между неметаллом и кислородом. Оксиды неметаллов, в отличие от металлических оксидов, могут быть как газообразными, так и жидкими или твердыми веществами. Они образуются при соединении неметаллов с кислородом и обычно обладают кислотными свойствами. Неметаллические оксиды могут быть растворимыми в воде и реагировать с ней, образуя кислоты. Они также могут быть растворимыми в щелочах или взаимодействовать с ними, образуя соли.
Металлические оксиды и неметаллические оксиды играют важную роль в химических реакциях и промышленных процессах. Они могут использоваться в качестве катализаторов, красителей, пигментов, абразивов и других материалов. Изучение и распознавание этих оксидов помогает понять их свойства и применение в различных областях науки и промышленности.
Металлический оксид: определение и свойства
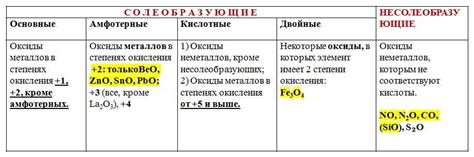
Металлический оксид - это химическое соединение между металлом и кислородом. В металлическом оксиде кислород образует анион O2-, или присоединяется к металлу как кислородный мостик. Металлический оксид образуется в результате окисления металла, то есть взаимодействия его с кислородом.
Металлические оксиды обладают свойствами, характерными для любых кислотных оксидов. Они могут образовывать кислотные растворы или соли, реагировать с щелочами и обладать конкретными физическими свойствами. Например, некоторые металлические оксиды обладают металлическим блеском, хорошей теплопроводностью и электропроводностью.
Металлические оксиды могут быть как базическими, так и амфотерными. Базические оксиды реагируют с кислотами, образуя соли и воду. Амфотерные оксиды могут реагировать и с кислотами, и с щелочами, выполняя функцию как базы, так и кислоты.
Примеры металлических оксидов включают оксид железа (Fe2O3), оксид алюминия (Al2O3), оксид никеля (NiO) и многие другие. Металлические оксиды широко используются в различных отраслях промышленности, включая производство металлов, керамики, стекла и катализаторов.
Неметаллический оксид: особенности и примеры
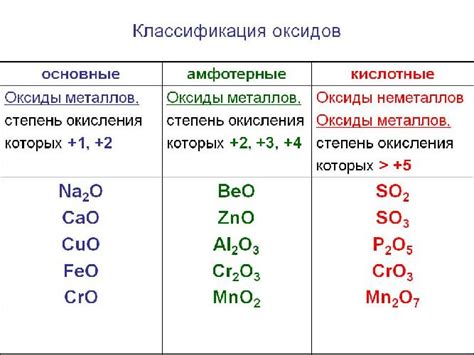
Неметаллические оксиды представляют собой химические соединения, которые образуются при соединении неметаллов с кислородом. Они отличаются от металлических оксидов тем, что не обладают металлическими свойствами, такими как теплопроводность и электропроводность. Неметаллические оксиды часто являются газообразными или твердыми веществами, которые обладают высокими температурами плавления и кипения.
Примером неметаллического оксида является двуокись углерода (CO2). Он образуется при сгорании углеводородных соединений и является основным компонентом атмосферы Земли. Двуокись углерода играет важную роль в природе и является растворителем для растений при фотосинтезе. Однако большое количество двуокиси углерода вызывает парниковый эффект и способствует глобальному потеплению.
Другим примером неметаллического оксида является двуокись серы (SO2). Этот газообразный оксид образуется при сгорании сероводородсодержащих соединений и является причиной образования кислотных дождей. Двуокись серы также является важным промышленным веществом, используемым при производстве серной кислоты.
Не стоит забывать, что неметаллические оксиды могут обладать различной активностью и реактивностью в зависимости от их состава и структуры. Некоторые неметаллические оксиды обладают ядовитыми свойствами и могут представлять опасность для человека и окружающей среды.
Как отличить металлический оксид от неметаллического оксида?

Оксиды представляют собой соединения, которые образуются в результате взаимодействия металлов или неметаллов с кислородом. При этом металлические и неметаллические оксиды имеют различные свойства и характеристики, поэтому их можно отличить друг от друга.
Металлические оксиды обычно имеют металлический блеск и отличаются высокой теплопроводностью и электропроводностью. Они часто являются твердыми веществами при комнатной температуре и могут быть провитые или непровитые. Металлические оксиды могут быть ионными или ковалентными соединениями, в зависимости от типа металла и степени окисления.
Неметаллические оксиды обычно имеют матовый или полуматовый вид и обладают плохой теплопроводностью и электропроводностью. Они могут быть газообразными, жидкими или твердыми веществами при комнатной температуре. Неметаллические оксиды могут быть ковалентными соединениями и образуются в результате соединения неметаллов с кислородом.
Для определения типа оксида можно также использовать таблицу химических элементов, где указаны свойства и характеристики каждого элемента. Таблица поможет определить, является ли элемент металлом или неметаллом, и, соответственно, отличить металлический оксид от неметаллического оксида.
Вопрос-ответ

Какие свойства характеризуют металлические оксиды?
Металлические оксиды обладают высокой электропроводностью и теплопроводностью. Они часто имеют металлический блеск и способны проявлять металлические свойства, такие как гибкость и плавкость.
Какие свойства характеризуют неметаллические оксиды?
Неметаллические оксиды обладают низкой электропроводностью и теплопроводностью. Они часто являются хрупкими и не обладают металлическим блеском. Возможно растворение неметаллических оксидов в воде, что вызывает образование кислотных растворов.
