Молярная масса металла является очень важным параметром, который позволяет определить количество металла вещества в единице объема или массы. Ее вычисление можно осуществить, используя удельную теплоемкость металла. Удельная теплоемкость – это количество теплоты, необходимое для нагревания единицы массы вещества на 1 градус Цельсия. Используя связь между удельной теплоемкостью и молярной массой металла, можно определить величину молярной массы.
Для вычисления молярной массы металла по удельной теплоемкости необходимо знать значение удельной теплоемкости металла и применить следующую формулу: Молярная масса = удельная теплоемкость / универсальная газовая постоянная. Универсальная газовая постоянная является физической постоянной, которая равна 8,314 Дж / (моль * К). Подставив значения в формулу, можно определить молярную массу металла.
Зная молярную массу металла, можно рассчитать его количество вещества в определенной массе или объеме. Это очень полезно для химических расчетов, анализа состава сплавов и других применений. Поэтому, умение вычислять молярную массу металла по удельной теплоемкости является важным навыком для химиков и материаловедов.
Что такое молярная масса?

Молярная масса — это физическая величина, которая показывает массу одного моля вещества. Она измеряется в г/моль. Молярная масса играет важную роль в химии, так как позволяет вычислить количество вещества, исходя из его массы, или наоборот.
Молярная масса рассчитывается путем сложения атомных масс всех элементов, входящих в состав химической формулы вещества. Например, молярная масса воды (H2O) будет равняться 18 г/моль (2 г за два атома водорода и 16 г за один атом кислорода).
Молярная масса играет особую роль в реакционной способности вещества. Она позволяет вычислить количество вещества, участвующего в химической реакции, и предсказывать итоговый результат. Также молярная масса является основой для вычисления других важных физических и химических характеристик вещества, таких как плотность, объем и концентрация растворов.
В химии молярная масса может быть вычислена различными способами. Один из них - использование периодической системы элементов, где указаны атомные массы каждого элемента. Другой способ - использование экспериментальных данных, таких как удельная теплоемкость или плотность вещества, которые позволяют вычислить молярную массу с помощью соответствующих формул и законов.
Что такое удельная теплоемкость?
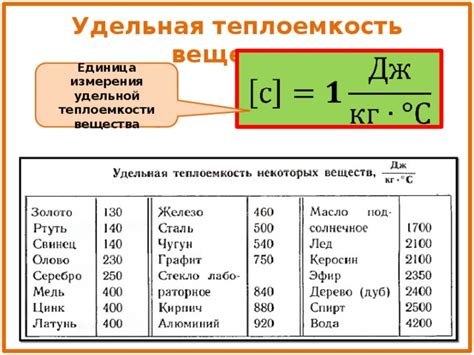
Удельная теплоемкость - это величина, которая характеризует количество теплоты, необходимое для нагревания единицы вещества на один градус по шкале температур. Она является важной характеристикой вещества и позволяет определить его способность поглощать и отдавать тепло.
Удельная теплоемкость обычно выражается в джоулях на грамм или в калориях на грамм на градус Цельсия. Отличается от удельной теплоемкости обычного теплоемкостью, которая выражается в джоулях на моль или в калориях на моль на градус Цельсия.
Значение удельной теплоемкости зависит от типа вещества, его состояния (твердое, жидкое, газообразное) и температуры. Например, удельная теплоемкость воды при константном давлении равна 4,18 дж/г°C, а удельная теплоемкость железа - примерно 0,46 дж/г°C.
Зная удельную теплоемкость вещества, можно вычислить его молярную массу, если известно количество вещества и количество поглощенной или отданной теплоты. Для этого можно использовать формулу Q = m * c * ΔT, где Q - поглощенная или отданная теплота, m - масса вещества, c - удельная теплоемкость, ΔT - изменение температуры.
Какие факторы влияют на удельную теплоемкость?
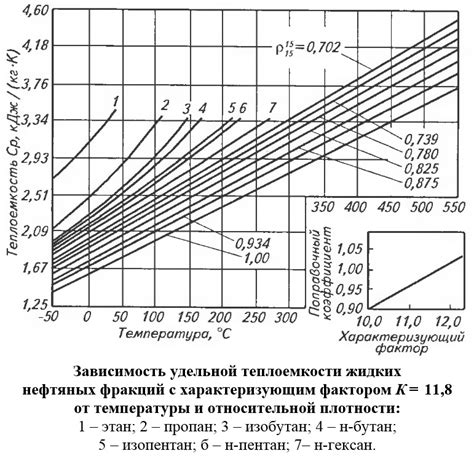
Удельная теплоемкость вещества зависит от ряда факторов, которые могут варьироваться в разных случаях. Одним из таких факторов является химический состав материала. Каждый элемент имеет свою характеристику удельной теплоемкости, и соответственно, при смешении разных элементов вещества, их удельные теплоемкости влияют на общую удельную теплоемкость.
Также удельная теплоемкость зависит от фазы агрегатного состояния вещества. Например, удельная теплоемкость жидкости обычно выше, чем удельная теплоемкость твердого материала того же вещества.
Температура является еще одним фактором, оказывающим влияние на удельную теплоемкость. В некоторых случаях удельная теплоемкость может зависеть от температуры и изменяться в зависимости от того, в каком диапазоне температур мы рассматриваем.
Структура и состояние вещества, такие как кристаллическая решетка или аморфность, также могут влиять на удельную теплоемкость. Например, кристаллический материал может обладать большей удельной теплоемкостью, чем его аморфный аналог.
Один из основных факторов, влияющих на удельную теплоемкость, - это наличие примесей или легирование вещества. Добавление примесей или сплавных элементов может изменить удельную теплоемкость и повлиять на его химическую стабильность.
Что такое молярная теплоемкость?

Молярная теплоемкость - это физическая величина, которая характеризует количество теплоты, необходимое для нагревания одного моля вещества на один градус Цельсия. Она обозначается как Cm и измеряется в джоулях на моль и градус Цельсия (Дж/(моль·К)).
Молярная теплоемкость является интенсивной физической величиной, которая не зависит от количества вещества и остается постоянной в определенных условиях, таких как температура и давление. Концепция молярной теплоемкости основывается на предположении, что вещество ведет себя как идеальный газ.
Молярная теплоемкость может быть измерена экспериментально с помощью калориметрии, где измеряются изменения температуры вещества при подводе или отводе теплоты. Значение молярной теплоемкости может зависеть от состояния вещества, например, при переходе между фазами (плавление, испарение) или при химических реакциях.
На практике значения молярной теплоемкости широко используются для расчетов тепловых эффектов химических реакций, определения энергии связи и других физических параметров системы. Она также имеет большое значение в термодинамике и обладает важным теоретическим и практическим значением в различных областях науки и промышленности.
Как связана молярная теплоемкость с удельной?

Удельная теплоемкость – это количество теплоты, которое необходимо передать единице массы вещества для его нагрева на единичную разность температур. Она является важным показателем для определения теплофизических свойств различных материалов. Молярная теплоемкость же представляет собой количество теплоты, которое нужно сообщить одному молярному количеству вещества для его нагрева на 1 К.
Молярная теплоемкость является функцией удельной теплоемкости и молярной массы вещества. Математически связь между ними выражается следующим образом: Cm = cp * M, где Cm – молярная теплоемкость, cp – удельная теплоемкость, M – молярная масса.
Таким образом, чтобы вычислить молярную теплоемкость вещества, необходимо знать его удельную теплоемкость и молярную массу. Эти параметры позволяют определить, сколько теплоты потребуется для нагрева определенного количества вещества на единичную разность температур.
Знание молярной теплоемкости позволяет провести более точные расчеты и прогнозировать тепловые процессы в веществе. Это особенно важно при выполнении термических расчетов и проектировании различных устройств и систем, где учет теплообмена играет важную роль.
Как вычислить молярную массу металла?
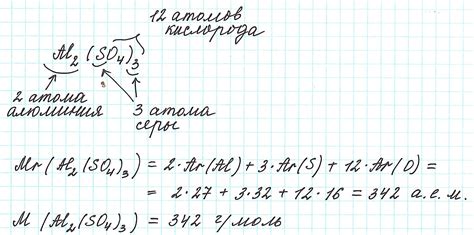
Молярная масса металла является важным параметром, который определяет массу одного моля вещества. Это величина, измеряемая в граммах на моль (г/моль) и помогает в определении количества вещества в химических реакциях.
Для вычисления молярной массы металла по удельной теплоемкости, необходимо знать удельную теплоемкость металла (верхний индекс c), его молярную массу (выражаемую в единицах г/моль) и химическую формулу металла.
Шаги вычисления молярной массы металла следующие:
- Найти удельную теплоемкость металла c, используя литературные данные или экспериментальные измерения.
- Определить количество теплоты Q, поглощенной металлом при нагревании.
- Используя формулу q = mcΔT, где q - количество теплоты, m - масса вещества, c - удельная теплоемкость, ΔT - изменение температуры, выразить массу металла.
- Выразить количество вещества N, используя формулу N = m/M, где N - количество вещества, m - масса вещества, M - молярная масса.
- Выразить молярную массу М, используя формулу М = m/N, где М - молярная масса, m - масса вещества, N - количество вещества.
Вычисление молярной массы металла позволяет определить его структуру, свойства и использовать эти данные в различных химических расчетах. Такой подход широко применяется в области материаловедения, металлургии и других науках.
Какие данные нужны для расчета?

Для расчета молярной массы металла по удельной теплоемкости необходимо иметь следующие данные:
- Удельная теплоемкость металла: это физическая величина, которая указывает, сколько теплоты нужно для нагревания единицы массы металла на один градус Цельсия.
- Молярная теплоемкость: это энергия, которую нужно сообщить системе для изменения температуры молярного количества вещества на один градус Цельсия.
- Масса металла: это количество вещества металла, измеряемое в граммах или килограммах.
- Температурные данные: исходные и конечные значения температуры металла для расчета изменения его температуры.
С помощью этих данных можно использовать формулу молярной теплоемкости, чтобы вычислить молярную массу металла.
Пример формулы для расчета молярной массы металла по удельной теплоемкости:
cp = M * Cm
где:
- cp - молярная теплоемкость
- M - молярная масса металла
- Cm - удельная теплоемкость металла
Следуя этой формуле, можно подставить известные значения удельной теплоемкости и молярной теплоемкости, а затем решить уравнение относительно молярной массы металла (M).
Какой формулой вычислить молярную массу?

Молярная масса (M) — это масса одного моля вещества, выраженная в граммах. Однако молярная масса не всегда известна напрямую, и иногда необходимо вычислить ее по другим известным величинам.
Одной из основных формул для вычисления молярной массы является газовая формула, которая устанавливает прямую пропорциональность между молярной массой и удельной теплоемкостью газа при постоянном объеме:
M = Cv * R
где M - молярная масса, Cv - удельная теплоемкость газа, R - универсальная газовая постоянная.
Для вычисления молярной массы металла по удельной теплоемкости необходимо знать удельную теплоемкость металла и значение универсальной газовой постоянной.
Важно отметить, что формула для вычисления молярной массы может различаться в зависимости от конкретных условий и свойств вещества. Поэтому перед использованием формулы необходимо убедиться в ее применимости к конкретному случаю и учитывать все факторы, влияющие на данное вычисление.
Пример вычисления молярной массы металла

Для вычисления молярной массы металла по удельной теплоемкости можно использовать формулы и данные из известных источников. Например, давайте представим, что у нас есть металлический образец, масса которого известна, а также есть информация об его удельной теплоемкости.
Для начала необходимо измерить массу образца металла с помощью точных весов. Допустим, мы имеем образец металла массой 10 г.
Затем нам необходимо узнать удельную теплоемкость этого металла. Удельная теплоемкость - это количество теплоты, необходимое для нагревания единицы массы данного вещества на один градус Цельсия. Предположим, что у нас есть данные, что удельная теплоемкость данного металла составляет 0,385 Дж/г·°C.
Для вычисления молярной массы металла по удельной теплоемкости необходимо воспользоваться следующей формулой:
Молярная масса металла = Масса металла / (Удельная теплоемкость * 1000)
В нашем случае:
- Масса металла = 10 г
- Удельная теплоемкость = 0,385 Дж/г·°C
Подставляя эти значения в формулу, получаем:
Молярная масса металла = 10 г / (0,385 Дж/г·°C * 1000) = 26,0 г/моль
Таким образом, в данном примере молярная масса металла составляет 26,0 г/моль.
Вопрос-ответ

Как вычислить молярную массу металла по удельной теплоемкости?
Для вычисления молярной массы металла по удельной теплоемкости необходимо знать формулу вещества, соотношение атомных масс элементов в формуле и удельную теплоемкость этого вещества. Формула для вычисления молярной массы металла выглядит следующим образом: M = C * 12.01 / Cp. Здесь M - молярная масса металла, C - удельная теплоемкость вещества, 12.01 - атомная масса углерода, а Cp - удельная теплоемкость углерода. Простым подстановкой значений в эту формулу можно вычислить молярную массу металла.
Какие данные необходимы для вычисления молярной массы металла по удельной теплоемкости?
Для вычисления молярной массы металла по удельной теплоемкости необходимо знать формулу вещества и соотношение атомных масс элементов в этой формуле. Также необходимо знать удельную теплоемкость этого вещества и атомную массу углерода. С этими данными можно воспользоваться формулой M = C * 12.01 / Cp, где M - молярная масса металла, C - удельная теплоемкость вещества, 12.01 - атомная масса углерода, а Cp - удельная теплоемкость углерода. Подставив известные значения в эту формулу, можно получить значение молярной массы металла.
