Кислоты и основания являются важными химическими соединениями, которые играют важную роль в различных процессах. Одним из наиболее интересных и важных аспектов химии является изучение реакций, происходящих между кислотами и металлами или основаниями.
Реакции кислот с металлами широко представлены в природе и синтезе. Одной из наиболее известных реакций является реакция соляной кислоты с металлами, например, цинком или железом. В результате таких реакций образуются соли и выделяется водород. Это объясняется тем, что кислоты отдают водородные ионы, а металлы оказываются достаточно активными, чтобы заменить водород в молекуле кислоты.
Основания также могут реагировать с металлами, образуя соли и выделяя водород, подобно кислотам. Реакция щелочи с металлами, такими как натрий или калий, является одним из ярких примеров.
Основания отдают гидроксильные ионы, которые реагируют с активной поверхностью металла, вызывая его разрушение и образование соли.
Реакции между кислотами и металлами или основаниями имеют огромное значение в промышленности и обычной жизни. Они используются в процессе получения различных соединений, а также широко применяются в химическом анализе и качественном определении веществ.
Реакция кислот с металлами

Кислоты – это химические соединения, обладающие кислотными свойствами и способные отдавать положительные ионы в водном растворе. Кислоты взаимодействуют с различными веществами, включая металлы. Реакция кислот с металлами является одной из наиболее распространенных и известных.
При взаимодействии кислоты с металлом происходит образование соли и выделение водорода. Образование соли связано с замещением положительных ионов металла на ионы водорода в кислоте. В зависимости от активности металла и его растворимости в кислоте, скорость реакции и характер продуктов может различаться.
Наиболее активные металлы, такие как натрий, калий и литий, реагируют с кислотами с выделением большого количества водорода и образованием солей. Например, при реакции натрия с серной кислотой образуется серная соль и выделяется водородный газ.
Менее активные металлы, такие как железо и цинк, могут реагировать с некоторыми кислотами, но реакция происходит медленнее и выделение водорода – менее интенсивное. Например, железо образует соль и выделяет водород при реакции с уксусной кислотой.
Однако не все металлы реагируют с кислотами. Некоторые металлы, такие как золото и платина, стабильны и не вступают в реакцию с кислотами. Это связано с их низкой активностью и химической инертностью.
Реакция кислот с металлами имеет большое практическое значение. Например, она используется для получения солей и водорода, а также в химическом анализе для выявления наличия и характера металлов в различных образцах.
Взаимодействие металлов с кислотами: химический процесс

Взаимодействие металлов с кислотами – это химический процесс, при котором образуются соли и выделяется водород. Оно основано на реакции обмена, где металл замещает водород в кислоте.
Этот процесс протекает в результате присутствия свободных металлических ионов, которые активно реагируют с отрицательными ионами кислоты. Такая реакция не происходит со всеми металлами, а зависит от их активности.
Например, агрессивные кислоты, такие как соляная (HCl) или серная (H2SO4), могут реагировать с такими металлами, как железо (Fe), цинк (Zn), алюминий (Al) и многими другими. При этом образующийся водород может проявляться в виде пузырьков или просто выделяться газом.
Взаимодействие металлов с кислотами можно использовать в различных приложениях, например, для очистки поверхностей от ржавчины или при производстве водорода. Также важно помнить о безопасности, так как некоторые реакции могут быть очень бурными или даже опасными. Поэтому необходимо соблюдать меры предосторожности и работать с кислотами и металлами в специальных условиях.
Химические реакции кислот с различными металлами

Химические реакции кислот с металлами определяются химическими свойствами как металлов, так и кислот. Металлы могут быть активными или пассивными, а кислоты могут быть сильными или слабыми. Взаимодействие между ними зависит от степени активности металлов и их способности образовывать ионы.
Сильные кислоты, такие как серная кислота и хлороводородная кислота, сильно реагируют с активными металлами, такими как натрий, калий и железо. В результате этих реакций образуется соль металла и вода. Например, реакция между серной кислотой и натрием выглядит следующим образом:
H2SO4 + 2Na → Na2SO4 + H2
Слабые кислоты, такие как уксусная кислота, не реагируют с пассивными металлами, такими как алюминий и медь. Однако, они могут реагировать с некоторыми активными металлами, например, с цинком. При этом образуется соль металла и вода. Например, реакция между уксусной кислотой и цинком выглядит следующим образом:
CH3COOH + Zn → Zn(CH3COO)2 + H2
Некоторые кислоты, такие как соляная кислота и азотная кислота, могут реагировать с различными металлами. Однако, реакция может проходить по-разному в зависимости от металла. Например, реакция между соляной кислотой и цинком выглядит следующим образом:
HCl + Zn → ZnCl2 + H2
Взаимодействия кислот с металлами представляют собой важные химические реакции, которые находят широкое применение в различных областях, включая промышленность, медицину и научные исследования.
Реакция кислот с основаниями

Реакция кислот с основаниями представляет собой химическую реакцию, при которой ионы водорода из кислоты обмениваются на ионы металла или ионы OH- из основания. Результатом такой реакции является образование соли и воды.
Реакция между кислотами и основаниями осуществляется по принципу нейтрализации, при которой ионы H+ из кислоты соединяются с ионами OH- из основания, образуя молекулы воды. При этом ионы металла или ион OH- из основания образуют соль, которая растворяется в воде.
Примером реакции кислоты с основанием является реакция между соляной кислотой (HCl) и гидроксидом натрия (NaOH). При взаимодействии этих веществ образуется соль - хлорид натрия (NaCl) и вода (H2O).
Уравнение реакции выглядит следующим образом:
| HCl + NaOH | → | NaCl + H2O |
Таким образом, реакция кислот с основаниями играет важную роль в химии, позволяя получать соли и воду, а также проводить нейтрализацию кислотных и щелочных сред.
Взаимодействие кислот с основаниями: особенности и химическая реакция

Взаимодействие кислот с основаниями – важный процесс в химии, который приводит к образованию соли и воды. Основания являются химическими соединениями, которые обладают способностью принимать протоны от кислот. Этот процесс называется нейтрализацией. В результате химической реакции между кислотой и основанием образуется соль, которая состоит из положительного и отрицательного ионов.
Примером взаимодействия кислоты с основанием является реакция соляной кислоты (HCl) с гидроксидом натрия (NaOH). При смешении этих веществ образуется натриевая соль (NaCl) и вода (H2O). Химическое уравнение реакции выглядит следующим образом: HCl + NaOH → NaCl + H2O.
Важно отметить, что реакция между кислотой и основанием имеет экзотермический характер, то есть сопровождается выделением тепла. Это можно наблюдать, когда основание или кислота добавляются в раствор друг друга. Возникающая реакция может быть более или менее интенсивной в зависимости от концентрации и свойств веществ.
Также стоит упомянуть, что взаимодействие кислот с основаниями играет большую роль в нашей повседневной жизни. Мы часто используем продукты, полученные в результате подобных реакций, такие как моющие средства и лекарственные препараты. Например, аспирин – распространенное лекарство для снятия боли и жара – является солью, полученной в результате реакции салициловой кислоты с натрием.
Примеры реакций кислот с различными основаниями

1. Реакция кислоты с гидроксидами:
Когда кислота реагирует с гидроксидом, происходит нейтрализационная реакция, при которой образуется соль и вода. Например, реакция между соляной кислотой (HCl) и гидроксидом натрия (NaOH) приведет к образованию соли натрия (NaCl) и воды (H2O).
2. Реакция кислоты с оксидами:
Реакция кислоты с оксидом приводит к образованию соли и воды. Например, реакция между серной кислотой (H2SO4) и оксидом меди (II) (CuO) приведет к образованию сульфата меди (II) (CuSO4) и воды (H2O).
3. Реакция кислоты с гидридами:
Реакция кислоты с гидридом металла приводит к образованию соли и водорода. Например, реакция между соляной кислотой (HCl) и гидридом алюминия (AlH3) приведет к образованию хлорида алюминия (AlCl3) и водорода (H2).
4. Реакция кислоты с основными оксидами:
Когда кислота реагирует с основным оксидом, образуется соль и вода. Например, реакция между серной кислотой (H2SO4) и оксидом кальция (CaO) приведет к образованию сульфата кальция (CaSO4) и воды (H2O).
5. Реакция кислоты с основными гидроксидами:
Реакция между кислотой и основным гидроксидом приводит к образованию соли и воды. Например, реакция между соляной кислотой (HCl) и гидроксидом бария (Ba(OH)2) приведет к образованию хлорида бария (BaCl2) и воды (H2O).
6. Реакция кислоты с основными солями:
Когда кислота реагирует с основной солью, происходит реакция нейтрализации, при которой образуется вода и соли. Например, реакция между уксусной кислотой (CH3COOH) и ацетатом натрия (CH3COONa) приведет к образованию уксуснокислого натрия (CH3COONa) и воды (H2O).
Особенности реакции кислот с металлами и основаниями
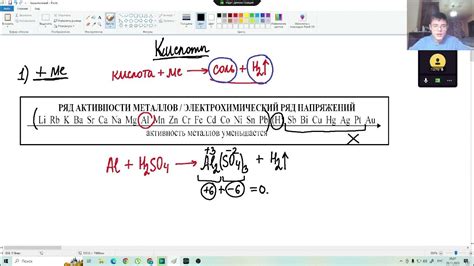
Реакция кислот с металлами является одной из основных химических реакций, которая происходит при взаимодействии кислоты с металлическими элементами. При этом образуется соль и выделяется водород. Реакцию кислот с металлами можно описать следующим образом: HCl + Zn = ZnCl2 + H2.
Одной из особенностей реакции является выделение водорода. В случае реакции с металлами, которые имеют положительный потенциал восстановления, такими как цинк или алюминий, реакция происходит с выделением газа. Выделение водорода можно пронаблюдать при взаимодействии с кислотами на практике, например, при реакции кислоты с цинком в присутствии индикатора.
Реакция кислот с основаниями также представляет собой одно из наиболее распространенных химических взаимодействий. При взаимодействии кислоты с щелочью или основанием происходит образование соли и воды. Реакция можно записать следующим образом: HCl + NaOH = NaCl + H2O.
Одной из особенностей реакции кислот с основаниями является нейтрализация. Кислота, содержащая в своем составе ион водорода, при взаимодействии с основанием забирает его, образуя воду. В результате образуется соль, которая обладает различными свойствами, в зависимости от состава кислоты и основания.
Итак, реакция кислот с металлами и основаниями имеет свои особенности. При взаимодействии с металлами происходит выделение водорода, а при реакции с основаниями – нейтрализация и образование соли. Изучение этих реакций позволяет лучше понять принципы химических процессов и их воздействие на окружающую среду.
Вопрос-ответ

Какие продукты образуются при реакции кислот с металлами?
При реакции кислот с металлами образуются соли и водород. Например, соляная кислота (HCl) при взаимодействии с цинком (Zn) образует хлорид цинка (ZnCl2) и молекулярный водород (H2).
Как происходит реакция кислот с основаниями?
Реакция кислот с основаниями, или нейтрализационная реакция, приводит к образованию соли и воды. Например, реакция соляной кислоты (HCl) с гидроксидом натрия (NaOH) дает хлорид натрия (NaCl) и воду (H2O).
Какие особенности есть у реакции кислот с металлами?
Одной из особенностей реакции кислот с металлами является выделение водорода. При этом реакция протекает более интенсивно с активными металлами, такими как цинк (Zn), железо (Fe) или алюминий (Al). Кроме того, некоторые металлы могут реагировать с кислотами только при нагревании.
