Металлы – это группа элементов периодической таблицы, обладающих такими свойствами, как высокая теплопроводность, электропроводность, пластичность, и твердость. Однако, не все металлы обладают одинаковыми свойствами. В периодической таблице элементы расположены в порядке возрастания атомного номера, а также в соответствии с их химическими свойствами. Это позволяет установить закономерности и выявить изменение свойств металлов по группе сверху вниз.
Первая группа металлов - щелочные металлы, включает такие элементы, как литий, натрий, калий и другие. Они обладают высокой реактивностью и образуют ионы с положительным зарядом легко, что объясняется низкой энергией ионизации. В связи с этим, они активно взаимодействуют с водой и воздухом, превращаясь в гидроксиды и оксиды соответственно. Щелочные металлы характеризуются низкой плотностью, низким температурным плавлением и мягкостью. Они также обладают высокой электропроводностью и используются в различных сферах, включая производство батарей, легирование стали и многое другое.
Следующая группа металлов - щелочноземельные металлы. Она включает элементы, такие как магний, кальций и барий. Эти металлы также обладают высокой реактивностью, однако, они менее реактивны, чем щелочные металлы. У них выше энергия ионизации, поэтому они менее склонны образовывать ионы с положительным зарядом. Щелочноземельные металлы имеют большую плотность и более высокое температурное плавление, чем щелочные металлы. Они также обладают высокой теплопроводностью и используются в металлургической промышленности, в производстве сплавов и других приложениях.
По мере движения по периодической таблице, схема меняется. В целом, металлы внизу группы становятся менее реактивными и менее легкоплавкими. Это связано с увеличением энергии ионизации и размеров атомов. Более тяжелые металлы обладают более высокой плотностью и твердостью, а также могут образовывать более сложные соединения и сплавы. Они также могут иметь более высокую теплопроводность и устойчивость к окислению. Примерами таких металлов являются железо, медь, свинец, золото и многие другие.
Как изменяются свойства металлов по группе сверху вниз
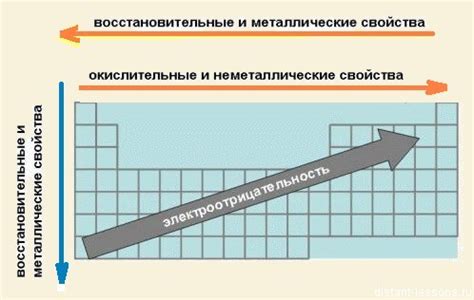
Металлы, расположенные по группе сверху вниз в периодической системе, обладают различными свойствами, которые меняются в зависимости от их положения.
Первым фактором, который влияет на свойства металлов, является размер атома. По мере движения вниз по группе, атомы металлов становятся больше. Большие атомы имеют более слабое притяжение электронов к ядру, что приводит к более слабым межатомным связям. В результате, металлы внизу группы становятся мягче, что проявляется в их свойствах, таких как пластичность и хрупкость.
Еще одной характеристикой металлов, изменяющейся по группе сверху вниз, является электроотрицательность. Электроотрицательность - это способность атомов привлекать электроны к себе. Чем меньше электроотрицательность атома, тем он легче отдает электроны и образует положительные ионы. Следовательно, металлы внизу группы имеют более низкую электроотрицательность и более тенденцию образовывать положительные ионы.
Кроме того, свойства металлов также изменяются по группе сверху вниз в отношении их реактивности. Металлы в верхней части группы обычно более реактивны, так как они имеют более слабую металлическую связь и более легко отдают электроны. В то время как металлы в нижней части группы обычно менее реактивны, поскольку их более сильная металлическая связь удерживает электроны более прочно.
В целом, изменение свойств металлов по группе сверху вниз связано с изменением размера атома, электроотрицательности и реактивности. Понимание этих изменений помогает в изучении и использовании различных свойств металлов в различных отраслях промышленности и научных исследованиях.
Свойства металлов в верхней группе
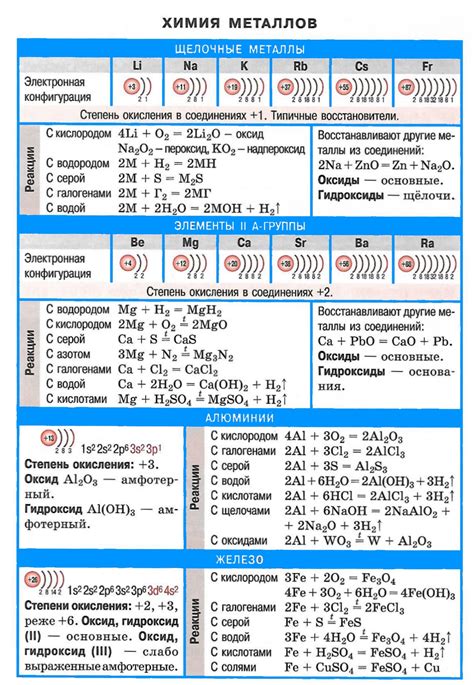
Металлы в верхней группе периодической системы элементов обладают рядом особенных свойств, которые отличают их от других металлов. Вместе с тем, каждый металл в этой группе имеет свои уникальные характеристики.
1. Литий (Li) – самый легкий из всех металлов. Он обладает низкой плотностью и высокой электрической проводимостью. Литий является очень реактивным металлом, легко сочетается с кислородом и образует стабильные соединения.
2. Бериллий (Be) – металл с высокой температурой плавления и крайне жесткий. Бериллий обладает отличной теплопроводностью и является прекрасным проводником электричества. Однако, он токсичен и может вызывать серьезные заболевания при вдыхании его пыли.
3. Натрий (Na) – характеризуется высокой реактивностью и хорошей проводимостью электричества. Натрий образует стабильные соединения с другими элементами, такими как кислород и хлор. Более того, он является основным компонентом домашней пищи – кулинария без натрия не представляется возможной.
4. Магний (Mg) – металл средней плотности, обладающий высокой химической стойкостью. Магний находит широкое применение в промышленности благодаря своим антикоррозионным свойствам. Он также необходим для нормального функционирования организма человека, так как входит в состав многочисленных ферментов и коферментов.
5. Алюминий (Al) – легкий, прочный и хорошо проводящий тепло и электричество металл. Алюминий является самым распространенным металлом на Земле и широко используется в различных отраслях промышленности, строительстве и производстве. Он также является незаменимым элементом в питании человека и играет важную роль в нормализации уровня гормонов и запуске белкового синтеза.
Свойства металлов в центре группы
Металлы, расположенные в центре группы таблицы периодов, обладают интересными свойствами, которые отличают их от металлов на краю группы. Один из таких металлов – медь. Она характеризуется высокой электропроводностью и теплопроводностью, что делает ее востребованной в различных отраслях промышленности, включая электротехнику и строительство.
Медь также имеет высокую пластичность и формоизменяемость, что делает ее прекрасным материалом для производства проводов и кабелей. Благодаря своим уникальным свойствам медь используется в производстве электронных устройств, солнечных батарей и других технологических продуктов. Ее сплавы широко применяются в ювелирном искусстве, создавая прочные и красивые украшения.
Еще одним металлом из центральной части группы является цинк. Он обладает высокой коррозионной стойкостью и используется для окрашивания металлических изделий, а также в производстве защитных покрытий. Цинк также является важным микроэлементом для растений и животных, необходимым для нормального функционирования их организмов.
Цинк, в сочетании с другими металлами, образует сплавы, которые обладают повышенной прочностью и устойчивостью к повреждениям. Эти сплавы широко применяются в авиационной и автомобильной промышленности, а также в производстве строительных материалов. Свойства металлов из центральной части группы делают их важными компонентами в различных областях промышленности и науки.
Свойства металлов в нижней группе

Металлы в нижней группе периодической таблицы обладают определенными свойствами, отличающимися от свойств металлов в верхних группах.
Одно из основных свойств металлов в нижней группе - увеличение активности. Уже на примере первого элемента данной группы - ртути - можно увидеть, что она активнее и реактивнее, чем металлы в верхних группах. Это связано с более слабым удержанием электронов в атоме и, соответственно, большей восприимчивостью к взаимодействию с другими веществами.
Еще одним характерным свойством металлов нижней группы является понижение температуры плавления. Это связано с постепенным увеличением размеров атомов и более слабой силой взаимодействия между ними. Например, в нижней группе находится свинец, у которого низкая температура плавления, что позволяет легко переходить в жидкое состояние при относительно низких температурах.
Другим важным свойством металлов нижней группы является увеличение плотности. Благодаря увеличению размеров атомов, металлы данной группы имеют большую массу и занимают меньший объем. Например, золото, которое является металлом нижней группы, имеет высокую плотность, что делает его одним из самых тяжелых металлов.
Вопрос-ответ

Какие свойства металлов изменяются по группе сверху вниз?
Свойства металлов, меняющиеся по группе сверху вниз, включают точку плавления, плотность, радиус атомов, межатомное расстояние, электроотрицательность, электропроводность и химическую активность. В общем, металлы становятся более твердыми, плотными, менее электропроводными и менее активными химически по мере движения от верхних групп к нижним.
Какие причины лежат в основе изменения свойств металлов по группе?
Изменение свойств металлов по группе связано с изменением электронной структуры и внутренней структуры атомов при увеличении атомного номера. Увеличение атомного радиуса и количество энергии уровней определяют электронную структуру, которая влияет на свойства металлов. Количество валентных электронов и способность к образованию ионов также изменяются в зависимости от положения металла в периодической системе.

