Восстановительные свойства атомов металлов являются одной из важных характеристик этих веществ. Они определяют способность металлов принимать участие в химических реакциях, особенно в реакциях окисления и восстановления. Изменение этих свойств может происходить из-за различных механизмов, которые зависят от особенностей атомной структуры металлов и их взаимодействия с другими веществами.
Одним из основных механизмов изменения восстановительных свойств атомов металлов является изменение их электронной структуры. Атомы металлов в основном состоят из положительно заряженного ядра и свободных электронов. Изменение числа свободных электронов может привести к изменению их способности принимать или отдавать электроны при реакциях.
Кроме того, изменение восстановительных свойств атомов металлов может происходить из-за изменений в их структуре. Например, металлы могут образовывать сплавы с другими металлами или не металлами, что приводит к изменению их атомной структуры и свойств. Также, изменение условий окружающей среды, таких как температура и давление, может вызывать изменение восстановительных свойств атомов металлов.
Изменение восстановительных свойств атомов металлов имеет важное значение в различных областях науки и промышленности. На базе этих свойств разрабатываются новые материалы с улучшенными характеристиками, а также различные методы обработки и синтеза веществ. Изучение основных механизмов изменения восстановительных свойств металлов позволяет создать более эффективные и экологически безопасные процессы производства и использования металлических материалов.
Восстановительные свойства атомов металлов

Металлы обладают особыми свойствами, связанными с их способностью вступать в реакции окисления и восстановления. Восстановительные свойства атомов металлов определяют их способность отдавать электроны при взаимодействии с другими веществами.
Механизмы изменения восстановительных свойств атомов металлов связаны с изменением их электронной структуры. Восстановление металлов может происходить путем отдачи электронов из своей внешней оболочки, при этом они переходят в более низкую энергетическую оболочку. Этот процесс осуществляется за счет образования ионов металла с положительным зарядом.
Одной из основных причин изменения восстановительных свойств атомов металлов является различие в электроуровне валентных электронов. Если валентные электроны находятся на верхнем уровне энергии, то они легче отдаются во время реакции восстановления. Это связано с меньшей силой притяжения ядра к таким электронам.
Кроме того, влияние на восстановительные свойства атомов металлов оказывает их радиус. Чем больше радиус атома металла, тем легче электроны отдаются при взаимодействии с окислителями. Это связано с увеличением расстояния между ядром атома и его внешней оболочкой, что уменьшает силу притяжения ядра к валентным электронам.
Таким образом, изменение восстановительных свойств атомов металлов определяется их электронной структурой, электроуровнем валентных электронов и радиусом атомов металлов.
Процессы восстановления

Восстановление – это процесс, который возвращает атомы металлов к их исходному состоянию после оказания воздействия внешних факторов, таких как экстремальные условия окружающей среды или механические повреждения. Основным механизмом восстановления является передача электронов между атомами, что позволяет корректировать их энергетическое состояние.
Одним из основных процессов восстановления является катодная реакция, при которой атомы металлов получают электроны и уменьшают свою положительную заряду. Это происходит в результате редокс-реакции, где электроны передаются от атомов, имеющих более низкую электроотрицательность, к атомам с более высокой электроотрицательностью.
Еще одним важным процессом восстановления является термическое восстановление. При нагревании атомы металлов получают энергию, способствующую их перемещению и восстановлению. По мере повышения температуры происходит увеличение скорости молекулярных движений, что способствует восстановительным реакциям.
Восстановительные процессы в металлах могут происходить как внутрикристаллически, так и межкристаллически. Внутрикристаллическое восстановление представляет собой процесс восстановления атомов внутри кристаллической решетки. Межкристаллическое восстановление происходит на границах раздела различных кристаллов или фаз, где возможно более легкое перемещение атомов.
Восстановление в химических реакциях

Восстановление является одной из основных химических реакций, которая происходит между веществами и включает передачу электронов. Оно происходит при участии вещества, которое называется восстановителем, и вещества, которое называется окислителем.
Восстановление может протекать различными способами. Одним из наиболее распространенных механизмов восстановления является передача электронов от восстановителя к окислителю. В данном случае восстановитель теряет электроны, а окислитель приобретает их.
Еще одним механизмом восстановления является присоединение водорода или других атомов к веществу, которое должно быть восстановлено. В этом случае вещество принимает дополнительные атомы и становится восстановленным.
Восстановление может проходить как в кислой, так и в щелочной среде. В кислой среде восстановление происходит в присутствии воды и протонов, а в щелочной среде – в присутствии гидроксидных ионов.
Восстановление имеет широкое применение в различных областях науки и промышленности. Например, восстановительные свойства атомов металлов используются для получения металлических соединений, производства электроники, обработки поверхностей и многих других целей.
Изучение восстановительных свойств атомов металлов и механизмов восстановления в химических реакциях имеет важное значение для понимания реакционной способности веществ и разработки новых методов синтеза и технологий.
Значение восстановительных свойств

Восстановительные свойства атомов металлов играют важную роль в различных процессах и явлениях, связанных с химическими реакциями и электрохимией. Восстановление – это процесс передачи электронов или электронных пар, при котором атом или ион восстанавливают свою окислительность.
Первоначально, восстановительные свойства атомов металлов определяют их активность в химических реакциях. Активные металлы обладают высокой электроотрицательностью и способностью легко отдавать электроны, что делает их хорошими восстановителями.
Кроме того, восстановительные свойства металлических атомов определяют их способность функционировать как электроды в электрохимических процессах. Металлы, обладающие большей восстановительной активностью, могут быть использованы в качестве анодов в гальванических элементах или электролизерах.
Кроме того, восстановительные свойства металлических атомов также влияют на их способность образовывать соединения с различными элементами. Например, металлы с более высокой восстановительной активностью способны образовывать межметаллические соединения с металлами менее активными.
Также, восстановительные свойства металлов имеют практическое значение в различных отраслях промышленности. Например, металлы с высокой восстановительной активностью используются в процессах по обработке поверхностей и покрытию металлических изделий для защиты от коррозии.
Изменение восстановительных свойств
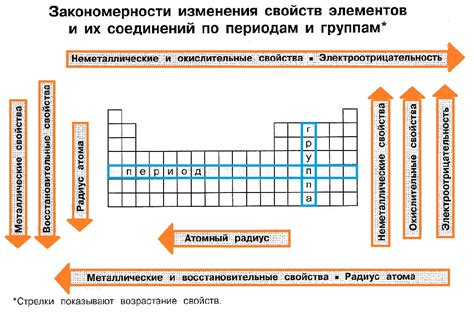
В процессе химических реакций атомы металлов могут изменять свои восстановительные свойства. Восстановительная способность атомов металлов определяет их способность передавать электроны другим веществам и превращать окислители в восстановители.
Изменение восстановительных свойств атомов металлов может происходить под воздействием различных факторов, таких как изменение окружающей среды, наличие катализаторов или повышение температуры. В результате таких изменений атомы металлов могут приобретать новые восстановительные свойства или терять их.
Одним из основных механизмов изменения восстановительных свойств атомов металлов является изменение их электронной структуры. Под действием внешних факторов, атомы металлов могут переходить из одного энергетического уровня на другой, что может приводить к изменению их восстановительных свойств.
Еще одним механизмом изменения восстановительных свойств атомов металлов является изменение их окислительно-восстановительного потенциала. Под воздействием внешних факторов, таких как изменение температуры или наличие катализаторов, окислительно-восстановительный потенциал атомов металлов может изменяться, что приводит к изменению их способности передавать электроны другим веществам.
Таким образом, изменение восстановительных свойств атомов металлов является важным процессом с точки зрения химических реакций. Понимание основных механизмов этих изменений позволяет предсказывать и контролировать восстановительные свойства атомов металлов и использовать их в различных областях, таких как катализ и производство электроэнергии.
Физические механизмы

Физические механизмы изменения восстановительных свойств атомов металлов обусловлены различными физическими процессами, которые происходят в материале при его воздействии на окружающую среду.
Одним из таких механизмов является диффузия, которая обусловлена тепловым движением атомов. При повышении температуры атомы металла получают дополнительную энергию, что позволяет им перемещаться с одного места на другое. В результате этого процесса атомы металла могут мигрировать и присоединяться к поверхности образующейся пленки оксида или другого вещества.
Еще одним физическим механизмом является адсорбция. В процессе адсорбции атомы металла привлекаются к поверхности другого вещества (например, кислорода) и взаимодействуют с ним, образуя слой оксида или другой химической соединительной пленки.
Кроме того, физические механизмы изменения восстановительных свойств атомов металлов могут быть связаны с фазовыми переходами. Например, при нагреве некоторых металлов происходит переход из ферромагнитной фазы в парамагнитную. В результате этого процесса могут изменяться магнитные свойства металла и его способность к окислительно-восстановительным реакциям.
В целом, физические механизмы изменения восстановительных свойств атомов металлов представляют собой сложный взаимосвязанный комплекс процессов, который в значительной степени определяет химическую и физическую стабильность металла в окружающей среде.
Химические механизмы
Изменение восстановительных свойств атомов металлов может происходить посредством химических механизмов, которые определяются способностью металлов образовывать соединения с другими веществами. В результате химической реакции между атомами металла и молекулами вещества происходят изменения во внутренней структуре атомов, что приводит к изменению их восстановительных свойств.
Одним из химических механизмов является окисление металла, когда атомы металла соединяются с кислородом из воздуха, в результате чего образуется оксид металла. Это приводит к изменению восстановительной способности металла, поскольку оксид металла не обладает такой активностью в химических реакциях, как непосредственно металл. Таким образом, окисление металла может ограничивать его возможности восстановления.
Другим химическим механизмом является образование комплексных соединений металла с другими веществами, например, с кислотами или основаниями. В результате таких химических реакций атомы металла образуют соединения с более сложной структурой, что изменяет их восстановительные свойства. Комплексные соединения могут обладать различной активностью в химических реакциях, поэтому восстановительные свойства металла могут зависеть от его способности образовывать комплексные соединения.
Также химические механизмы изменения восстановительных свойств атомов металлов могут быть связаны с взаимодействием с другими элементами, например, с хлором или серой. В результате образуются химические соединения, которые также могут ограничивать возможности восстановления металла.
Влияние внешних факторов

Восстановительные свойства атомов металлов могут изменяться под влиянием различных внешних факторов. Одним из таких факторов является температура окружающей среды. При повышении температуры атомы металлов обладают большей энергией и могут активнее участвовать в химических реакциях. Это может привести к увеличению их восстановительных свойств и повышению скорости реакции.
Другим фактором, влияющим на восстановительные свойства атомов металлов, является давление. Под действием высокого давления атомы металлов могут изменять свою структуру и становиться более активными в реакциях восстановления. В отсутствие давления атомы металлов могут быть более устойчивыми и меньше склонны к восстановлению.
Еще одним важным внешним фактором, влияющим на восстановительные свойства атомов металлов, является наличие катализаторов. Катализаторы могут повысить скорость процесса восстановления, обеспечивая альтернативный путь для химической реакции. Они могут образовывать комплексы с атомами металлов, что способствует ускорению процесса восстановления.
Таким образом, внешние факторы, такие как температура, давление и наличие катализаторов, играют важную роль в изменении восстановительных свойств атомов металлов. Понимание и контроль этих факторов могут быть полезными при разработке новых методов восстановления металлических материалов и применении их в различных отраслях промышленности.
Вопрос-ответ

Какие механизмы влияют на изменение восстановительных свойств атомов металлов?
Изменение восстановительных свойств атомов металлов может зависеть от нескольких механизмов, включая эффект температуры, образование дефектов решетки, взаимодействие с окружающей средой и примесями.
Как температура влияет на восстановительные свойства атомов металлов?
Повышение температуры может способствовать активации восстановительных свойств атомов металлов, поскольку это увеличивает их энергию и подвижность. Однако слишком высокие температуры могут привести к слиянию и сегрегации атомов, что может отрицательно повлиять на восстановительные свойства.
Как образование дефектов решетки влияет на восстановительные свойства атомов металлов?
Образование дефектов решетки, таких как примесные атомы, дислокации или вакансии, может существенно повлиять на восстановительные свойства атомов металлов. Эти дефекты могут изменять химическую активность атомов и влиять на их способность к восстановлению.
Как взаимодействие с окружающей средой влияет на восстановительные свойства атомов металлов?
Взаимодействие с окружающей средой может вызывать окисление атомов металлов, что может ухудшить их восстановительные свойства. Некоторые вещества в окружающей среде могут также создавать пассивные пленки на поверхности металла, что может уменьшить его активность восстановления.
Как примеси влияют на восстановительные свойства атомов металлов?
Примеси могут иметь как положительное, так и отрицательное влияние на восстановительные свойства атомов металлов. Некоторые примеси могут улучшать восстановительные свойства, например, ускоряя каталитические реакции, в то время как другие могут замедлять или даже препятствовать процессу восстановления.
