Электродный потенциал металла – это важный параметр, который определяет его химические и физические свойства в контакте с другими веществами. Основными причинами изменения электродного потенциала являются влияние окружающей среды и электрохимические процессы, происходящие на поверхности металла.
Одной из причин изменения электродного потенциала является влияние окружающей среды. Металл может находиться в контакте с различными веществами, которые оказывают влияние на его потенциал. Например, воздух содержит в себе влагу и кислород, которые могут вызывать окисление металла и изменение его потенциала. Также, наличие агрессивных сред, таких как растворы кислот или щелочей, может приводить к коррозии металла и изменению его потенциала.
Другой причиной изменения электродного потенциала являются электрохимические процессы, происходящие на поверхности металла. Когда металл находится в контакте с электролитом, например, в растворе солей, на его поверхности могут происходить окислительно-восстановительные реакции. Эти реакции могут изменять состояние поверхности металла и его потенциал. Также, на поверхности металла могут формироваться различные соединения или слои окиси, которые также влияют на его потенциал.
Изменение электродного потенциала металла – это сложный процесс, обусловленный влиянием окружающей среды и электрохимическими реакциями на поверхности металла. Понимание этих причин и факторов позволяет контролировать и предотвращать нежелательные изменения в электродном потенциале металла, что имеет большое значение в различных областях, таких как материаловедение, электрохимия и коррозиология.
Установление равновесия электродного потенциала

Равновесие электродного потенциала металла на поверхности зависит от множества факторов и причин. Одной из основных причин изменения электродного потенциала является окружающая среда и ее взаимодействие с поверхностью металла.
При контакте металла с окружающей средой происходит обмен электронами между металлом и окружающей средой. Этот процесс может приводить к переносу электрического заряда и, следовательно, к изменению электродного потенциала металла. Такой перенос заряда может быть вызван, например, растворением металла в окружающей среде или образованием оксидной пленки на поверхности металла.
Кроме того, геометрические особенности поверхности металла также играют важную роль в установлении равновесия электродного потенциала. Поверхность металла может содержать микронеровности, неровности, пленки и другие примеси, которые могут влиять на процесс взаимодействия с окружающей средой и, следовательно, на электродный потенциал.
Для установления равновесия электродного потенциала металла на его поверхности могут также играть роль электролитические реакции, влияние других металлов, температурные факторы и другие внешние условия. Все эти факторы взаимодействуют между собой и могут приводить к изменению электродного потенциала металла на его поверхности.
Химические реакции и их влияние на потенциал металла
Химические реакции играют значительную роль в изменении электродного потенциала металла. При взаимодействии металла с различными веществами происходят окислительно-восстановительные процессы, которые влияют на электрический заряд и электродный потенциал металла.
Одной из наиболее распространенных химических реакций, которая влияет на потенциал металла, является окисление. Металл может реагировать с кислородом из воздуха или с другими окислителями, образуя оксиды. Это приводит к изменению состояния электродной поверхности металла и снижению его потенциала.
Также химические реакции могут привести к образованию оснований или кислот, которые взаимодействуют с металлом и изменяют его электродный потенциал. Например, взаимодействие металла с кислотой может привести к образованию ионов водорода на его поверхности, что повышает его потенциал.
Кроме того, химические реакции могут вызвать изменение концентрации растворенных веществ на поверхности металла, что также влияет на его потенциал. Ионная оболочка металла может растворяться в реакции с раствором, что меняет состояние поверхности и электродный потенциал металла.
Таким образом, химические реакции играют существенную роль в изменении электродного потенциала металла. Различные окислительно-восстановительные процессы, образование оксидов, взаимодействие с кислотами и основаниями, а также изменение концентрации растворенных веществ на поверхности металла влияют на электрический заряд металла и его электродный потенциал.
Эффекты среды на электродный потенциал

Электродный потенциал металла может быть значительно изменен в зависимости от воздействия окружающей среды. Различные факторы, такие как растворитель, температура, pH-значение и наличие других химических веществ, могут оказывать влияние на электродный потенциал.
Один из основных эффектов среды на электродный потенциал металла - растворительный эффект. В растворителе могут присутствовать ионы, которые способны взаимодействовать с поверхностью металла и изменить его электродный потенциал. Например, в кислой среде ионы водорода могут накапливаться на поверхности металла и вызывать снижение его электродного потенциала.
Температура также оказывает влияние на электродный потенциал металла. При повышении температуры молекулы растворителя обычно получают больше энергии, что может способствовать активации электрохимических реакций на поверхности металла и, следовательно, изменению его электродного потенциала.
Другим важным фактором, который может влиять на электродный потенциал, является pH-значение среды. Различные ионы, содержащиеся в растворе, могут взаимодействовать с поверхностью металла и изменить его заряд. Это в свою очередь может привести к изменению электродного потенциала металла.
Кроме того, наличие других химических веществ в растворе также может оказывать влияние на электродный потенциал металла. Например, наличие активных ионов может способствовать ускоренной коррозии металла и, как результат, вызывать изменение его электродного потенциала.
В целом, эффекты среды на электродный потенциал металла весьма сложны и могут быть обусловлены совокупностью различных факторов. Поэтому, при проведении электрохимических исследований и рассмотрении вопросов связанных с коррозией, необходимо учитывать влияние окружающей среды на электродный потенциал металла.
Температурные изменения и их влияние на потенциал металла
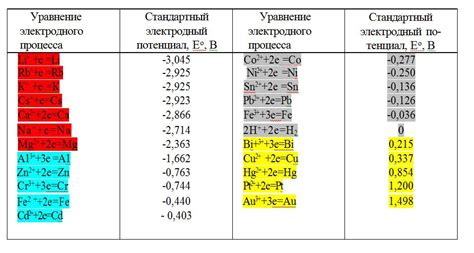
Температура является одним из важных факторов, влияющих на электродный потенциал металла. При изменении температуры, происходят изменения в структуре и свойствах металла, а также в его взаимодействии с окружающей средой. Все это сказывается на его электродном потенциале.
Увеличение температуры может привести к увеличению электродного потенциала металла. Это связано с увеличением энергии, необходимой для разделения ионов и электронов на электроде. При повышении температуры происходит активация электрохимических процессов, что может привести к более интенсивному и быстрому снижению потенциала металла.
Температурные изменения также влияют на реакцию процессов окисления и восстановления на металлической поверхности. При повышении температуры активность этих процессов может возрасти, что приведет к изменению электродного потенциала металла. Кроме того, изменения в структуре и сдвиг в равновесии электрохимических реакций также могут вызвать изменение потенциала металла при изменении температуры.
Однако важно отметить, что влияние температуры на электродный потенциал металла может быть нелинейным и зависит от конкретных условий и свойств металла. Поэтому для более точного определения влияния температуры на потенциал металла требуется проведение специальных экспериментов и исследований.
Механическое напряжение и его влияние на потенциал металла

Механическое напряжение может влиять на электродный потенциал металла. Когда металлическая конструкция подвергается механическим нагрузкам, изменения в ее структуре могут привести к изменению ее электродного потенциала. Это связано с тем, что механическое напряжение вызывает деформацию кристаллической решетки металла, которая влияет на распределение электронов внутри материала.
Когда металл подвергается растяжению, его электронная структура меняется, что приводит к изменению электродного потенциала. В результате растяжения электроны смещаются ближе к поверхности металла, что снижает его потенциал. Это явление называется пиезоэлектрическим эффектом и активно используется в различных электронных устройствах и датчиках.
Однако при сжатии металла, его электродный потенциал может повышаться. При сжатии электроны отдаляются от поверхности металла, что увеличивает его потенциал. Это явление называется механической поляризацией и может быть применено в различных технических устройствах, например, в пьезокерамических пьезоэлектрических элементах.
- Механическое напряжение может вызывать изменение электродного потенциала металла.
- Растяжение металла снижает его потенциал, а сжатие – повышает.
- Эти явления используются, например, в пьезоэлектрических датчиках и устройствах.
Вопрос-ответ

Почему у разных металлов разный электродный потенциал?
Причина разной величины электродного потенциала у разных металлов заключается в различии их электрохимической активности. Каждый металл имеет свой электрохимический потенциал, который зависит от его способности участвовать в окислительно-восстановительных реакциях. Эта способность определяется физико-химическими свойствами металла, такими как электроотрицательность, электропроводность и т. д.
Какие факторы могут вызывать изменение электродного потенциала металла?
Электродный потенциал металла может меняться под влиянием различных факторов. Одним из основных факторов, влияющих на изменение потенциала, является окружающая среда. Взаимодействие металла с окружающей средой может вызывать растворение металла в электролите или образование окисленной пленки на поверхности металла, что приводит к изменению его потенциала. Также изменение потенциала может быть вызвано воздействием повышенных температур, механическим напряжениям, радиацией и другими факторами.
Может ли изменение электродного потенциала металла привести к коррозии?
Да, изменение электродного потенциала металла может быть связано с его коррозией. Коррозия — это процесс разрушения металла под воздействием окружающей среды. Когда электродный потенциал металла изменяется, его склонность к окислительно-восстановительным реакциям также может измениться. В результате этого, металл может раствориться в электролите или образовать окисленную пленку, что приводит к разрушению металлической структуры и образованию коррозионных процессов.
