Ионная связь является одной из основных форм химической связи, в которой возникают притяжение между ионами разных зарядов. Ионы – это заряженные атомы или группы атомов. Они могут образовываться как в результате отдачи или приема электронов, так и на основе ионизации атома.
Металлы, в отличие от неметаллов, обладают определенными свойствами, такими как хорошая проводимость электроны и тепла, гибкость и блеск. Эти свойства объясняются именно ионной связью между атомами металлов.
В ионной связи между атомами металлов возникает перенос электронов, что приводит к образованию положительно заряженных ионов - катионов. Эти катионы образуют кристаллическую решетку, где металлические ионы находятся в состоянии рассеяния. Электроны в металлах свободно движутся по всей решетке между положительно заряженными атомами, что обеспечивает силу связи и характерные свойства металлов.
Атомы металлов и ионная связь
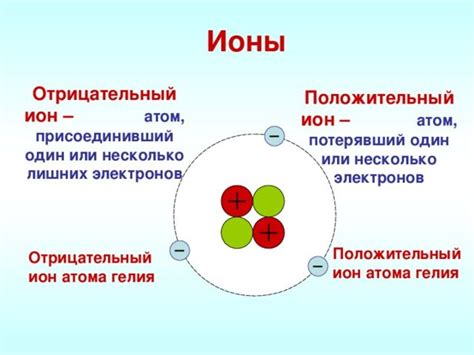
Ионная связь - это тип химической связи, который возникает между атомами металлов и неметаллов. Она основывается на притяжении положительно заряженных ионов металла к отрицательно заряженным ионам неметалла.
Атомы металлов обычно имеют маленькую электроотрицательность, что означает, что они имеют тенденцию отдавать электроны. Неметаллы, с другой стороны, имеют большую электроотрицательность и имеют склонность принимать электроны.
Когда атом металла отдает один или несколько электронов, он становится положительно заряженным ионом, которого называют катионом. Когда атом неметалла принимает эти электроны, он становится отрицательно заряженным ионом, которого называют анионом.
В ионной связи возникает сильное притяжение между катионами и анионами, что образует кристаллическую решетку. Эта решетка является устойчивой и стабильной структурой, что делает ионные соединения твердыми и хрупкими веществами.
Атомы металлов в ионной связи обычно образуют положительно заряженные ионы, так как они имеют небольшую электроотрицательность и готовы отдать электроны. Примером такого металла может быть натрий или алюминий.
Таким образом, в ионной связи между атомами металлов возникает сильное притяжение на основе обмена электронами, что приводит к образованию устойчивых ионных соединений.
Что такое ионная связь
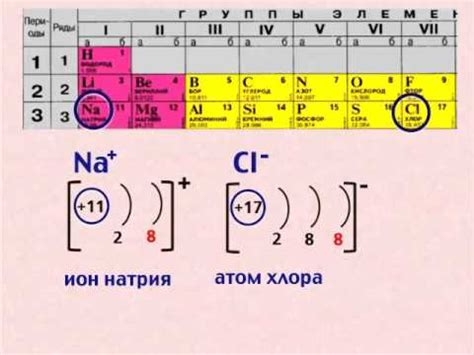
Ионная связь - это сила притяжения, действующая между положительно заряженными ионами металла и отрицательно заряженными ионами неметалла. В основе ионной связи лежит передача электронов от металла к неметаллу.
Ионная связь возникает из-за разности электроотрицательностей металла и неметалла. Металлы, как правило, имеют низкую электроотрицательность, поэтому легко отдают электроны и образуют положительно заряженные ионы. Неметаллы, напротив, имеют высокую электроотрицательность, поэтому легко принимают электроны и образуют отрицательно заряженные ионы.
В ионной связи между металлом и неметаллом образуется кристаллическая решетка, в которой положительно и отрицательно заряженные ионы располагаются вблизи друг друга. Связь между ионами является очень сильной, что придает многим соединениям с ионной связью специфические свойства, такие как высокие точки плавления и кипения.
Ионная связь проявляется во многих химических соединениях, в том числе в солях, оксидах и галогенидах. Примеры таких соединений: хлорид натрия (NaCl), оксид кальция (CaO), нитрат аммония (NH4NO3) и другие.
Структура атомов металлов

Структура атомов металлов отличается от структуры атомов неметаллов и обладает определенными особенностями. Атомы металлов имеют низкую электроотрицательность, что связано с их способностью отдавать электроны и образовывать ионные связи.
Атомы металлов обычно имеют большое число внешних электронов, которые легко могут быть отданы. В результате этого, ионы металлов образуются с положительным зарядом и обладают октетным строением электронов. Такая структура позволяет ионам металлов образовывать ионные решетки в кристаллической решетке металлов.
Структура атомов металлов также может быть представлена в виде кристаллической решетки, где положительно заряженные ионы располагаются в узлах решетки, а электроны образуют облака вокруг каждого иона. Такая структура обеспечивает металлам свойства, такие как высокая пластичность и проводимость электричества и тепла.
Определенные особенности структуры атомов металлов объясняют их способность образовывать ионные связи и использоваться в различных промышленных и научных областях. Ионная связь между атомами металлов является основой для образования металлических соединений и способствует образованию различных структур и свойств металлов.
Взаимодействие атомов металлов
Атомы металлов вступают во взаимодействие, образуя ионную связь. Ионная связь возникает, когда атомы металлов отдают свои внешние электроны атомам неметаллов.
В этом процессе происходит образование ионов, положительно заряженных катионами и отрицательно заряженных анионами. Катионы металлов имеют меньшую электроотрицательность, поэтому они отдают свои электроны анионам неметаллов.
Ионная связь обладает сильной электростатической силой притяжения между катионами и анионами. Эта сила приводит к образованию кристаллической решетки, в которой атомы металлов располагаются в упорядоченном порядке. Кристаллическая решетка обеспечивает структурную прочность металлов.
Взаимодействие атомов металлов также обусловливает множество свойств металлов, таких как высокая теплопроводность, электропроводность и пластичность. Благодаря ионной связи атомы металлов образуют электронное облако, которое позволяет электронам свободно двигаться и переносить электрический ток.
Таким образом, взаимодействие атомов металлов через ионную связь является основой для формирования их химических и физических свойств и обуславливает множество уникальных характеристик металлических материалов.
Факторы, влияющие на возникновение ионной связи между атомами металлов
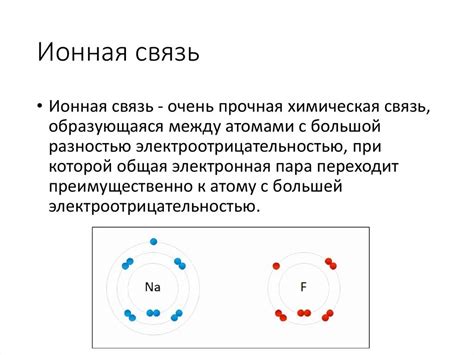
Ионная связь между атомами металлов возникает при выполнении определенных условий. Основными факторами, которые влияют на возникновение ионной связи, являются:
- Электроотрицательность атомов. Чем больше разница в электроотрицательности между атомами, тем сильнее будет ионная связь. Металлы, обладающие низкой электроотрицательностью, имеют большую склонность к образованию ионной связи.
- Число валентных электронов. У атомов металлов, имеющих малое число валентных электронов, возможно переход этих электронов на атомы других элементов, что способствует образованию ионной связи.
- Размер атомов. Чем меньше размер атомов металлов, тем больше вероятность их соприкосновения и перехода электронов, что способствует образованию ионной связи.
- Кристаллическая структура. Ионная связь часто формируется в кристаллической структуре металлов, где атомы расположены в регулярном порядке и образуют ионы с положительным и отрицательным зарядом.
Эти факторы взаимно влияют друг на друга и определяют вероятность возникновения ионной связи между атомами металлов. Чем больше значения этих факторов соответствуют требованиям ионной связи, тем сильнее будет образовываться связь между атомами металлов.
Важность ионной связи для свойств металлов

Металлы являются основными строительными блоками современного мира и играют ключевую роль во многих отраслях промышленности. Одной из основных причин их уникальных свойств является ионная связь между атомами металлов.
Ионная связь представляет собой силу притяжения между положительно заряженными ионами металлов и отрицательно заряженными электронами. Эта связь крайне прочна и позволяет металлам обладать высокой температурной и механической стойкостью.
Благодаря ионной связи, металлы обладают отличными электропроводными свойствами. Ионы металлов легко перемещаются в решетке металлической структуры, образуя так называемое "море электронов". Именно эти свободные электроны являются причиной проводимости металлов и используются в различных электронных устройствах.
Кроме того, ионная связь играет решающую роль в формировании структуры и формы металлов. Именно благодаря этой связи металлы образуют кристаллическую решетку, что придает им устойчивость и позволяет выдерживать большие деформации без разрушения.
Важность ионной связи для свойств металлов подчеркивается их широким применением. Именно благодаря этой связи металлы обладают высокой прочностью, термической и электрической проводимостью, а также способностью быть слегка гибкими. Без ионной связи металлы не могли бы обладать своими уникальными свойствами и быть основой для множества технологических и промышленных процессов.
Вопрос-ответ

Как возникает ионная связь между атомами металлов?
Ионная связь между атомами металлов возникает из-за перехода электронов от одного атома к другому. Металлы обычно содержат отрицательно заряженные электроны в своей валентной оболочке, которые слабо привязаны к ядру и могут свободно двигаться. Когда металлические атомы сходятся, эти свободные электроны могут переходить от одного атома к другому, образуя положительно заряженные ионы и образцы ионной связи между атомами металлов.
Какие примеры можно найти ионной связи между атомами металлов?
Примеры ионной связи между атомами металлов можно найти во многих металлургических соединениях, таких как соль натрия хлорида и магния оксида. В соли натрия хлорида, катионы натрия и анионы хлорида образуются из-за перехода электронов от атома натрия к атому хлора, что создает ионную связь между двумя атомами металлов. Такие ионные соединения обычно обладают высокой степенью электропроводности и характерным кристаллическим строением.
