Взаимодействие соляной кислоты (HNO3) с металлами является одним из основных процессов в химии. Эта реакция называется окислительным взаимодействием, так как в ее результате происходит окисление металла. HNO3 является сильным окислителем, что обуславливает ее способность образовывать ионы NO3- и окислять металлы.
Окисление металлов в результате взаимодействия с HNO3 происходит путем передачи электронов от металла к ионам NO3-. При этом образуются ионы металла со своим степенью окисления и ионы NO3-. Часто такая реакция сопровождается выделением газа – водорода. Это объясняется тем, что при окислении металла электроны передаются на ионы H+ из HNO3, образуя молекулы воды (H2O) и молекулы газообразного водорода (H2).
Окисление металлов с помощью HNO3 может происходить с разной скоростью в зависимости от свойств металла и концентрации кислоты. Некоторые металлы, такие как цинк и железо, могут образовывать пассивную пленку на поверхности, что замедляет процесс окисления. Другие металлы, такие как алюминий и медь, могут растворяться в HNO3 с образованием комплексных ионов.
Важно отметить, что взаимодействие HNO3 с металлами является опасным и может привести к возникновению взрывоопасных ситуаций. Прежде чем проводить любые эксперименты, необходимо ознакомиться с соответствующими правилами и нормами безопасности.
Взаимодействие HNO3 с металлами
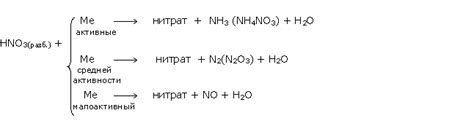
Взаимодействие азотной кислоты (HNO3) с металлами является одним из основных процессов, которые происходят при контакте этих веществ. HNO3 обладает сильными окислительными свойствами, поэтому она способна вызывать окисление металлов.
При контакте HNO3 с металлами происходит реакция окисления, в результате которой металлы переходят в ионы металла, а нитратная группа (NO3-) остается в растворе. Окисление металлов в этой реакции сопровождается выделением газа - водорода (H2), что делает этот процесс хорошо заметным.
HNO3 взаимодействует с различными металлами, включая щелочные, щелочноземельные и переходные металлы. Некоторые металлы, такие как алюминий (Al) и цинк (Zn), реагируют с азотной кислотой более активно и интенсивно выделяют водород.
Взаимодействие HNO3 с металлами можно использовать для их качественной и количественной анализа. В результате реакции окисления металла до иона можно определить присутствие и количество конкретного металла в образце.
Учитывая сильные окислительные свойства HNO3, при работе с ней необходимо соблюдать осторожность и применять защитное оборудование, чтобы избежать контакта с кожей и глазами.
Окисление металлов

Окисление металлов - это процесс, при котором металлы вступают в химическую реакцию с кислородом, выделяясь в виде ионов с положительным зарядом. Окисление может происходить как в атмосфере, так и в растворах кислот или щелочей.
Основным окислителем при окислении металлов является кислород. При взаимодействии металла с кислородом происходит передача электронов от металла к кислороду, что приводит к образованию положительно заряженных ионов металла и отрицательно заряженных ионов кислорода.
Окисление металлов может протекать как при контакте с воздухом, так и при взаимодействии с кислотами. Например, медь при контакте с кислородом воздуха окисляется и образует зеленоватую патину. Также известен пример окисления железа, при котором происходит образование ржавчины.
Уровень активности металла влияет на скорость и интенсивность процесса окисления. Более активные металлы, такие как натрий или калий, реагируют с кислородом намного быстрее и интенсивнее, чем менее активные металлы, например, серебро или золото.
Окисление металлов можно использовать в различных областях. Например, в процессе производства стали окисление железа приводит к образованию оксида железа, который является основным компонентом стального сплава. Также окисление металлов может быть использовано в химических реакциях для получения других соединений металлов.
Выделение водорода
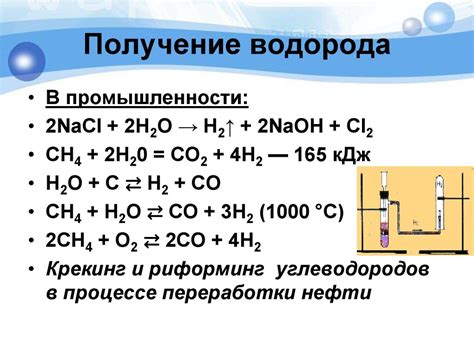
Выделение водорода – это одна из ключевых реакций взаимодействия HNO3 с металлами. В результате этой реакции металлы окисляются, а нитраты металлов присутствуют в получаемом растворе. Главной целью выделения водорода является исследование активности металла и оценка его способности реагировать с кислотой.
Выделение водорода происходит при взаимодействии металла с разбавленной HNO3. В результате окисления металла и восстановления кислорода в кислоте образуется гидроксид металла и диоксид азота, а также выделяется водородный газ. При этом реакция может протекать с различной интенсивностью в зависимости от активности металла и концентрации кислоты.
Одним из способов выделения водорода является его сбор над водой. При этом газ собирается над открытой колбой с водой, погруженной в сосуд с водой. Выделенный газ заполняет верхнюю часть колбы и можно наблюдать его как пузырьки, поднимающиеся над поверхностью воды. Для увеличения эффективности сбора можно использовать аппарат Джелинского или каскадную систему с колбами.
Вопрос-ответ

Какие металлы могут взаимодействовать с HNO3?
HNO3 может взаимодействовать с широким спектром металлов, включая железо, медь, цинк, алюминий и другие.
Можно ли использовать HNO3 для очистки металлических поверхностей?
Да, HNO3 можно использовать для очистки металлических поверхностей. Оно способно удалять оксидные пленки и загрязнения с поверхности металла, оставляя его чистым.
