Серная кислота (H2SO4) является одним из наиболее известных и широко используемых химических соединений. Она обладает множеством уникальных свойств, которые определяют ее роль во многих промышленных и химических процессах. Важно понять, является ли H2SO4 оксидом металла или основанием.
Согласно определению, оксид металла - это химическое соединение, содержащее атомы металла и кислорода. Основание же - это химическое соединение, способное отдавать водородные ионы в растворе. Итак, какие свойства H2SO4 позволяют определить его природу?
Во-первых, H2SO4 обладает кислотными свойствами. Она реагирует с водой, формируя ионы водорода (H+) и сульфата (SO4^2-), что позволяет классифицировать ее как кислоту. Эта реакция наблюдается как в растворе H2SO4, так и при смешивании с веществами, содержащими воду.
Однако H2SO4 также может выступать в роли основания. Это происходит при реакции с веществами, которые способны отдавать протонные ионы, например сильными кислотами. В результате образуются ионы сульфатной кислоты (HSO4^-), и H2SO4 действует как основание. Такое поведение свидетельствует о дуализме свойств H2SO4 и его способности проявлять как кислотные, так и основные характеристики.
Реакция с металлами
Концентрированная серная кислота (H2SO4) ведет себя по-разному в реакции с различными металлами. Она обладает способностью взаимодействовать с некоторыми металлами, образуя соль и выделяя водород.
Серная кислота реагирует с активными металлами из группы щелочных металлов (например, натрием и калием), превращая их в соответствующие соли и выделяя водород. Реакция такого рода является очень интенсивной, сопровождается выделением большого количества тепла и водорода.
Некоторые более пассивные металлы, такие как железо и цинк, также реагируют с H2SO4. Однако в этом случае реакция протекает гораздо медленнее и требует повышения температуры или использования дополнительных катализаторов.
Реакция металлов с H2SO4 может описываться следующей химической формулой:
| Металл | Реакция |
| Na | 2Na + H2SO4 → Na2SO4 + H2 |
| K | 2K + H2SO4 → K2SO4 + H2 |
| Fe | Fe + H2SO4 → FeSO4 + H2 |
| Zn | Zn + H2SO4 → ZnSO4 + H2 |
В реакции с металлами оксид металла, эта особенность свойств H2SO4 проявляется только в реакциях с металлами группы щелочных металлов. В остальных случаях она является кислотой и реагирует с металлами как с кислотным оксидом, образуя соответствующие соли и выделяя водород.
Свойства кислоты

Кислоты - это важный класс химических соединений, имеющих ряд характерных свойств. Кислоты обладают кислотностью, то есть способностью отдавать протоны (водородные ионы) в реакциях с другими веществами. Кислотность кислот проявляется в их реакции с основаниями, образуя соль и воду.
Другой характерной свойство кислоты - это образование водородионов при диссоциации в водном растворе. В результате диссоциации, многие кислоты образуют положительные водородные ионы, которые при взаимодействии с водой образуют неполярные молекулы.
Также следует отметить, что некоторые кислоты проявляют коррозионную активность. Они способны поражать материалы, такие как металлы, полимеры и др., и вызывать их разрушение или изменение свойств. Коррозионная активность кислот может быть определена по их pH-значению.
Еще одним важным свойством кислоты является их растворимость в воде. Некоторые кислоты легко растворяются, образуя хорошо проводящие ток растворы, в то время как другие кислоты слабо растворимы или практически не растворимы в воде.
Кислоты также обладают специфическими физическими свойствами, такими как высокая плотность, высокая вязкость и обычно сильные запахи. Некоторые кислоты имеют твердую форму при комнатной температуре и только при нагревании переходят в жидкое состояние.
В общем, свойства кислот обусловлены их структурой и способностью отдавать протоны при реакциях с веществами. Изучение этих свойств позволяет понять особенности кислот и их применение в различных областях науки и техники.
Кислотная диссоциация
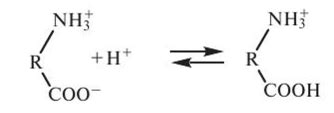
Кислотная диссоциация – это процесс распада кислоты на ионы водорода (H+) и отрицательные ионы. Реакция диссоциации кислоты в растворе протекает из-за слабости связи между атомами водорода и атомами кислоты.
Диссоциация серной кислоты (H2SO4) происходит с образованием двух ионов водорода (2H+) и одного аниона сернокислого (HSO4-). Данный процесс можно записать следующим образом:
H2SO4 → 2H+ + HSO4-
Кислотная диссоциация характеризуется числом иона водорода, образующихся при диссоциации одной молекулы кислоты. Такое число называют кислотностью кислоты. В случае серной кислоты ее кислотность равна 2.
На рисунке ниже приведена таблица с кислотностями нескольких общеизвестных кислот:
| Название кислоты | Формула | Кислотность |
|---|---|---|
| Серная кислота | H2SO4 | 2 |
| Соляная кислота | HCl | 1 |
| Уксусная кислота | CH3COOH | 1 |
| Фосфорная кислота | H3PO4 | 3 |
Влияние на окружающую среду

Содержащаяся в серной кислоте сера может вызывать отрицательные последствия для окружающей среды. При сгорании серы образуются вредные газы, которые способны загрязнять атмосферу. Одним из таких газов является диоксид серы (SO2), который в сочетании с водными испарениями может образовывать серную кислоту. Это может приводить к образованию кислотных дождей, которые имеют разрушительное воздействие на растительный и животный мир.
Серная кислота также является коррозионно активным веществом, способным вызывать повреждения металлических и неметаллических поверхностей. Это может приводить к повреждению инфраструктуры, включая здания, транспортные средства и инженерные сооружения.
При попадании серной кислоты в водные системы она может вызывать загрязнение воды и негативное воздействие на экосистемы. Она может уничтожать живые организмы, включая рыб и других водных животных, а также снижать качество воды для питья.
В целом, из-за ее химических свойств и высокой коррозионной активности, серная кислота может иметь значительное отрицательное влияние на окружающую среду и вызывать серьезные проблемы для здоровья человека и экосистем.
Вопрос-ответ

Что такое H2SO4?
H2SO4 - это химическое соединение, известное как серная кислота. Она состоит из двух молекул воды (H2O) и одной молекулы серы (S). Серная кислота является одним из самых важных промышленных химических соединений, применяемых в различных отраслях, включая производство удобрений, нефтепереработку и очистку воды.
Можно ли сказать, что H2SO4 - оксид металла?
Нет, H2SO4 не является оксидом металла. Она является кислотой, которая образуется при реакции сероводорода (H2S) с кислородом (O2). Оксиды металлов, наоборот, образуются при реакции металлического элемента с кислородом и являются основными соединениями металлов.
