Периодическая система химических элементов является удивительным способом организовать и классифицировать все известные химические элементы. Одной из важных групп элементов в этой системе является группа металлов.
Металлы представляют собой категорию химических элементов, обладающих определенными физическими и химическими свойствами. Они характеризуются высокой проводимостью электричества и тепла, а также обычно являются твердыми и блестящими. В периодической системе металлы обычно располагаются слева и посередине таблицы.
Группа металлов включает различные элементы, такие как железо, алюминий, медь, свинец, цинк, никель, серебро, золото и многие другие. Эти металлы широко используются в различных отраслях промышленности и находят применение в производстве металлических конструкций, электроники, автомобильной промышленности и других областях.
Кроме того, металлы играют важную роль в химических реакциях и взаимодействиях. Они могут образовывать различные соединения с другими элементами, что позволяет использовать их в качестве катализаторов, а также в процессах синтеза новых веществ.
Роль металлических элементов в периодической системе

Металлические элементы являются важной группой в периодической системе химических элементов. Они обладают рядом особенностей, которые делают их неотъемлемой частью материального мира и являются основой для различных технологий и промышленных процессов.
Во-первых, металлические элементы обладают высокой электропроводностью, что делает их идеальными материалами для проводов и электрических контактов. Они способны эффективно переносить электрический ток и применяются в различных устройствах, начиная от электрических проводов и заканчивая электронными компонентами.
Во-вторых, металлические элементы обладают высокой теплопроводностью. Они способны переносить тепло эффективно и применяются в конструкциях, где требуется равномерное распределение тепла, например, в теплообменниках. Благодаря своим свойствам, металлические материалы широко используются в промышленности и строительстве.
Кроме того, металлические элементы часто обладают высокой прочностью и устойчивостью к износу, что делает их идеальными материалами для создания различных инженерных конструкций и оборудования. Они используются в производстве автомобилей, самолетов, кораблей, мостов и других сооружений.
Благодаря своим уникальным свойствам, металлические элементы играют ключевую роль в различных областях, от промышленности и энергетики до медицины и электроники. Они являются неотъемлемой частью современного мира и продолжают активно применяться в различных сферах деятельности человека.
Металлы: свойства и химические реакции
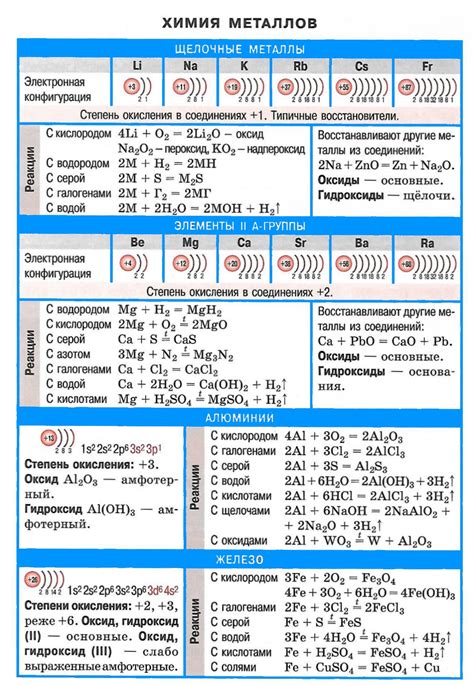
Металлы - это группа химических элементов, обладающих особыми свойствами. Они отличаются высокой тепло- и электропроводностью, прочностью, пластичностью и блеском. Многие металлы имеют высокую плотность и тяжелы на ощупь. Эти свойства делают металлы важными для различных отраслей промышленности и строительства.
Металлы способны образовывать ионы положительного заряда и легко теряют электроны при химических реакциях. Оксиды металлов имеют щелочную реакцию и растворяются в воде, образуя гидроксиды. Металлы могут образовывать соли, реагируя с кислотами.
Металлы показывают разнообразные реакции с кислородом. Некоторые металлы способны гореть на воздухе: горение магния сопровождается ярким свечением и выделением большого количества тепла. Другие металлы, такие как железо, образуют окисленные образцы при взаимодействии с кислородом. Они могут образовывать ржавчину на поверхности.
Металлы также могут образовывать соединения с неметаллами. Например, металлы могут реагировать с хлором, образуя хлориды. Эти реакции могут быть взрывоопасными или ядовитыми, поэтому необходимо соблюдать осторожность.
Использование металлов в разных сферах жизни - одно из важнейших достижений человечества. Железо, алюминий, медь и другие металлы используются для создания инструментов, машин, электроники, а также в строительстве и производстве автомобилей. Металлы давно стали неотъемлемой частью нашей жизни и без них современная технологическая цивилизация была бы невозможна.
Переходные металлы: особенности расположения и свойства

Переходные металлы – это группа элементов, расположенных в середине периодической системы химических элементов, между металлами главной подгруппы и элементами побочных подгрупп. Они занимают блок д из-за особенности их последовательной заполненности электронных оболочек.
Основной характеристикой переходных металлов является изменчивость их внешней электронной оболочки. Это позволяет им образовывать соединения с различными элементами и обладать разнообразными свойствами. Важная особенность переходных металлов – способность образовывать соединения с переменной степенью окисления.
Внешняя электронная оболочка переходных металлов содержит переменное число электронов, что приводит к возможности наличия нескольких энергетически близких электронных уровней, что, в свою очередь, позволяет им образовывать соединения с различными атомами, обладающими разными энергетическими уровнями. В результате возможны различные окислительные состояния переходных металлов, что делает их способными к представлению различных цветов в соединениях, создающих разнообразие окрасок в природе.
Переходные металлы также обладают высокой электропроводностью, прочностью и твердостью, что делает их очень полезными для различных индустриальных и технологических приложений. Они используются в производстве металлургических сплавов, катализаторов, магнитов, электроники и многих других областях, где требуется их уникальная комбинация свойств.
Лантаноиды и актиноиды: металлические элементы с уникальными свойствами
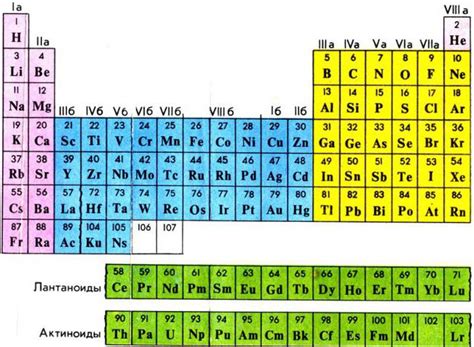
Лантаноиды и актиноиды – это две группы металлических элементов, которые располагаются в периодической системе химических элементов под основным блоком.
Значительное внимание уделяется исследованию и использованию лантаноидов и актиноидов из-за их уникальных свойств. Одно из ключевых свойств данных элементов – их способность образовывать ионы в различных степенях окисления. Это позволяет использовать их в качестве катализаторов во многих химических реакциях.
Лантаноиды обладают подобными свойствами их третьего элемента – лантана. Из них самыми широко используемыми являются церий и неодим, которые применяются в производстве автомобилей, электроники и других отраслях промышленности.
Актиноиды, в свою очередь, являются элементами из актиния и обладают еще более уникальными свойствами. Они отличаются очень высокой плотностью и радиоактивностью. Именно из-за этих свойств актиноиды имеют большое значение в науке и применяются в исследованиях по созданию новых материалов и ядерной энергетике.
Исследование свойств и применение лантаноидов и актиноидов играют важную роль в современной науке и технологии. Они предоставляют уникальные возможности и перспективы для различных областей промышленности и научных исследований.
Щелочные металлы: группа с самыми активными элементами
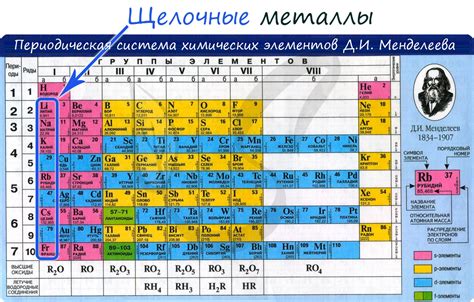
Щелочные металлы - это группа элементов в периодической системе химических элементов, которая находится слева от таблицы. В группе щелочных металлов находятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Все эти металлы обладают сходными свойствами и характеризуются высокой активностью.
Щелочные металлы имеют один валентный электрон во внешней оболочке и легко отдают этот электрон. Из-за этого они становятся самыми активными металлами в периодической системе. Благодаря своей активности щелочные металлы реагируют с водой, кислородом и большинством неметаллов, образуя соответствующие оксиды или соли. Франций - самый редкий и радиоактивный элемент в группе щелочных металлов и имеет очень короткий период полураспада.
Щелочные металлы очень мягкие и легкие, что делает их удобными для применения в различных отраслях промышленности. Например, литий используется в батареях, натрий - в производстве стекла и мыла, а калий - в удобрениях. Кроме того, щелочные металлы хорошо проводят электричество и тепло, что делает их важными компонентами в различных электронных устройствах и технологиях.
Щелочноземельные металлы: свойства и значение в практике

Щелочноземельные металлы представлены в периодической системе химических элементов группой IIA. К ним относятся бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Эти металлы обладают рядом сходных свойств, которые определяют их значение в практике.
Одним из главных характеристик щелочноземельных металлов является их высокая электропроводность. Это свойство делает их незаменимыми в производстве электрических проводов и контактов. Кроме того, они применяются в производстве батарей и аккумуляторов, где их электропроводность обеспечивает эффективную передачу энергии.
Еще одним важным свойством щелочноземельных металлов является их способность реагировать с водой. При этом они выделяются водород и образуют гидроксиды. Это свойство используется в процессе производства кислорода при электролизе воды.
Бериллий, один из наиболее известных щелочноземельных металлов, обладает такими свойствами, как легкость и прочность. Именно поэтому его используют при создании легких конструкций, а также в производстве сплавов с другими металлами. Кроме того, бериллий обладает высокой теплопроводностью и применяется в производстве ядерных реакторов и аппаратной электроники.
В целом, щелочноземельные металлы имеют широкое применение в различных сферах промышленности. Их свойства и высокая химическая активность делают их востребованными материалами для создания различных конструкций и промышленных изделий.
Постпереходные металлы: основные представители и свойства

Постпереходные металлы - это группа элементов в периодической системе химических элементов, расположенная между переходными металлами и полупроводниками. Эта группа состоит из 14 элементов, включая группу цинк, группу кадмий и группу ртуть.
Основными представителями постпереходных металлов являются цинк, кадмий и ртуть. Цинк (Zn) обладает благородными свойствами и часто используется в производстве сплавов и анодов, а также в качестве покрытия для защиты от коррозии. Кадмий (Cd) также используется в сплавах, а его соединения применяются в электронике, фотографии и кадмиевых аккумуляторах. Ртуть (Hg) является единственным металлом, которым можно заполнить ртутный термометр и применять в термоэлектрических устройствах.
Свойства постпереходных металлов имеют свои особенности. Например, цинк обладает низкой температурой плавления и высокой устойчивостью к коррозии. Кадмий является мягким металлом, который легко обрабатывается. Ртуть является жидким металлом при комнатной температуре и имеет специфическую плотность. Постпереходные металлы обладают разными химическими свойствами и могут образовывать различные соединения, что делает их важными для различных промышленных процессов и технологий.
Выводы:
- Постпереходные металлы - это группа элементов, которая находится между переходными металлами и полупроводниками в периодической системе химических элементов.
- Основными представителями постпереходных металлов являются цинк, кадмий и ртуть.
- Постпереходные металлы имеют различные свойства, такие как низкая температура плавления, высокая устойчивость к коррозии и возможность образования различных соединений.
- Цинк используется в производстве сплавов и анодов, кадмий - в электронике и фотографии, ртуть - в термоэлектрических устройствах.
Блок p: металлы со специфической составляющей
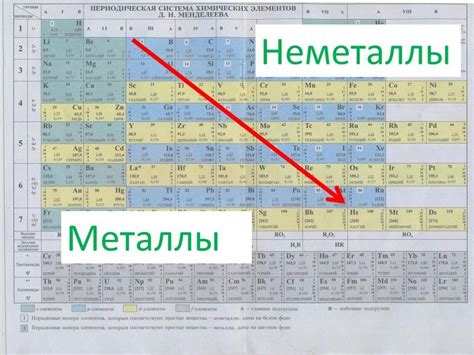
В периодической системе химических элементов металлы со специфической составляющей находятся в блоке p. Этот блок расположен между блоком s и блоком d. Металлы этого блока обладают определенными химическими и физическими свойствами, которые делают их особенными в сравнении с другими группами металлов.
Основными элементами блока p являются бор, алюминий, галлий, индий и таллий. Эти элементы отличаются от других металлов периодической системы своими электронными конфигурациями и атомными радиусами. Например, бор является полуметаллом, так как он обладает как металлическими, так и неметаллическими свойствами.
Металлы блока p также имеют особый электронный строение. Их внешний энергетический уровень заполнен нестандартно, что придает им дополнительные химические свойства. Элементы этого блока способны образовывать химические соединения с различными элементами, как металлическими, так и неметаллическими.
Примечательно, что некоторые элементы блока p имеют специфические применения в промышленности и научных исследованиях. Например, алюминий широко используется в производстве легких и прочных конструкций, а бор находит применение в нуклеарной энергетике и стекольной промышленности.
Вопрос-ответ

Что такое группа металлических элементов в периодической системе химических элементов?
Группа металлических элементов в периодической системе химических элементов - это ряд элементов, обладающих общими свойствами, такими как химическая активность, металлический блеск, хорошая электропроводность и теплопроводность. Эти элементы находятся в левой части периодической таблицы и включают такие металлы, как литий, натрий, калий, магний, алюминий, железо, медь и другие.
Какие свойства присущи группе металлических элементов?
Группа металлических элементов обладает рядом общих свойств, таких как металлический блеск (за исключением ряда элементов, таких как железо и медь), химическая активность, хорошая электропроводность и теплопроводность. Они также обычно обладают высокой плотностью, что делает их тяжелыми элементами. Кроме того, они способны образовывать положительные ионы, которые легко реагируют с другими элементами.
Какие элементы относятся к группе металлических элементов?
К группе металлических элементов относятся элементы периодической таблицы, которые находятся в левой части таблицы. Это включает элементы первой и второй групп, а также элементы из групп 3-12, которые называются переходными металлами. Конкретные элементы включают литий, натрий, калий, магний, алюминий, железо, медь и многие другие.
Какую роль играют металлические элементы в химии и промышленности?
Металлические элементы играют важную роль в химии и промышленности. Они широко используются в производстве различных материалов, включая металлы и сплавы, которые являются основой для строительства, машиностроения и других отраслей промышленности. Металлы также используются в производстве множества продуктов, таких как батарейки, провода, магниты и многое другое. Они также находят применение в медицине, электронике, авиации и многих других областях.
