Периодическая таблица – это основа химической науки. Она представляет собой систематическую организацию химических элементов по их атомным свойствам и с учетом их последовательных атомных номеров. Эта таблица позволяет лучше понять и предсказывать взаимодействие и свойства различных элементов.
Первый ряд таблицы начинается с наиболее химически активных металлов - щелочных металлов. Эти элементы, такие как литий, натрий и калий, обладают низкой плотностью, низкой температурой плавления и реагируют с водой, образуя щелочные растворы. Щелочные металлы широко используются в различных промышленных процессах и в производстве аккумуляторов.
Следующий ряд таблицы включает щелочноземельные металлы, такие как магний и кальций. Щелочноземельные металлы являются менее активными, чем щелочные металлы, но все же обладают высокой реактивностью. Они имеют большую плотность и температуру плавления, чем щелочные металлы, и широко используются в производстве сплавов и пиротехнических смесей.
В центральной части таблицы находятся переходные металлы, такие как железо, медь и цинк. Они обладают разнообразными физическими и химическими свойствами и широко применяются в различных областях, включая строительство, электронику и пищевую промышленность.
В последних рядах таблицы находятся так называемые инертные газы, такие как гелий и неон. Инертные газы обладают низкой реактивностью и практически не вступают в химические реакции. Они широко используются в научных исследованиях, в анализе газов и в различных промышленных процессах.
Щелочные металлы: особенности и свойства

Щелочные металлы - это группа элементов первой группы периодической таблицы. В эту группу входят литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они отличаются высокой реактивностью и активностью, что делает их самыми химически активными металлами.
Одной из основных особенностей щелочных металлов является их мягкость. Они настолько мягкие, что могут быть нарезаны ножом. Кроме того, они обладают низкой плотностью, что делает их легкими и хорошо плавающими в воде. Именно поэтому щелочные металлы широко используются в производстве легких конструкций и элементов бытовой техники.
Щелочные металлы также известны своей высокой химической реактивностью. Они активно реагируют с водой, кислородом и многими другими веществами. Кроме того, они обладают способностью образовывать соли и гидроксиды. Например, гидроксид натрия (NaOH), получаемый из обработки натрия водой, широко используется в бытовых и промышленных целях.
Не следует забывать и о том, что щелочные металлы являются отличными проводниками электричества. Они обладают высокой электропроводностью, что делает их незаменимыми в производстве аккумуляторов и других электронных устройств. Благодаря своим свойствам, щелочные металлы нашли широкое применение в различных отраслях промышленности и науки.
Переходные металлы: средняя часть таблицы
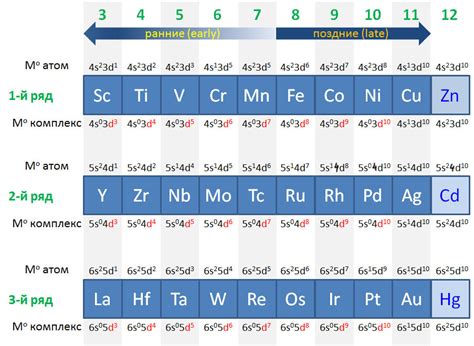
Периодическая таблица элементов химии включает в себя различные классы элементов, и одной из наиболее интересных и важных групп являются переходные металлы. Они занимают центральную часть таблицы и включают элементы с атомными номерами от 21 до 30, а также от 39 до 48.
Переходные металлы обладают множеством уникальных свойств, которые делают их необходимыми для многих процессов и приложений. Они обладают высокой прочностью, твёрдостью и пластичностью, что делает их идеальными материалами для производства различных сплавов и конструкций.
Кроме того, переходные металлы играют большую роль в каталитических процессах, так как они способны активировать множество химических реакций. Они также играют важную роль в биологии, участвуя в формировании металлопротеинов и ферментов.
Переходные металлы образуют стабильные соединения с другими элементами, образуя так называемые комплексные соединения. Эти соединения обладают разнообразными цветами и свойствами, что делает переходные металлы очень интересными и полезными для исследований и приложений в различных областях науки и технологий.
Постпереходные металлы: отличия и применение

Постпереходные металлы - это группа элементов, расположенных в периодической таблице между щелочными и щелочноземельными металлами и рядом с основными металлами. Они включают элементы такие как алюминий, цинк, индий, олово и свинец.
В отличие от щелочных металлов, постпереходные металлы обладают большей прочностью и твердостью. Они являются хорошими проводниками тепла и электричества, а также обладают высокой устойчивостью к коррозии. Эти свойства делают постпереходные металлы идеальными для использования в различных промышленных отраслях.
Алюминий является одним из самых распространенных постпереходных металлов. Он обладает легким весом, высокой прочностью и отличной коррозионной стойкостью. Алюминий широко применяется в производстве авиационной и автомобильной промышленности, а также в строительстве и упаковочной промышленности.
Цинк также является важным постпереходным металлом. Он используется в производстве огнеупорных материалов, высокопрочных сплавов и в отрасли строительных материалов. Цинковые покрытия используются для защиты металлических поверхностей от коррозии.
Индий и олово также имеют свои уникальные свойства и применения. Индий широко используется в производстве жидкокристаллических дисплеев, солнечных батарей и полупроводников. Олово применяется в производстве сплавов, припоев и покрытий, а также в конденсаторах и батареях.
В заключение, постпереходные металлы представляют собой важную группу элементов в периодической таблице. Они отличаются от других металлов своими свойствами и находят широкое применение в различных отраслях промышленности. Алюминий, цинк, индий, олово и свинец - это всего лишь некоторые примеры постпереходных металлов, которые играют важную роль в нашей повседневной жизни.
Металлоиды: свойства и роль
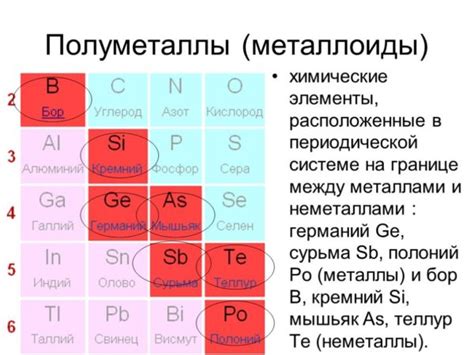
Металлоиды - это элементы периодической таблицы, которые обладают свойствами как металлов, так и неметаллов. Они занимают промежуточное положение между металлами и неметаллами и имеют уникальные свойства, которые важны для различных областей науки и технологий.
Одним из главных свойств металлоидов является их способность проводить электрический ток, но только при определенных условиях. Они обладают полупроводниковыми свойствами, что делает их особенно ценными для электронной промышленности. Металлоиды, такие как кремний и германий, широко используются в современных электронных устройствах, включая компьютеры, телефоны и солнечные батареи.
Кроме того, металлоиды играют важную роль в химической промышленности. Они могут выполнять функцию катализаторов, позволяющих ускорить химические реакции. Например, мышьяк, который является металлоидом, широко применяется в производстве лекарственных препаратов и пестицидов.
Еще одной важной ролью металлоидов является их влияние на окружающую среду. Например, мышьяк и сурьма являются токсичными веществами и могут повлиять на здоровье людей и окружающую природу. Поэтому их использование регулируется международными стандартами и требует особой осторожности.
Металлоиды представляют собой важную группу элементов периодической таблицы, которые объединяют в себе свойства металлов и неметаллов. Их уникальные свойства и роль в различных сферах науки и технологий делают их неотъемлемой частью современного мира.
Неметаллы: разнообразие и применение

Неметаллы – это элементы, которые не обладают металлическими свойствами, такими как хорошая термическая и электрическая проводимость. В периодической таблице они находятся справа от чередующейся линии металлов. Разнообразие неметаллов включает в себя такие элементы, как кислород, азот, сера, фосфор, хлор и многие другие.
Неметаллы играют важную роль во множестве сфер нашей жизни. Кислород, например, является неотъемлемым компонентом атмосферы и необходим для поддержания жизни. Азот применяется в производстве удобрений и пищевой промышленности. Сера используется в производстве пластмасс, резиновых изделий и горючих веществ. Фосфор используется в производстве удобрений, огнетушителей и стекла. Хлор широко применяется в производстве пластмасс, белков, лекарственных препаратов и многих других продуктов.
Помимо промышленного применения, неметаллы играют важную роль в нашей жизни и здоровье. Например, йод является необходимым элементом в питании человека и его недостаток может привести к заболеваниям щитовидной железы. Фтор применяется в стоматологии для защиты зубов от кариеса. Эти и другие неметаллы неотъемлемы для правильного функционирования нашего организма.
Таким образом, неметаллы представляют собой разнообразную группу элементов с широким спектром применения. Они играют важную роль в различных отраслях промышленности, а также в нашей повседневной жизни. Без неметаллов невозможно представить нашу современную цивилизацию и ее достижения.
Инертные газы: особенности и использование

Инертные газы - это группа химически нейтральных газов, которые практически не реагируют с другими элементами и соединениями. Их отличительной особенностью является полная заполненность электронными оболочками и отсутствие возможности принять или отдать электроны.
Одним из наиболее распространенных инертных газов является аргон. Он широко используется в промышленности для создания инертной атмосферы, защиты от окисления и предотвращения взрывоопасных реакций. Аргон применяется при сварке, печати металлов, производстве полупроводниковых материалов и других технологических процессах.
Другим известным инертным газом является неон. Он наиболее известен своим свечением в рекламных вывесках и освещении. Неон является одним из редких инертных газов, который образует стабильные соединения с другими элементами, такими как хлор, фтор и галогены. Этим объясняется его применение в производстве лазеров, гелиево-неоновых лазеров и других источников света.
Криптон и ксенон также являются инертными газами и находят применение в различных областях. Криптон используется в электрических выключателях, фильтрах для очистки воздуха и в световых источниках. Ксенон широко применяется в автомобильной промышленности для создания ярких фар и фар для ксеноновых ламп.
Инертные газы также используются в биологии и медицине. Например, диоксид углерода является инертным газом и используется для создания искусственной атмосферы в инкубаторах для выращивания клеток и тканей. В медицине инертные газы применяются для анестезии и искусственной вентиляции легких.
Вопрос-ответ

Какие элементы входят в группу щелочных металлов?
В группу щелочных металлов входят литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Почему щелочные металлы считаются самыми активными?
Щелочные металлы считаются самыми активными, так как они имеют одну валентную электронную оболочку, которая легко отдается при вступлении в химические реакции. Это обусловлено их низкой ионизационной энергией.
Какие элементы являются инертными газами?
Инертными газами являются элементы группы 18 (VIII A) периодической таблицы: гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) и радон (Rn).
Что делает инертные газы особенными и востребованными в различных областях науки и промышленности?
Инертные газы обладают высокой стабильностью и отсутствием химической активности. Они практически не взаимодействуют с другими веществами, что делает их особенно полезными в различных областях науки и промышленности. Например, инертные газы используются как защитная среда при сварке и пайке, для создания атмосферы чистоты в лабораториях и процессах производства полупроводников, а также в медицинской практике.
Какие элементы являются самыми "железными" в периодической таблице?
Самыми "железными" элементами в периодической таблице являются железо (Fe), кобальт (Co) и никель (Ni). Они относятся к д-блоку таблицы и обладают схожими химическими свойствами, такими как устойчивость окислительных состояний и способность образовывать комплексные соединения.
