Натрий и калий - это два щелочных металла, которые хорошо известны своими реактивными свойствами и способностью гореть при взаимодействии с воздухом. Оба вещества встречаются в природе в виде соединений, таких как соль и минералы.
Одним из главных химических свойств натрия и калия является их реакция с кислородом. При контакте с воздухом, щелочные металлы начинают гореть, образуя яркий пламя и высокую температуру. Этот процесс, известный как окисление, является очень быстрым и может привести к серьезным последствиям.
Горение натрия и калия не только очень яркое, но и опасное. При горении выделяются ядовитые газы, такие как оксиды азота и серы, которые могут представлять угрозу для здоровья человека. Кроме того, высокая температура горения может вызывать пожары и разрушение окружающих материалов.
Оба металла также обладают высокой реактивностью и способностью реагировать с другими веществами, такими как вода и кислоты. Эти реакции происходят быстро и могут привести к высвобождению большого количества энергии. Взаимодействие щелочных металлов с водой может вызывать взрывы и образование взрывоопасных газов.
Горение натрия и калия - это сложный процесс, связанный с высокой реактивностью металлов и их способностью реагировать с различными веществами. Правильное обращение с этими материалами требует особой осторожности, чтобы избежать опасных ситуаций и нанести вред окружающей среде.
Химические свойства щелочных металлов натрия и калия
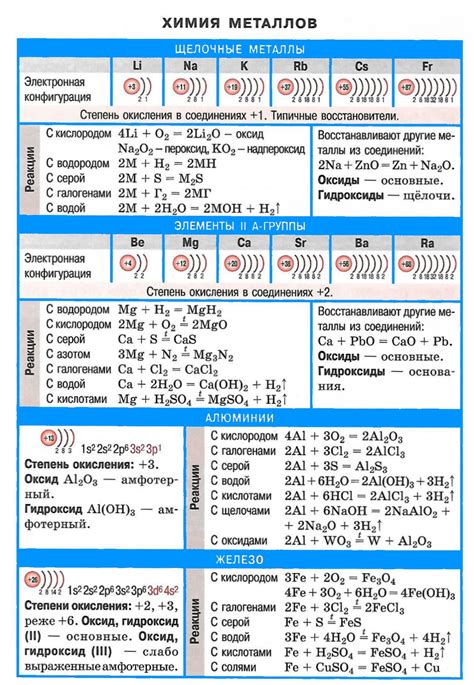
Щелочные металлы натрий и калий являются химически активными элементами, обладающими разнообразными свойствами. Натрий и калий образуют соединения с большинством элементов периодической системы, что делает их важными участниками химических реакций.
Одно из основных свойств щелочных металлов - их способность вступать в реакцию с кислородом из воздуха, образуя оксиды. Натрий горит желтоватым пламенем при контакте с воздухом, при этом образуется оксид натрия (Na2O). Калий горит с ярким фиолетовым пламенем, образуя оксид калия (K2O).
Еще одной характерной особенностью щелочных металлов является их реактивность с водой. При контакте с водой натрий и калий реагируют с образованием щелочного раствора, окислительно-восстановительных реакций и выделением водорода. Натрий реагирует более медленно, но равномерно, образуя щелочной раствор гидроксида натрия и выделяя водород. Калий реагирует более бурно, иногда даже с искрением, образуя щелочной раствор гидроксида калия и выделяя значительное количество водорода.
Еще одним интересным свойством щелочных металлов является их способность окрашивать пламя в яркие цвета. Натрий и калий являются одними из немногих элементов, которые при горении образуют яркие цвета. Натрий окрашивает пламя в желтый цвет, а калий - в фиолетовый.
Опасность горения щелочных металлов

Щелочные металлы, такие как натрий и калий, обладают высокой способностью реагировать с кислородом воздуха и взрываться. Горение щелочных металлов сопровождается ярким свечением и высокой температурой.
Горение натрия и калия происходит при контакте с воздухом или водой, из-за чего эти металлы являются чрезвычайно опасными. При горении маслообразные струи горящего металла выбрасываются вокруг, что может привести к возгоранию окружающих предметов.
Опасность горения щелочных металлов заключается также в выделении токсичных газов, таких как оксиды азота и оксиды калия. Эти газы могут повредить дыхательные пути и вызвать отравление.
Для предотвращения горения щелочных металлов необходимо соблюдать меры безопасности. Хранение натрия и калия должно производиться в специальных упаковках, избегая контакта с воздухом и влагой. При работе с этими металлами необходимо носить защитные очки, перчатки и специальную одежду.
В случае возгорания щелочных металлов необходимо немедленно принять меры по тушению. Для этого можно использовать специальные песочные или огнетушительные смеси, а также удалить источник кислорода и избегать контакта с водой.
Таким образом, горение щелочных металлов, в том числе натрия и калия, представляет собой серьезную опасность из-за высокой температуры, выделения токсичных газов и возможности взрыва. При работе с этими металлами необходимо соблюдать меры безопасности и быть готовым к незамедлительным действиям при возникновении возгорания.
Свойства натрия и его горение

Натрий – один из самых химически активных элементов химической группы щелочных металлов. Он представляет собой мягкий металлический элемент серебристо-серого цвета.
Натрий обладает высокой реакционной способностью. Он реагирует с водой, кислородом и другими химическими веществами. Когда натрий вступает в реакцию с водой, образуется щелочь и выделяется водородный газ.
Однако наиболее известное свойство натрия - его способность к горению. Горение натрия происходит при контакте с кислородом воздуха. При этом образуется яркий пламя желтого цвета. Пламя горения натрия имеет высокую температуру и может вызывать опасность при неправильном обращении.
Горение натрия можно контролировать, добавляя его постепенно в воду или использовать специальные глушители. Однако несоблюдение правил безопасности может привести к неожиданным последствиям. Важно помнить, что при контакте с водой или влагой натрий реагирует очень быстро и может вызвать возгорание, выбрасывая горящие частицы.
Свойства калия и его горение

Калий – это щелочной металл, который относится к химической группе алкалиевых металлов. Он обладает рядом уникальных свойств, которые делают его полезным в различных областях.
Одно из основных свойств калия – его активная реакция с водой. При соприкосновении калия с водой возникает сильное горение, сопровождающееся выбросом пламени и выделением водорода. Это свойство может стать опасным при неправильном обращении с калием, поэтому необходимо соблюдать особую осторожность при работе с ним.
Горение калия является разрушительным процессом, который протекает с высокой скоростью. Пламя при горении калия яркое и имеет фиолетовый оттенок. Возникающие при этом оксиды калия являются ядовитыми веществами и могут представлять опасность для здоровья человека.
Калий также обладает свойством взрываться при взаимодействии с некоторыми веществами, такими как хлор, бром и йод. При взаимодействии с этими веществами образуются сильно окисляющие соединения, которые могут привести к аварийной ситуации. Поэтому важно соблюдать особую предосторожность при работе с калием и его соединениями.
Вопрос-ответ

Какие химические свойства имеют натрий и калий?
Натрий (Na) и калий (K) относятся к группе щелочных металлов и обладают рядом общих химических свойств. Они оба очень активны и легко реагируют с водой, кислородом и многими другими веществами. Они обладают высокой электропроводностью и обычно находятся в состоянии ионов в растворе или соединениях. Кроме того, оба металла мягкие и образуют лёгкие сплавы с другими металлами.
Что происходит при горении натрия и калия?
При горении натрия и калия происходит быстрое окисление металла в присутствии кислорода. Это реакция, при которой образуется оксид натрия (Na2O) или оксид калия (K2O), а также выделяется большое количество тепла и света. Горение идёт с ярким пламенем, которое может быть опасно из-за высокой температуры и возможного выброса искр и пепла.
Какие опасности связаны с горением натрия и калия?
Горение натрия и калия может быть опасным из-за высокой температуры и интенсивности пламени. При горении эти металлы могут испаряться и выделяться в виде паров, что может привести к отравлению или образованию взрывоопасных смесей с воздухом. Кроме того, при взаимодействии с водой натрий и калий могут выделяться водород, который является горючим газом. Поэтому необходимо соблюдать осторожность при работе с этими металлами и применять соответствующие меры безопасности.
Какие другие свойства у натрия и калия, кроме горения?
Натрий и калий имеют множество других химических свойств и широко применяются в различных областях. Например, они используются для производства щелочей, таких как гидроксид натрия (NaOH) и гидроксид калия (КОН), которые используются в промышленности и быту. Они также являются важными компонентами питательных сред для растений и удобрений. Калий также играет важную роль в функционировании нервной системы и мышц организма.
