Соли тяжелых металлов обладают большим интересом для исследования и изучения их гидролитических свойств. Гидролиз солей тяжелых металлов — это процесс разложения соединений водой, в результате которого образуются ионы металла и оксидические или гидрооксидные ионы. Этот процесс происходит при взаимодействии растворов солей тяжелых металлов с водой или влагой в окружающей среде.
Гидролиз солей тяжелых металлов имеет ряд особенностей, связанных с особенностями структуры и электронной конфигурации металлических ионов. Так, в связи с высокой зарядностью ионов тяжелых металлов, гидролитические реакции на них обычно протекают с большей интенсивностью и медленнее, чем на ионах легких металлов. Это связано с высокой поляризующей способностью тяжелых металлов и возможностью образования многочисленных гидролитических продуктов.
Гидролиз солей тяжелых металлов может происходить по разным механизмам в зависимости от условий реакции. Важным фактором является pH раствора, так как он определяет ионизированность воды и степень гидролиза соли. Чем ниже pH, тем более гидролитически активными становятся ионы металла, что приводит к образованию гидрооксидных групп. При высоком pH возможно образование комплексных соединений и осаждение гидрооксидов металлов.
Изучение гидролиза солей тяжелых металлов имеет важное практическое значение. Это позволяет понять физико-химические свойства этих соединений, предсказать их поведение в различных окружающих условиях, а также разработать методы их нейтрализации или очистки растворов от ионов тяжелых металлов.
Гидролиз солей тяжелых металлов
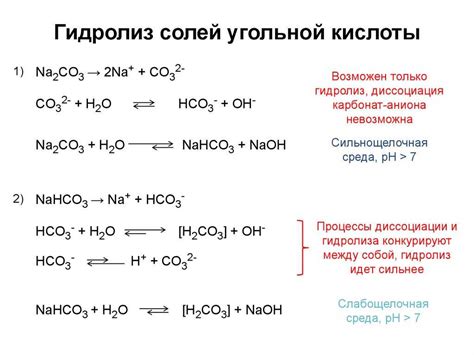
Гидролиз солей тяжелых металлов является химической реакцией, при которой соль взаимодействует с водой, приводя к образованию гидроксидов металлов и кислоты или основания. Особенностью гидролиза солей тяжелых металлов является их высокая токсичность и способность накапливаться в биологических системах.
Механизм гидролиза солей тяжелых металлов может быть различным и зависит от конкретного металла и его степени окисления. Некоторые тяжелые металлы, такие как свинец и кадмий, подвергаются гидролизу при нейтральных условиях, в то время как другие металлы требуют кислой или щелочной среды для гидролиза.
При гидролизе солей тяжелых металлов образующиеся гидроксиды металлов могут образовывать осадки, что приводит к их выпадению и осаждению на поверхности водных систем, таких как реки и озера. Это может привести к загрязнению воды и негативному влиянию на окружающую среду и здоровье людей.
Гидролиз солей тяжелых металлов является одной из основных причин загрязнения окружающей среды токсичными металлами. Поэтому необходимы меры по контролю и обработке сточных вод и отходов, содержащих соли тяжелых металлов, для минимизации их негативного воздействия на природу и человека.
Особенности гидролиза
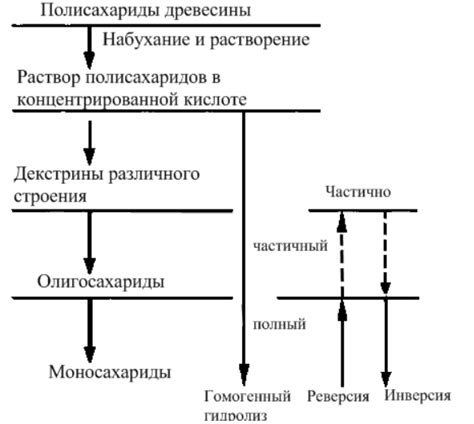
Гидролиз - это процесс, при котором ионы солей взаимодействуют с молекулами воды, приводя к образованию кислоты или щелочи. Гидролиз солей тяжелых металлов имеет свои особенности и механизмы.
Одной из особенностей гидролиза солей тяжелых металлов является образование нерастворимых осадков. Это происходит из-за того, что ионы тяжелых металлов обладают малой растворимостью в воде. При гидролизе эти ионы запутываются в структуре осадка, который мало подвижен и может образовывать настоящую преграду для дальнейших реакций.
Еще одной особенностью гидролиза солей тяжелых металлов является образование комплексных соединений. Тяжелые металлы обладают большим числом свободных d-электронов, которые могут образовывать особые структуры с водой и другими веществами. Это позволяет им образовывать стабильные комплексы, которые могут оказывать влияние на химические реакции и физические свойства окружающей среды.
Гидролиз солей тяжелых металлов также может приводить к образованию кислот или щелочей. Например, гидролиз солей свинца может образовывать растворимые кислые ионы, что может привести к изменению pH окружающей среды.
Итак, гидролиз солей тяжелых металлов имеет свои особенности, включая образование нерастворимых осадков, образование комплексных соединений и изменение pH окружающей среды. Эти особенности могут иметь важные последствия для окружающей среды и могут быть использованы в различных областях науки и технологии, таких как экология, металлургия и химическая промышленность.
Механизмы гидролиза

Гидролиз солей тяжелых металлов может происходить различными механизмами в зависимости от условий окружающей среды. Основными механизмами гидролиза являются протонный механизм и гидрокомплексный механизм.
Протонный механизм гидролиза возникает при нейтрализации солей тяжелых металлов сильными кислотами или щелочами. В этом случае происходит образование гидроксокомплексов металлов и положительно заряженных ионов металла. В процессе гидролиза протон из растворителя присоединяется к отрицательно заряженным группам, образуя кислоту.
Гидрокомплексный механизм гидролиза проявляется при взаимодействии солей тяжелых металлов с водой, содержащей заряженные гидроксокомплексы. В этом случае происходит образование гидроксидов металлов и ионов гидроксокомплексов. Гидроксиды металлов могут дальше реагировать и превращаться в осадки.
Также существуют и другие механизмы гидролиза солей тяжелых металлов, которые зависят от конкретной соли и условий реакции. Например, иногда механизм гидролиза может быть связан с образованием комплексов с другими веществами, такими как органические кислоты или аминокислоты.
Вопрос-ответ

Каковы особенности гидролиза солей тяжелых металлов?
Основной особенностью гидролиза солей тяжелых металлов является возможность образования гидроксо-комплексных и гидратных ионов, что приводит к изменению степени диссоциации соли в растворе. Это может сказаться на pH раствора, его окрашивании или осадке.
Каков механизм гидролиза солей тяжелых металлов?
Механизм гидролиза солей тяжелых металлов может быть различным в зависимости от конкретного металла. Однако, общей чертой является протекание реакции между металлическим и гидроксильным ионами. Это может привести к образованию гидроксо-комплексов или осадков в растворе. Также, влияние радиоактивных изотопов может изменить механизм гидролиза.
