Гидриды щелочных металлов – это химические соединения, в которых металлы образуют анионы с отрицательным зарядом, носящим имя гидрид и включающим атом водорода. Учитывая известные свойства водорода, гидриды щелочных металлов обладают рядом уникальных характеристик.
Особенностью гидридов щелочных металлов является их высокая реакционная способность. Это связано с тем, что атомы водорода в гидридах щелочных металлов легко отдают электроны, обладая значительной общей оболочкой вокруг ядра. Поэтому гидриды щелочных металлов реагируют с огнем и взрывчатыми веществами, а также активно вступают в реакции с водой.
Другой важной особенностью гидридов щелочных металлов является их способность к адсорбции (поглощению) водорода. Такие гидриды могут накапливать огромное количество молекул водорода в своих кристаллических решетках. Поэтому они могут использоваться для хранения и транспортировки водорода, который сейчас считается перспективным экологически чистым источником энергии.
В целом, гидриды щелочных металлов при обычных условиях обладают множеством интересных свойств, которые активно изучаются в научных исследованиях. Изучение этих соединений помогает расширить наши знания о химических и физических свойствах металлов и водорода, а также открыть новые перспективы их применения в различных областях науки и технологий.
Общая информация о гидридах щелочных металлов
Гидриды щелочных металлов представляют собой химические соединения, содержащие атомы водорода и атомы щелочных металлов. Гидриды обладают значительной реакционной активностью и разнообразными свойствами.
Одним из главных свойств гидридов щелочных металлов является их способность реагировать с водой, освобождая водород. Это свойство применяется в различных технологических процессах, например, при получении водорода для использования в качестве топлива.
Гидриды щелочных металлов также обладают высокой электроотрицательностью и способностью образовывать ионы в растворах. Эти свойства делают гидриды важными компонентами в различных химических реакциях и процессах, таких как катализ и формирование соединений с другими элементами.
Кроме того, гидриды щелочных металлов обладают высокой теплопроводностью и электропроводностью, что делает их полезными материалами для применения в различных областях, включая электронику и энергетику.
Определение и структура гидридов щелочных металлов

Гидриды щелочных металлов представляют собой химические соединения, в которых металл образует соединение с водородом. Гидриды щелочных металлов являются одними из наиболее известных и широко распространенных соединений щелочных металлов.
Структура гидридов щелочных металлов может быть разнообразной. В основном они образуют кристаллические соединения с ионными или ковалентными связями. При этом структура гидрида зависит от соотношения между металлом и водородом, а также от условий синтеза.
В гидридах щелочных металлов обычно преобладает ионная связь. Водородные ионы встраиваются в решетку металлического катиона, образуя структуру с координационными числами 6 или 12. Однако в некоторых гидридах может присутствовать и ковалентная связь, особенно при наличии высокого содержания водорода.
Структура гидридов щелочных металлов также может зависеть от размера металлического катиона. Например, величина ионного радиуса лиития приводит к образованию тетраэдрической решетки в его гидриде, тогда как величины ионных радиусов других щелочных металлов обеспечивают образование гидридов с кубической или гексагональной решеткой.
Физические свойства гидридов щелочных металлов
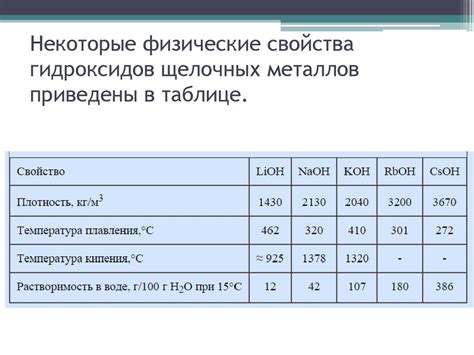
Гидриды щелочных металлов - это соединения металлов с водородом. Они обладают рядом характерных физических свойств, которые определяют их поведение при обычных условиях.
Прежде всего, гидриды щелочных металлов являются кристаллическими соединениями, образующимися при взаимодействии металлов с водородом. В зависимости от структуры кристаллической решетки, гидриды могут быть ионными или металлическими.
Одним из основных свойств гидридов щелочных металлов является их способность к диссоциации. Под воздействием влаги или тепла, гидриды распадаются на металл и молекулярный водород. Это позволяет использовать гидриды как источники водорода при его производстве и хранении.
Кроме того, гидриды щелочных металлов обладают высокой плотностью и малой массой. Эти свойства делают их привлекательными для использования в различных технологических процессах, включая производство батарей и легких конструкций.
Также стоит отметить, что гидриды щелочных металлов являются хорошими проводниками электричества. Это свойство позволяет использовать их в различных электрохимических процессах, например, в производстве водородных топливных элементов.
Химические свойства гидридов щелочных металлов

Гидриды щелочных металлов – это соединения, состоящие из атомов металла и атомов водорода. Они обладают рядом уникальных химических свойств, проявляющихся при обычных условиях.
Реактивность и химическая активность являются одними из основных свойств гидридов щелочных металлов. Они легко реагируют с водой, выделяясь в виде гидроксида металла и легко воспламеняются на воздухе. Реакция с водой происходит с выделением водорода и образованием щелочного гидроксида, которые в свою очередь могут реагировать с другими веществами.
Гидриды щелочных металлов обладают сильно основными свойствами. Они растворяются в воде с образованием гидроксидов, что является характерной особенностью этих соединений. При взаимодействии с кислотами образуются соли и выделяется водород. Реакция гидридов с кислородом приводит к образованию гидроксидов или смешанных гидроксидов.
Одно из особых свойств гидридов щелочных металлов – это их способность образования анионов гидрида. При взаимодействии с металлами образуются гидридные соединения, которые могут использоваться в неорганическом синтезе или в качестве реагентов при проведении химических реакций.
Применение гидридов щелочных металлов

Гидриды щелочных металлов - это соединения щелочных металлов с водородом. Они обладают рядом уникальных свойств, благодаря которым нашли широкое применение в различных областях.
Одним из основных применений гидридов щелочных металлов является их использование как источников водорода. Так, гидрид натрия (NaH) может служить источником водорода при его выделении в реакции с водой или другими соединениями. Это особенно актуально в случаях, когда требуется хранение и перенос водорода безопасным и эффективным способом.
Другим важным применением гидридов щелочных металлов является их использование в качестве катализаторов. Гидриды натрия, лития и калия активно применяются в гидрировании органических соединений, таких как алкены, кетоны и альдегиды. Эти реакции позволяют получать различные органические соединения, используемые в промышленности и научных исследованиях.
Гидриды щелочных металлов также находят применение в области энергетики и хранения энергии. Например, гидрид натрия обладает высокой энергоемкостью и может использоваться в батареях и аккумуляторах. Это позволяет значительно увеличить энергетическую плотность электрических устройств и улучшить их характеристики.
Таким образом, гидриды щелочных металлов имеют широкий спектр применения в различных областях, начиная от хранения и переноса водорода до использования в катализаторах и энергетике.
Вопрос-ответ

Какие свойства обладают гидриды щелочных металлов при обычных условиях?
Гидриды щелочных металлов при обычных условиях обладают следующими свойствами: они являются кристаллическими веществами, обладающими высоким плавлением и кипением, а также имеют низкую плотность. Они выступают в качестве сильных восстановителей и обладают высокой электропроводностью. Также они реагируют с водой, выделяя водородный газ.
Можно ли использовать гидриды щелочных металлов в качестве источника водорода?
Да, гидриды щелочных металлов можно использовать в качестве источника водорода. При взаимодействии с водой они выделяют водородный газ, который можно собирать и использовать. Этот процесс называется гидролизом. Однако для этого требуется специальное оборудование и условия, так как гидриды щелочных металлов очень реактивны и могут быть опасными.
Какие еще реакции могут происходить с гидридами щелочных металлов?
Гидриды щелочных металлов могут реагировать с кислородом, образуя оксиды металлов. Также они могут реагировать с различными кислотами и образовывать соли металлов. Некоторые гидриды щелочных металлов могут реагировать с аммиаком, образуя амиды металлов. Кроме того, они могут реагировать с некоторыми органическими соединениями, такими как спирты и алкены, образуя гидроксиды и гидроксилы.
Можно ли использовать гидриды щелочных металлов в химической промышленности?
Да, гидриды щелочных металлов могут быть использованы в химической промышленности. Они могут быть использованы в качестве катализаторов или восстановителей в различных химических реакциях. Они также могут быть использованы в процессе производства водорода или как источник водорода для различных химических процессов. Однако, так как гидриды щелочных металлов реактивны и опасны, их использование требует специальных мер предосторожности и контроля.
