Гидриды металлов - это соединения, в которых металл образует химическую связь с водородом. Водород имеет возможность образовывать разные степени окисления в гидридах. Степень окисления водорода в гидридах может изменяться от -1 до -3. Изменение степени окисления водорода в гидридах связано с различием в электроотрицательности металла и водорода.
Гидриды металлов с водородом в степени окисления -1 называются гидридами металлов первой группы. В этих соединениях водород обладает отрицательным зарядом и выступает в роли гидрид-иона. Например, натрий образует гидрид NaH, в котором водород имеет степень окисления -1.
Гидриды металлов с водородом в степени окисления -2 называются гидридами металлов второй группы. В этих соединениях водород образует две химически связи с металлом. Например, магний образует гидрид MgH₂, в котором водород имеет степень окисления -2.
Гидриды металлов с водородом в степени окисления -3 называются гидридами металлов третьей группы. В этих соединениях водород образует три химически связи с металлом. Например, бор образует гидрид BH₃, в котором водород имеет степень окисления -3.
Изучение степени окисления водорода в гидридах металлов позволяет лучше понять химические свойства и реакционную способность этих соединений. Это важно для разработки новых материалов и применения гидридов металлов в различных сферах, включая энергетику и катализ.
Гидриды металлов: присутствие водорода
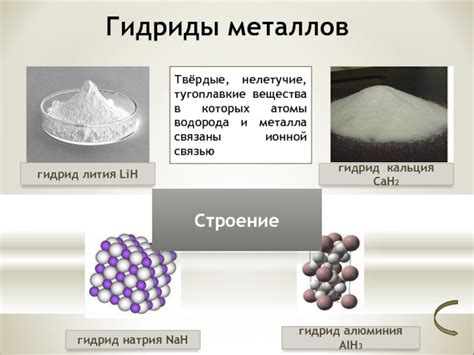
Гидриды металлов – это соединения, в которых металл образует химическую связь с атомами водорода. В таких соединениях водород имеет степень окисления -1. При этом водород может участвовать в различных типах химических связей с металлом.
Гидриды металлов обладают разнообразными физическими и химическими свойствами. Они могут быть как металлическими, так и не металлическими. Одним из примеров металлических гидридов является гидрид никеля, который обладает высокой электропроводностью и используется в технологии аккумуляторов.
Среди не металлических гидридов металлов можно выделить гидрид бора, который обладает высокой температурной стабильностью и применяется в ядерной энергетике. Водород, присутствующий в гидридах, может образовывать различные типы связей с металлом, такие как ионные, ковалентные или металлические.
Гидриды металлов находят широкое применение в различных отраслях промышленности. Они используются в качестве катализаторов, магнитных материалов, а также в процессе хранения и передачи водорода в водородной энергетике.
Степень окисления водорода в гидридах металлов

Гидриды металлов – это соединения металлов с водородом, которые обладают высокими теплофизическими и химическими свойствами. Вода – это самый известный гидрид, в котором водород обладает степенью окисления +1. Однако гидриды металлов могут иметь различные степени окисления водорода, которые варьируются в диапазоне от -1 до +1.
Гидриды с положительной степенью окисления водорода образуются при реакции между металлами и водородом. В этих соединениях водород передает электрон металлу и имеет положительный заряд. Примером может служить гидрид натрия NaH, в котором водород имеет +1 степень окисления.
Гидриды с отрицательной степенью окисления водорода образуются при реакции между металлами с отрицательной электроотрицательностью и водородом. В этих соединениях водород активно привлекает электроны, обладает отрицательным зарядом и имеет отрицательную степень окисления. Примером такого гидрида является гидрид алюминия AlH3, в котором водород имеет -1 степень окисления.
Изучение степени окисления водорода в гидридах металлов позволяет понять механизмы химических реакций, связанных с переносом электронов и изменением степени окисления. Это важно для понимания значимости гидридов металлов в каталитических процессах, энергетике, электрохимии и других областях науки и техники.
Вопрос-ответ

Какова структура гидридов металлов?
Гидриды металлов имеют сложную структуру, состоящую из металлических и водородных атомов. Обычно они образуют кристаллические решетки, в которых водородные атомы занимают определенные позиции.
Какие металлы образуют гидриды с различной степенью окисления водорода?
Водород может образовывать гидриды с большинством металлов, включая щелочные и щелочноземельные металлы, переходные металлы, лантаниды и актиниды. У гидридов металлов степень окисления водорода может быть различной, от -1 до -3.
Какие свойства имеют гидриды металлов?
Гидриды металлов обычно обладают хорошей проводимостью электричества и тепла, высокой плотностью и температурой плавления. Они также могут быть реактивными и образовывать взрывоопасные смеси с воздухом.
Как гидриды металлов используются в промышленности?
Гидриды металлов имеют широкое применение в промышленности. Например, они используются в водородных топливных элементах, в производстве лития-ионных аккумуляторов, в катализаторах химических реакций и в водородной переработке нефти и газа.
