Генетический ряд металлов – это систематическое упорядочивание химических элементов по возрастанию атомной массы, которое позволяет выявить и исследовать закономерности в их свойствах и химическом поведении. Каждый элемент в этом ряду имеет свои особенности и характеристики, которые определяют его место в таблице Менделеева.
Основные характеристики металлов в генетическом ряду – это их атомная масса, электронная конфигурация, металлические свойства (проводимость тепла и электричества, пластичность, шлифуемость, блеск), а также химическая активность, способность образовывать ионы и соединения.
Примеры элементов из генетического ряда металлов включают такие известные элементы, как литий (Li), натрий (Na), железо (Fe), серебро (Ag), золото (Au) и многие другие. Каждый из этих металлов имеет свои уникальные свойства и применения в различных отраслях промышленности, научных исследований и повседневной жизни.
Группа щелочных металлов

Щелочные металлы – это металлы, относящиеся к первой группе периодической системы химических элементов. Они включают в себя литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Щелочные металлы получили своё название из-за своей реактивности с водой, которая проявляется в образовании щелочных растворов.
Основные характеристики щелочных металлов:
- Атомный радиус: у щелочных металлов атомный радиус увеличивается по мере движения вниз по группе.
- Электроотрицательность: щелочные металлы обладают низкой электроотрицательностью.
- Плотность: плотность металлов также увеличивается по мере движения вниз по группе.
- Температура плавления и кипения: щелочные металлы имеют низкую температуру плавления и кипения.
- Химическая реактивность: щелочные металлы очень реактивны и легко реагируют с водой и кислородом.
Примеры использования щелочных металлов:
- Литий применяется в производстве аккумуляторов и лекарственных препаратов.
- Натрий используется в пищевой промышленности для приготовления пищевых добавок.
- Калий является необходимым элементом для растений и используется в сельском хозяйстве в качестве удобрения.
- Рубидий применяется в инфракрасной спектроскопии и ядерной медицине.
- Цезий используется в ионных двигателях и атомных часах.
Основные характеристики и примеры
Генетический ряд металлов - это систематическое расположение химических элементов в соответствии с их химическими свойствами и атомными структурами. В генетическом ряду можно выделить несколько основных характеристик:
- Постепенное изменение свойств: элементы ряда меняются постепенно, включая химические свойства, металлические свойства и периодический закон.
- Дополнение и преемственность: новые элементы появляются в ряду в результате дополнения предыдущих элементов, что свидетельствует о преемственности химических свойств.
- Стабильность и нестабильность: в генетическом ряду металлы могут быть стабильными или нестабильными в условиях окружающей среды.
Примеры металлов, расположенных в генетическом ряду, включают:
- Литий - легкий металл, химически активный, используется в производстве легких сплавов и аккумуляторов.
- Калий - щелочной металл, реактивный и легко окисляющийся, важный элемент для живых организмов.
- Железо - переходный металл, прочный и хорошо проводящий тепло и электричество, используется во многих отраслях промышленности.
- Медь - тяжелый металл, отличный проводник электричества, используется для изготовления проводов, монет и украшений.
Эти примеры демонстрируют разнообразие металлов, которые могут быть представлены в генетическом ряду, и их использование в различных сферах человеческой деятельности.
Группа щелочноземельных металлов

Щелочноземельные металлы – это группа элементов периодической системы, которая находится под группой щелочных металлов. Включает в себя металлы: магний, кальций, стронций, барий и радий.
Щелочноземельные металлы имеют характерные свойства, которые можно отнести к их электрохимической активности и реакционной способности. Они являются металлами мягкими, серыми, легкоплавкими и хорошо проводящими тепло и электричество.
Щелочноземельные металлы обладают низкой плотностью, что делает их легкими. Они реагируют с кислородом, нежелательными газами и водой, образуя оксиды, гидроксиды и гидраты. Эти металлы также способны образовывать ионы с положительным зарядом.
Щелочноземельные металлы широко используются в различных сферах. Например, магний используется в производстве легких сплавов, кальций широко применяется в строительстве и металлургии, стронций используется в производстве пиротехники, а радий в медицине.
Основные характеристики и примеры

Генетический ряд металлов - это упорядоченная последовательность химических элементов, отображающая их свойства и характеристики. Он основывается на расположении элементов в таблице Менделеева и представляет собой группы металлов, которые имеют схожие физические и химические свойства.
Примером генетического ряда металлов является ряд щелочных металлов, который включает литий, натрий, калий, рубидий, цезий и франций. Эти металлы характеризуются низким плотким и плавлением, высокой химической активностью и реакционной способностью с водой и кислородом.
Другим примером является ряд щелочноземельных металлов, включающий бериллий, магний, кальций, стронций, барий и радий. Эти металлы обладают высокой плотностью, ковкостью и проводимостью электричества. Они также реагируют с водой и кислородом, но менее активно, чем щелочные металлы.
Еще одним примером генетического ряда металлов являются переходные металлы, такие как железо, медь, цинк, никель, кобальт и многие другие. Эти металлы отличаются высокой прочностью, твердостью и устойчивостью к коррозии. Они широко используются в промышленности, электротехнике и строительстве.
Важно отметить, что генетический ряд металлов не является единственным способом классификации металлов, но он помогает понять основные характеристики элементов и их взаимосвязь.
Группа переходных металлов
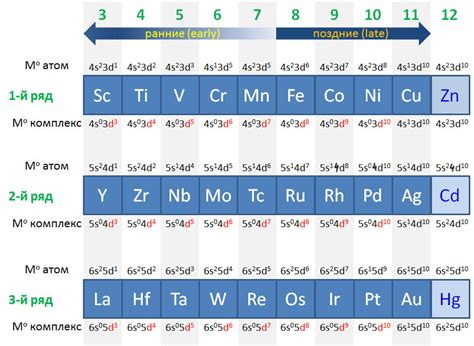
Группа переходных металлов включает элементы, расположенные в блоке d периодической таблицы химических элементов. Они представляют собой серию металлов, которые характеризуются особыми физическими и химическими свойствами.
Основные характеристики переходных металлов включают высокую теплопроводность, электропроводность и металлический блеск. Они обладают большим количеством свободных электронов, что делает их хорошими проводниками электричества и тепла.
Переходные металлы также обладают способностью образовывать соединения с различными степенями окисления, что делает их полезными во многих химических реакциях и в различных промышленных процессах.
Примеры переходных металлов включают железо, медь, цинк, никель и многие другие. Железо, например, широко используется в производстве стали, а медь является основным материалом для проводов и кабелей.
Таким образом, группа переходных металлов играет важную роль в нашей повседневной жизни и имеет широкий спектр применений в различных отраслях промышленности и науки.
Основные характеристики и примеры

Генетический ряд металлов представляет собой классификацию металлов по их химическим свойствам. Он основан на упорядочивании металлов в порядке увеличения их атомных номеров в периодической таблице элементов.
В генетическом ряду металлов можно выделить несколько основных характеристик:
- Атомные свойства: каждый металл в ряду имеет определенное число электронов в своей внешней электронной оболочке, что сказывается на его химических свойствах и реакциях.
- Физические свойства: металлы в ряду обладают высокой теплопроводностью и электропроводностью, а также способностью к деформации без разрушения.
- Химические свойства: с ростом атомного номера в ряду увеличивается химическая активность металлов, что проявляется в их способности образовывать ионы положительного заряда и реагировать с другими веществами.
Примеры металлов, входящих в генетический ряд, включают:
- Литий (Li) - металл с атомным номером 3, обладающий низкой плотностью и большой способностью к образованию ионов.
- Цинк (Zn) - металл с атомным номером 30, химически активный элемент, используемый в промышленности и в медицине.
- Уран (U) - металл с атомным номером 92, известный своей радиоактивностью и использованием в ядерной энергетике.
Таким образом, генетический ряд металлов позволяет систематизировать и классифицировать этот разнообразный класс элементов в соответствии с их химическими и физическими свойствами.
Группа благородных металлов

Благородные металлы относятся к группе химических элементов с высокой степенью химической инертности и стабильности. Они обладают прекрасными электрическими и термическими свойствами, а также блестящим внешним видом. К числу благородных металлов относятся платина, золото, родий, иридий, ослабневолость и их группы.
Платина - это благородный металл, который обладает высокой плотностью и устойчивостью к коррозии. Он используется в ювелирном и промышленном производстве, а также в катализаторах и электродных системах.
Золото - самый известный из благородных металлов. Оно обладает высокой проводимостью электричества и тепла, а также является устойчивым к коррозии и окислению. Золото широко используется в ювелирном и электронном производстве.
Родий - благородный металл с высокой плотностью и температурой плавления. Он обладает отличными каталитическими свойствами и широко используется в производстве автомобилей, солнечных батарей и химической промышленности.
Иридий - один из самых плотных и твердых металлов в мире. Он обладает высокой коррозионной стойкостью и устойчивостью к высоким температурам. Иридий используется в производстве электроники, зубных протезов, лабораторного исследования и других областях.
Ослаблевольность - это благородный металл с высокой плотностью и стабильностью. Он обладает высоким устойчивым к коррозии и устойчивостью к высоким температурам. Ослаблевольность применяется в промышленности для производства электрических контактов, электродных систем и катализаторов.
Вопрос-ответ

Какие основные характеристики генетического ряда металлов?
Основные характеристики генетического ряда металлов включают в себя понятия, такие как атомный радиус, ионный радиус, электроотрицательность, электропроводность, температура плавления и кипения, а также молекулярная форма. Эти характеристики определяют поведение металлов в химических реакциях и их способность образовывать сплавы с другими металлами.
Какие примеры можно привести в качестве иллюстрации генетического ряда металлов?
Примеры металлов, входящих в генетический ряд, включают в себя литий, натрий, калий, магний, алюминий, кальций, железо, никель, медь, серебро и золото. Эти металлы характеризуются определенными химическими и физическими свойствами, которые делают их уникальными и полезными для различных промышленных и научных приложений.
Каково значение атомного радиуса ионного радиуса в генетическом ряду металлов?
Атомный радиус ионного радиус металлов определяют их размер и способность образовывать связи с другими атомами. Металлы с большими атомными и ионными радиусами, такими как литий и натрий, имеют больше свободного пространства для формирования связей с другими атомами. С другой стороны, металлы с меньшими радиусами, такие как железо и серебро, имеют более компактные структуры и образуют более прочные и стабильные связи.
Какова роль электроотрицательности в генетическом ряду металлов?
Электроотрицательность металлов определяет их способность привлекать электроны при образовании химических связей. Металлы с низкой электроотрицательностью, такие как натрий и калий, имеют большую склонность отдавать электроны и образовывать положительно заряженные ионы. С другой стороны, металлы с высокой электроотрицательностью, такие как кислород и штатин, имеют большую способность привлекать электроны и образовывать отрицательно заряженные ионы.
