Фтор – это элемент химического периодического стола, который долгое время считался щелочным металлом. В научной литературе можно встретить упоминания о том, что фтор обладает рядом характеристик, типичных для щелочных металлов. Однако, существуют и аргументы в пользу того, что фтор не является щелочным металлом.
Фтор, симбол F, является самым электроотрицательным элементом в периодической системе Менделеева. Он образует соединения с практически всеми другими элементами, включая металлы. Это свойство делает его похожим на щелочные металлы, которые тоже активно взаимодействуют с другими веществами.
Однако, физические и химические свойства фтора отличают его от щелочных металлов. Например, фтор образует газообразные соединения при комнатной температуре, в то время как щелочные металлы обладают металлическим блеском и образуют кристаллические структуры. Кроме того, фтор не образует гидроксиды, а щелочные металлы образуют гидроксиды, растворимые в воде.
Таким образом, хотя фтор обладает некоторыми схожими свойствами с щелочными металлами, его отличительные черты делают его не полностью классифицированным как таковой.
Не смотря на дебаты о классификации фтора, его широкое применение в различных областях, таких как производство алюминия, стекла, и даже в медицинских целях, не вызывает сомнений. Фтор является важным элементом в современной промышленности и науке, и его свойства продолжают быть предметом исследований и дискуссий.
Фтор: химический элемент или разрыватель связей?
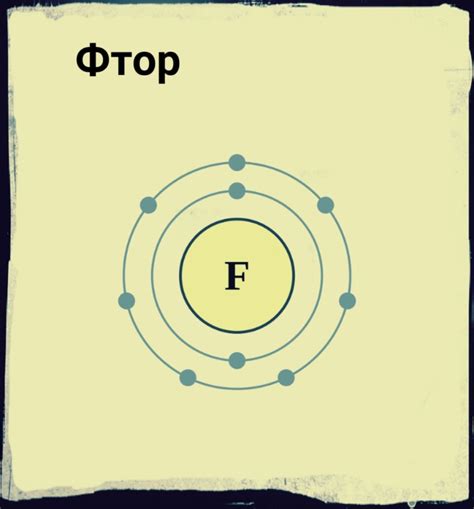
Фтор – галогенный химический элемент с атомным номером 9 и символом F. Он является самым электроотрицательным и реактивным химическим элементом из всех известных. Согласно его электроотрицательности, фтор обладает способностью эффективно притягивать электроны и образовывать ионные связи с другими элементами.
Фтор также известен своей способностью разрывать химические связи. Благодаря своей электроотрицательности и активности, фтор формирует очень сильные химические связи, особенно со свободными электронами. Это позволяет ему разрывать связи в молекулах с другими элементами, такими как кислород, углерод и водород. Таким образом, фтор способен разъединять множество химических соединений и оказывать разрушительное влияние на молекулярные структуры.
В природе фтор встречается в виде соединений, таких как фториды, которые образуются путем реакции фтора с другими элементами. Фториды имеют важное значение для здоровья человека и животных: фтор, добавляемый в питьевую воду и зубные пасты, способствует укреплению эмали зубов и предотвращению кариеса.
Вместе с тем, фтор является одним из самых ядовитых химических элементов. При попадании в организм, фтор может вызвать тяжелое отравление, повреждение органов и даже летальный исход. Поэтому необходимо соблюдать осторожность при работе с этим элементом и соблюдать соответствующие меры безопасности.
Существующие мнения о природе фтора:

Фтор (F) является химическим элементом, который иногда представляется как щелочной металл. Однако существует расхождение во мнениях по этому вопросу.
Одна из точек зрения заключается в том, что фтор является природным щелочным металлом, так как он принадлежит к первой группе периодической системы и имеет всего один электрон во внешней оболочке, что делает его аналогичным другим щелочным металлам, таким как литий, натрий и калий. Этот взгляд подтверждается также тем, что фтор образует гидриды, подобные гидридам щелочных металлов.
Однако существует и обратная точка зрения, согласно которой фтор не является щелочным металлом. Этот аргумент основан на том, что фтор имеет другие химические свойства, которые не характерны для щелочных металлов. Например, фтор обладает высокой электроотрицательностью и является самым активным элементом из всех химических элементов. Кроме того, фтор не образует соль с водой, которая является характеристикой щелочных металлов.
В целом, вопрос о характере фтора остается открытым и требует дальнейших исследований для достижения консенсуса. Возможно, в будущем будет разработана более точная классификация этого элемента, которая учитывает все его химические свойства и отношения с другими элементами.
Химические свойства фтора:
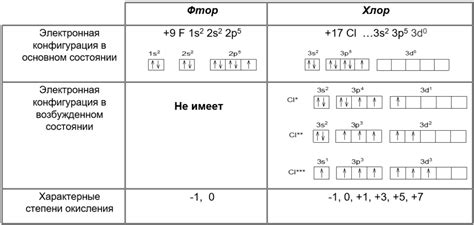
Фтор - самый электроотрицательный из всех элементов в периодической системе, что делает его очень реактивным химическим веществом. Он обладает способностью образовывать многочисленные химические соединения с другими элементами.
Основным и наиболее известным химическим свойством фтора является его высокая активность в реакциях с металлами. Фтор обладает способностью окислять металлы, образуя с ними соединения, называемые фторидами. Некоторые фториды металлов обладают высоким температурным стойкостью, являются суперкондукторами или имеют другие полезные свойства.
Фтор также может образовывать соединения с неметаллами, такими как кислород, сера и хлор. Например, фтор образует фторид кислорода (O2F2), который обладает свойствами сильного окислителя и может применяться в качестве локального анестетика.
Кроме того, фтор обладает способностью образовывать соединения с водородом. Например, фтор вступает в реакцию с водородом и образует газообразный гидрофторид (HF), который является кислотой и активным растворителем для некоторых веществ. Гидрофторид применяется в промышленности для производства различных химических соединений и материалов.
Применение фтора в различных отраслях:
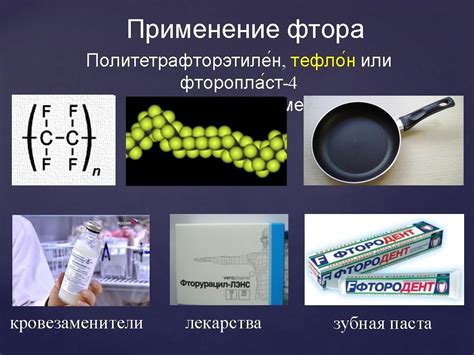
Нефтехимическая промышленность: Фтор используется в производстве различных органических соединений, таких как хлорфторсодержащие полимеры и резины, которые широко применяются в процессах бурения нефтяных скважин и производства нефтехимических продуктов.
Электроника: Использование фтора в электронике является важным компонентом для производства полупроводников, таких как кремний, галлий и индий, которые являются основой для создания различных электронных устройств, включая компьютеры, сотовые телефоны и телевизоры.
Металлургия: Фтор используется в металлургической отрасли для очистки и обработки металлов, таких как алюминий и уран, что позволяет улучшить их физические свойства и качество. Кроме того, фтор также используется для производства сплавов, которые необходимы для производства авиационных и автомобильных деталей.
Строительство: В строительной отрасли фтор применяется для создания специальных жидкостей и покрытий, которые улучшают защитные свойства материалов и поверхностей от воздействия агрессивных сред или разрушающих факторов, таких как коррозия и истирание.
Здравоохранение: Фтор применяется в зубных пастах и ополаскивателях для зубов, так как он способствует защите зубов от кариеса и укрепляет эмаль. Также, фтор используется для производства фармацевтических препаратов, включая антибиотики и противоопухолевые средства.
Пищевая промышленность: Фтор используется в пищевой промышленности для производства различных пищевых добавок, таких как консерванты и антиоксиданты, которые увеличивают срок годности продуктов и сохраняют их свежесть и качество. Также, фтор используется в производстве изделий из алюминия, которые широко используются в упаковке пищевых продуктов.
Разрушительная сторона фтора:

Фтор, несомненно, является одним из самых опасных химических элементов. Его разрушительное воздействие на живые организмы и материалы широко известно. Воздействие фтора на организм может привести к серьезным заболеваниям и даже смерти. Этот элемент сильно коррозирует металлы, вызывает выщелочивание стекла и расщепление древесины. Это делает его чрезвычайно опасным для окружающей среды и промышленного оборудования.
Насколько опасен фтор для здоровья человека? В больших дозах этот элемент может вызывать ожоги, повреждение дыхательных путей, проблемы с пищеварением и нервной системой. Длительное воздействие фтора может привести к хроническим заболеваниям, таким как остеофлюороз или фтороз зубов. Даже небольшое содержание фтора в воде, превышающее допустимую норму, может нанести непоправимый вред здоровью.
Кроме того, фтор имеет разрушительное воздействие на материалы. Он может разъедать металлы, такие как алюминий, сталь и свинец. Контакт с фтором может привести к образованию фторидных газов, которые являются высоко токсичными. Фтор также является сильным окислителем, способным вызвать воспламенение и взрывы при контакте с органическими веществами.
Взаимодействие фтора с обычными предметами быта также может привести к разрушению. Например, области с высоким содержанием фтора в воде могут вызывать коррозию сантехнических труб и оборудования. Украшения из металла, покрытые фтором, могут потерять свой блеск и стать непригодными для использования. Таким образом, разрушительная сторона фтора неизбежно влияет как на наше здоровье, так и на окружающую среду.
Будущее исследований фтора:
Фтор - уникальный элемент, который имеет много потенциальных применений в различных областях науки и технологий. Будущее исследований фтора обещает открыть новые горизонты в разработке новых материалов, применении в электронике и медицине, а также в сфере экологии и энергетики.
Одной из перспективных областей исследований фтора является его использование в разработке новых материалов с высокими техническими характеристиками. Фториды металлов например, могут использоваться в качестве оптических покрытий, способных повысить прочность и устойчивость материалов к коррозии. Исследования в этой области могут помочь создать новые легкие и прочные материалы для авиационной и космической промышленности.
Еще одной интересной областью исследования фтора является его применение в электронике. Фториды металлов могут быть использованы в качестве полупроводниковых материалов, способных значительно повысить эффективность электронных устройств. Такие материалы могут быть использованы в разработке новых плоских дисплеев, устройств хранения данных и солнечных батарей.
Еще одним направлением исследований фтора является его применение в медицине. Исследования показывают, что фтор может быть полезен в борьбе с бактериальными инфекциями и кариесом. Фториды могут быть использованы в разработке новых антимикробных препаратов и композитных материалов для стоматологии. Также фтор может быть полезен в области онкологии, где он может быть использован в качестве контрастного вещества для диагностики опухолей.
Кроме того, фтор имеет большое значение в сфере экологии и энергетики. Исследования показывают, что фтор может быть использован в качестве альтернативного источника энергии. Он может быть использован в солнечных батареях, беспроводной передаче энергии и электроаккумуляторах. Исследования в этой области могут помочь разработать новые источники энергии, которые будут экологически безопасными и эффективными.
Вопрос-ответ

Является ли фтор щелочным металлом?
Нет, фтор не является щелочным металлом. Щелочные металлы - это элементы первой группы периодической системы, такие как литий, натрий или калий. Фтор относится к галогенам, которые находятся в седьмой группе. Они имеют отличные свойства и относятся к неметаллам.
Какие свойства фтора говорят о его неметаллическом характере?
Фтор обладает рядом свойств, которые указывают на его неметаллический характер. Во-первых, фтор является одним из самых реактивных и химически активных элементов. Он способен реагировать с многими другими веществами и образовывать соединения. Во-вторых, фтор обладает высокой электроотрицательностью, что делает его сильным окислителем. Кроме того, у фтора нет металлического блеска и он не проводит электричество в твердом состоянии.
Какие еще элементы относятся к группе галогенов, подобно фтору?
В группу галогенов, подобно фтору, входят три других элемента: хлор, бром и иод. Они также обладают неметаллическим характером. Хлор находится во второй группе галогенов, бром - в третьей, а иод - в четвертой. Каждый из этих элементов имеет свои уникальные свойства, но все они обладают сходными химическими и физическими характеристиками, объединенными общим названием "галогены".
