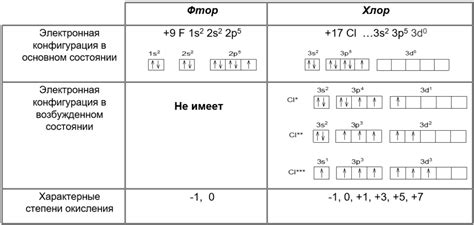
Фтор - химический элемент с атомным номером 9 и символом F. Он относится к галогенам и является самым электроотрицательным из всех элементов. Фтор является газообразным при нормальных условиях и обладает ярко-желтым цветом.
Свойства фтора делают его уникальным элементом в химии. Он обладает очень высокой реакционной способностью и образует со многими элементами стабильные химические соединения. Фтор обычно не образует металлические связи, что является характеристикой неметалла.
Однако, вещества, содержащие фтор, могут обладать как металлическими, так и неметаллическими свойствами. Например, фторид кальция (CaF2) обладает кристаллической структурой и имеет металлический оттенок, но при этом обладает химической активностью, характерной для неметаллов.
Таким образом, химические свойства фтора позволяют считать его неметаллом. Однако, его способность образовывать металлические соединения делает его уникальным и интересным элементом в периодической системе.
Свойства фтора

Фтор - химический элемент периодической системы с атомным номером 9. Он является самым электроотрицательным из всех элементов. Фтор имеет высокую реакционную активность и образует соединения с многими другими элементами.
Одним из основных свойств фтора является его способность к химическому соединению с другими элементами, образуя с ними фториды. Фториды обладают высокой термической и химической стабильностью.
Фтор обладает высокими физическими свойствами. Температура кипения фтора составляет 188,12 градусов Цельсия, а температура плавления - 53,48 градусов Цельсия. Он является единственным элементом, который способен образовывать такой низкотемпературный газ как фтороводород (HF).
Фтор является мощным окислителем. Он образует взрывчатые соединения с некоторыми веществами, такими как водород, углерод, сера и металлы. Из-за его реакционной активности, фтор встречается главным образом в виде соединений, таких как фторид калия, фторид натрия и фторид кальция.
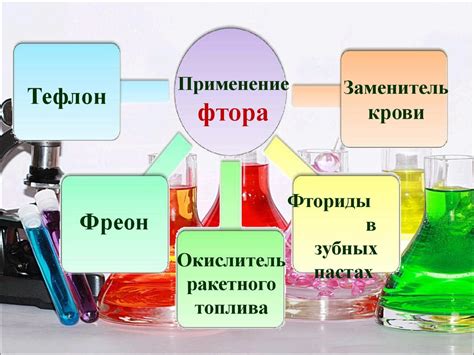
Фтор также обладает уникальными электронными свойствами. Он является сильным поглотителем электронов и может вытеснить другие элементы из их соединений. Это свойство делает его необходимым в производстве фторированных органических соединений, таких как фреоны и тефлон.
Распространение фтора

Фтор является одним из самых распространенных элементов на Земле и присутствует во множестве природных и искусственных материалов. Он широко распространен в земной коре и составляет примерно 0,05% ее массы.
Основным источником фтора являются минералы флюорит, фосфаты и плавиковые концентраты, которые содержат значительные количества этого элемента. Флюорит является наиболее распространенным минералом, из которого извлекается фтор. В мире добывается более 4 миллионов тонн флюорита ежегодно.
Фтор также присутствует в природных источниках воды, поскольку растворимые соединения фтора могут находиться в водах поверхностных и подземных источников. Высокие концентрации фторида в воде наблюдаются в некоторых районах, таких как плато Тихого океана и южное побережье США.
Фтор также широко используется в разных отраслях промышленности и научных исследованиях. Он применяется в производстве различных химических соединений, стекла, керамики, электроизоляционных материалов, медицинских препаратов и многих других продуктов. Фторсодержащие вещества также применяются в процессе плавления металлов, таких как алюминий, магний и титан, для удаления примесей и улучшения их качества.
Физические характеристики фтора

Фтор (F) - это химический элемент с атомным номером 9 и символом F в периодической системе элементов. Он является самым электроотрицательным элементом и принадлежит к группе галогенов.
Фтор является неметаллом и находится в газообразном состоянии при комнатной температуре и давлении. Он обладает ярко-желтой окраской и имеет характерный запах. Фтор - самый активный элемент из всех химических элементов и образует соединения со многими другими элементами.
Основные физические характеристики фтора:
- Температура плавления: фтор плавится при температуре -219 градусов Цельсия (-362 градуса Фаренгейта).
- Температура кипения: фтор кипит при температуре -188 градусов Цельсия (-306 градусов Фаренгейта).
- Плотность: плотность фтора составляет 1,7 г/см³.
- Теплоемкость: теплоемкость фтора равна 825 Дж/кг·К.
Фтор имеет высокую реактивность и реагирует со многими веществами, включая металлы, органические соединения и другие неметаллы. Благодаря своей активности, фтор используется в различных промышленных процессах, включая производство аллюминия, хлора и фторированных органических соединений.
Кроме того, в природе фтор находится главным образом в виде минерала флюорита (состоит из кальция и фтора) и флуорапатита (минерал, содержащий фтор, кальций и фосфор).
Химические свойства фтора
Фтор - это химический элемент, который обладает уникальными свойствами. Он является самым электроотрицательным из всех элементов и обладает большими возможностями для образования химических связей.
Взаимодействие фтора с другими веществами может быть очень реактивным и энергичным. Фтор легко реагирует с многими элементами, включая металлы, неметаллы и даже галогены. Он образует с ними различные соединения.
Одним из наиболее известных свойств фтора является его способность агрессивно реагировать с водой. Под влиянием фтора происходит окисление воды, а также происходит образование фтороводорода.
Фтор также обладает способностью образовывать многие стабильные химические связи, что делает его ценным элементом во многих областях науки и промышленности. Он применяется в производстве полимеров, пластиков, электроники, косметических и фармацевтических продуктов.
Кроме того, фтор имеет высокую токсичность и может вызывать ожоги и отравления при неправильном обращении с ним. Поэтому необходимо соблюдать осторожность при работе с фтором и его соединениями.
Реакции фтора с другими элементами

Фтор – один из самых активных элементов в периодической таблице, что объясняется его высокой электроотрицательностью. Он способен образовывать соединения с практически всеми элементами, включая металлы и неметаллы.
С металлами фтор образует сольфида. В результате реакции фтора с алюминием, например, образуется алюминийфторид AlF3. Это вещество имеет высокую термическую стабильность и используется в производстве керамики, стекла и электролитического алюминия.
С неметаллами фтор также образует соединения. Например, при взаимодействии с кислородом образуется химически активный фторид кислорода OF2. Данный соединение широко используется в химической промышленности в качестве окислителя и фторирующего агента.
Фтор также реагирует с галогенами (хлором, бромом, йодом) и образует галогенфториды. Например, реакция с хлором может привести к образованию пяти хлоридов: ClF, ClF3, ClF5, ClF7, Cl2F2.
Таким образом, реакции фтора с другими элементами являются важной частью его химических свойств. Они позволяют производить широкий спектр соединений, которые находят применение в различных отраслях промышленности и науки.
Использование фтора в промышленности
Фтор – это химический элемент с атомным номером 9 и символом F в периодической системе элементов. Благодаря своим уникальным свойствам, фтор нашел широкое применение в различных отраслях промышленности.
Электроника и полупроводники: Фтор используется в процессе производства полупроводников, таких как солнечные батареи, транзисторы и диоды. Фториды металлов, такие как фторид ксенона и фторид криптона, применяются в процессе создания лазерных источников света.
Авиационная и космическая промышленность: Фторированные полимеры, такие как политетрафторэтилен (ПТФЭ), известный также как тефлон, широко применяются в авиации и космической промышленности. Они непламеняемы, обладают высокой химической стойкостью и низким коэффициентом трения.
Металлургия: Фтор используется для очистки и дефторирования металлов, таких как алюминий и уран, в процессе их производства. Фторированные соединения также используются для создания низкотемпературных сплавов, которые обладают высокой стойкостью к коррозии и окислению.
Химическая промышленность: Фтор используется в производстве химических реагентов, таких как фториды, фторированные органические соединения и кислоты. Он также применяется в процессе полимеризации и фторирования пластмасс.
Стекольная промышленность: Фтор используется для создания флюсов – веществ, которые помогают уменьшить точку плавления стекла и облегчают его обработку. Он также применяется для удаления пузырьков и дефектов на поверхности стекла.
Все эти примеры говорят о широком спектре применения фтора в промышленности. Уникальные свойства этого химического элемента делают его необходимым компонентом в процессах производства различных продуктов и материалов, обеспечивая им высокую эффективность и стабильность.
Вредность и полезность фтора
Фтор является важным элементом, который может оказывать и положительное, и отрицательное влияние на организм человека.
С одной стороны, фтор играет важную роль в формировании и укреплении зубной эмали, что делает его необходимым для поддержания здоровья зубов. Большинство зубных паст содержат фтор, который помогает предотвратить разрушение зубов и появление кариеса. Кроме того, фтор используется в процессефторирования воды, что позволяет снизить риск заболевания зубов у населения.
С другой стороны, фтор может приводить к различным проблемам со здоровьем, особенно при превышении его допустимой концентрации. Постоянное употребление в больших количествах фтора может вызывать флюороз зубов, который проявляется в виде желтых или коричневых пятен. Кроме того, фтор может негативно влиять на функцию щитовидной железы и оказывать токсическое действие на организм.
Важно отметить, что оптимальный уровень фтора в организме должен быть соблюден, чтобы избежать его негативного воздействия. Установленные нормы потребления фтора регулируются законодательными актами каждой страны. Также следует обратить внимание на концентрацию фтора в питьевой воде и продуктах, чтобы избежать его избыточного употребления.
Итак, фтор является как полезным, так и вредным элементом для организма. Следует соблюдать оптимальные нормы его потребления, чтобы получить пользу от его полезных свойств и избежать негативных последствий для здоровья.
Вопрос-ответ

Фтор является металлом или неметаллом?
Фтор относится к классу веществ, которые называются галогены, и является неметаллом.
Металлический ли характер у фтора?
Нет, фтор не обладает металлическими свойствами, поскольку он является неметаллом.
Какие свойства фтора определяют его как неметалл?
Фтор обладает характерными неметаллическими свойствами, такими как низкая плотность, хрупкость, слабая электропроводность и отсутствие металлического блеска.
Может ли фтор встречаться в металлическом состоянии?
Нет, фтор не может существовать в металлическом состоянии. При комнатной температуре фтор находится в виде газа.
Какие элементы могут считаться металлами в таблице химических элементов?
Металлами в таблице химических элементов считаются элементы, находящиеся слева от линии, которая проходит через группы 13-16. Это включает такие элементы, как натрий, алюминий, железо, медь и т.д.
