Фосфаты металлов являются важным классом химических соединений, которые широко используются в различных областях промышленности и науки. В частности, фосфаты натрия, кальция и алюминия с группой атомов остатка H3PO4 обладают особыми свойствами и находят применение в различных неорганических и органических реакциях.
Формула фосфата натрия с группой атомов остатка H3PO4 выглядит следующим образом: NaH2PO4. Это соединение представляет собой белые кристаллы, хорошо растворимые в воде. Фосфат натрия используется в производстве удобрений, а также играет важную роль в пищевой промышленности как регулятор кислотности и стабилизатор для молочных продуктов, напитков и кондитерских изделий.
Фосфат кальция с группой атомов остатка H3PO4 обозначается формулой CaHPO4. Это белый кристаллический порошок, нерастворимый в воде. Фосфат кальция является ключевым компонентом костей и зубов, поэтому широко используется в фармацевтической промышленности для производства добавок к пище, витаминно-минеральных комплексов и других продуктов, способствующих здоровью костной ткани.
Фосфат алюминия с группой атомов остатка H3PO4 обозначается формулой Al(H2PO4)3. Это белый порошок, растворимый в воде. Фосфат алюминия играет значительную роль в процессах обработки воды и сточных вод, так как обладает сорбционными свойствами и способен удалять из раствора нежелательные примеси и загрязнители. Кроме того, фосфат алюминия широко используется в производстве лакокрасочных материалов, керамики и стекла.
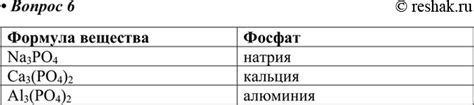
Формулы фосфатов металлов

Фосфаты металлов – это химические соединения, состоящие из атомов металла и группы атомов остатка фосфорной кислоты (H3PO4). Они имеют различные формулы в зависимости от металла и количества атомов фосфора в молекуле.
Фосфат натрия (Na3PO4) представляет собой соль, образующую бесцветные кристаллы. Он обладает высокой растворимостью в воде и является прекурсором для получения других фосфатов металлов.
Фосфат кальция (Ca3(PO4)2) – это основной компонент костей и зубов. Он образует твердые кристаллы и плохо растворяется в воде. Фосфат кальция также используется в качестве пищевой добавки, а также в производстве удобрений и фармацевтических препаратов.
Фосфат алюминия (AlPO4) – это соединение, обладающее различными полиморфными модификациями. Оно применяется в качестве катализатора в различных химических реакциях, а также в производстве огнеупорных материалов и керамики.
Формулы фосфатов металлов могут варьироваться в зависимости от условий синтеза и типа используемых реагентов. Эти соединения имеют широкий спектр применений в различных отраслях промышленности и науки.
Фосфат натрия и его формула
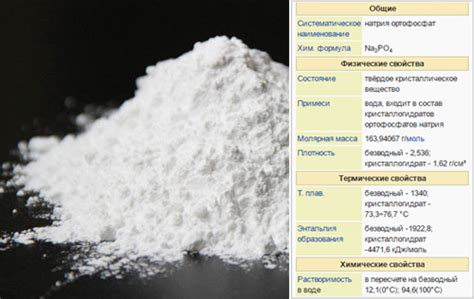
Фосфат натрия - неорганическое соединение, обладающее формулой Na3PO4. Это соль, образованная из металла натрия (Na) и кислоты фосфорной (H3PO4). Фосфат натрия широко применяется в различных отраслях промышленности и научных исследованиях.
Свойства:
- Фосфат натрия образует бесцветные кристаллы, легко растворяющиеся в воде.
- Он обладает слабо щелочными свойствами и может вызывать раздражение на коже и слизистых оболочках.
- Фосфат натрия является стабильным соединением и не образует взрывоопасных смесей с другими веществами.
Применение:
- Фосфат натрия используется в пищевой промышленности в качестве стабилизатора и консерванта.
- Он применяется в качестве добавки в моющих средствах для удаления жира и загрязнений.
- Фосфат натрия играет важную роль в процессе коагуляции и флокуляции при очистке воды.
- Он используется в медицине для приготовления различных лекарственных препаратов.
Фосфат натрия является важным соединением для многих отраслей и имеет широкий спектр применения благодаря своим свойствам и химической стабильности.
Фосфат кальция и его состав

Фосфат кальция – это соединение, образующееся при реакции между кальциевыми соединениями и фосфорной кислотой (H3PO4). Из-за своей высокой растворимости, фосфат кальция широко используется в медицине, пищевой промышленности и сельском хозяйстве.
Состав фосфата кальция зависит от его формы. Существуют две основные формы фосфата кальция: двухосновный гидроксиапатит (Ca5(PO4)3OH) и трехосновный гидроксиапатит (Ca10(PO4)6(OH)2).
Двухосновный гидроксиапатит – это основной минерал, образующий зубы и кости. Этот соединение имеет симметричную кристаллическую структуру и высокую устойчивость. Гидроксиапатит является важным для поддержания костной ткани и стимуляции роста костей.
Трехосновный гидроксиапатит обладает более сложной структурой, чем двухосновный гидроксиапатит. Он используется в медицине для создания имплантатов и зубных наполнителей. Трехосновный гидроксиапатит обеспечивает стабильность и прочность искусственных зубов и костных имплантатов.
Формула фосфата алюминия
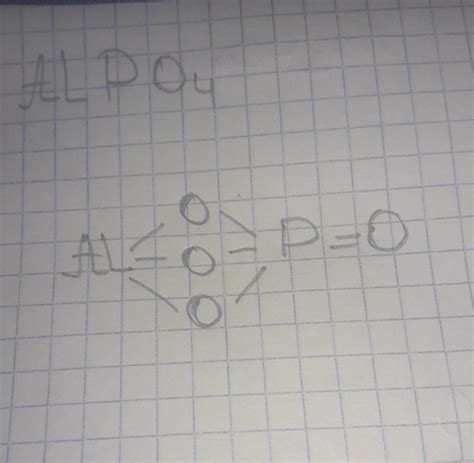
Фосфат алюминия (AlPO4) представляет собой химическое соединение, состоящее из атомов алюминия (Al), фосфора (P) и кислорода (O). Фосфат алюминия образуется при взаимодействии фосфорной кислоты (H3PO4) с алюминием или алюминиевой пудрой.
Фосфат алюминия – это белый кристаллический порошок, который по своим свойствам очень похож на другой фосфат – фосфат кальция. Он является нерастворимым в воде и этиловом спирте, но легко растворяется в солях и некоторых кислотах, например, в растворе серной кислоты (H2SO4).
Фосфат алюминия широко используется в различных отраслях промышленности. Он применяется в качестве катализатора в процессах нефтехимической и пищевой промышленности. Этот соединение также используется в производстве стекла, керамики, эмалей и других материалов.
Молекулярная структура фосфата натрия
Фосфат натрия (Na3PO4) - безцветные кристаллы, растворимые в воде. Его молекулярная структура состоит из атомов натрия (Na), фосфора (P) и кислорода (O), связанных между собой химическими связями.
Фосфат натрия образует кристаллические структуры, в которых одна натриевая ионная группа соединена с трехатомным фосфорным остатком (PO43-). Фосфатная группа в молекуле фосфата натрия состоит из одного атома фосфора и четырех атомов кислорода. Атомы натрия, в свою очередь, образуют октаэдрическую структуру вокруг фосфатного иона.
Фосфат натрия является важным химическим веществом, используемым в различных промышленных процессах. Он широко применяется в производстве моющих средств, стекла, лаков и фосфорной кислоты. Молекулярная структура фосфата натрия определяет его свойства и возможности в химических процессах.
Использование фосфата натрия в различных отраслях промышленности требует строгого контроля и соблюдения безопасности при его хранении и транспортировке. Взаимодействие фосфата натрия с другими химическими веществами может приводить к опасным реакциям, поэтому необходимо соблюдать меры предосторожности при работе с этим веществом.
Соединение фосфата кальция с молекулой H3PO4
Фосфат кальция - это
соединение, которое образуется при взаимодействии ионов кальция Ca2+ с
ионами фосфата PO43-. Данное соединение имеет химическую
формулу Ca3(PO4)2, что означает, что в его структуре присутствуют три
иона кальция и два иона фосфата.
При взаимодействии фосфата кальция
с молекулой H3PO4 образуется осадок, который представляет собой смесь
фосфата кальция и не ионизированной молекулы H3PO4. Фосфат кальция
выпадает в виде белого порошка или кристаллов.
Фосфат кальция широко применяется в
сельском хозяйстве как удобрение, так как кальций является важным
питательным элементом для растений. Кроме того, в фармацевтической
промышленности фосфат кальция используется в качестве добавки в
препараты для профилактики и лечения заболеваний костей и зубов.
Взаимодействие фосфата кальция с
молекулой H3PO4 является одним из примеров химической реакции
нейтрализации, так как при этом происходит образование соли и воды.
Реакция идет по уравнению:
Ca3(PO4)2 + 2H3PO4 → 3Ca(H2PO4)2
Взаимодействие фосфата алюминия с группой атомов остатка H3PO4
Взаимодействие фосфата алюминия с группой атомов остатка H3PO4 является одним из важных процессов в химии. Фосфат алюминия (AlPO4) представляет собой соединение, образованное атому алюминия и фосфата. Атомы остатка H3PO4, в свою очередь, представляют группу атомов, оставшихся после отщепления одной или нескольких молекул воды от фосфорной кислоты.
Взаимодействие фосфата алюминия с группой атомов остатка H3PO4 приводит к образованию структуры сетчатого типа. Это связано с тем, что атомы фосфора и алюминия образуют катионы, которые притягивают отрицательно заряженные атомы кислорода из группы атомов остатка H3PO4.
В результате взаимодействия фосфата алюминия с группой атомов остатка H3PO4 образуется прочная связь, которая обеспечивает стабильность соединения. Кроме того, данное взаимодействие способствует образованию трехмерной структуры, что делает фосфат алюминия одним из наиболее устойчивых соединений.
Фосфат алюминия, полученный в результате взаимодействия с группой атомов остатка H3PO4, применяется в различных областях, включая строительство, медицину, производство керамики и другие. Благодаря своим уникальным свойствам и структуре, фосфат алюминия представляет значительный научный и практический интерес.
Вопрос-ответ

Какая формула фосфата натрия?
Формула фосфата натрия - Na3PO4.
Какие формулы могут иметь фосфаты кальция?
Фосфаты кальция могут иметь такие формулы: Ca(H2PO4)2, CaHPO4 и Ca3(PO4)2.
Какая формула фосфата алюминия?
Формула фосфата алюминия - AlPO4.
Какие формулы фосфатов металлов могут содержать группу атомов остатка H3PO4?
Фосфаты металлов, содержащие группу атомов остатка H3PO4, могут иметь такие формулы: Na3PO4, Ca(H2PO4)2, CaHPO4, Ca3(PO4)2 и AlPO4.
