Щелочные металлы - это группа элементов периодической таблицы химических элементов. Они включают литий (Li), натрий (Na), калий (K), рубидий (Rb) и цезий (Cs). Все эти металлы являются активными химическими элементами, обладающими определенными физическими и химическими свойствами.
Формула "щелочные металлы" была предложена учеными для обозначения данной группы элементов. Эти металлы характеризуются высокой реактивностью, низкой плотностью и низкой температурой плавления. Они обладают способностью к реакции с водой, образуя щелочные растворы, отсюда и происходит название данной группы.
Щелочные металлы имеют особые химические свойства. Например, при реакции с водой они выделяют водород и образуют щелочную среду. Они также являются отличными проводниками электричества и тепла. Многие щелочные металлы огнеопасны и должны храниться в специальных условиях.
Использование щелочных металлов в промышленности широко распространено. Например, натрий используется в производстве мыла и стекла, а калий - в производстве удобрений и лекарств. Они также используются в батареях и аккумуляторах, так как образуют стабильные химические соединения. В то же время, щелочные металлы имеют также и ряд опасных свойств и могут быть ядовитыми, если использование происходит неправильно.
Щелочные металлы: общая характеристика

Щелочные металлы – это группа элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они относятся к самым активным металлам в химической таблице. Щелочные металлы имеют низкую плотность и мягкость, при комнатной температуре они могут быть нарезаны ножом.
Основной химический характеристикой щелочных металлов является их реакция с водой. При контакте с водой они образуют гидроксиды, которые обладают щелочными свойствами. Например, калий взаимодействует с водой с выделением водорода и образованием гидроксида калия:
2K + 2H2O → 2KOH + H2
Щелочные металлы также реагируют с кислородом воздуха, образуя оксиды. Например, литий при контакте с воздухом образует оксид лития:
4Li + O2 → 2Li2O
Одной из особенностей щелочных металлов является их способность формировать положительные ионы, наиболее часто +1 заряд. Это связано с тем, что они имеют один валентный электрон во внешней электронной оболочке. Положительные ионы щелочных металлов обладают особой реакционной способностью и часто вступают в реакции с анионами, образуя соли.
Щелочные металлы находят широкое применение в различных областях. Например, натрий используется в производстве стекла, а калий – в удобрениях. Щелочные металлы также широко применяются в химической и фармацевтической промышленности, а также в производстве батарей и аккумуляторов.
Состав и свойства щелочных металлов

Щелочные металлы включают в себя элементы периодической таблицы химических элементов, а именно литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они обладают следующими общими свойствами.
- 1. Атомы щелочных металлов имеют одну электрон этой оболочки, что делает их атомы стабильными и легко отдающими электроны во внешние электроды.
- 2. Щелочные металлы обладают низкой плотностью и малыми температурами плавления и кипения.
- 3. Они являются хорошими проводниками электричества и тепла.
- 4. Взаимодействуя с водой, щелочные металлы образуют щелочные растворы.
Щелочные металлы химически активны и реактивны, легко вступают во взаимодействие с другими веществами. Это делает их важными элементами в различных сферах нашей жизни, включая медицину, энергетику, промышленность и технологии. Они используются для производства батарей, промышленных катализаторов, удобрений и многих других веществ и материалов.
Физические свойства щелочных металлов

Щелочные металлы - это элементы первой группы периодической системы, включающие литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). У этих металлов есть ряд общих физических свойств, которые делают их уникальными.
Первым заметным физическим свойством щелочных металлов является их низкая плотность. Они настолько легкие, что плавают на воде и могут быть разрезаны ножом. Например, плотность лития составляет всего около 530 килограммов на кубический метр.
Другим важным физическим свойством щелочных металлов является их мягкость. Они настолько мягкие, что могут быть резко согнуты и вытянуты в тонкие проволоки или протянуты в фольгу. Это свойство делает их удобными для использования в процессе изготовления батарей или электродов.
Щелочные металлы обладают также хорошей электропроводностью. Они являются отличными проводниками тока и могут легко передавать электроны. Это способность делает их полезными для использования в аппаратах и устройствах, где необходимо обеспечить электрическую связь.
- еще
- еще
- еще
- еще
Однако, следует отметить, что щелочные металлы очень реактивны и легко соединяются с другими веществами. Они часто образуют соединения с кислородом и водой, образуя щелочные гидроксиды и оксиды. Это свойство делает их опасными в хранении и использовании, и требует соблюдения осторожности при работе с ними.
Все вместе, физические свойства щелочных металлов делают их уникальными и полезными во многих областях. Их низкая плотность, мягкость и хорошая электропроводность делают их ценными материалами для общества и технологии.
Химические свойства щелочных металлов
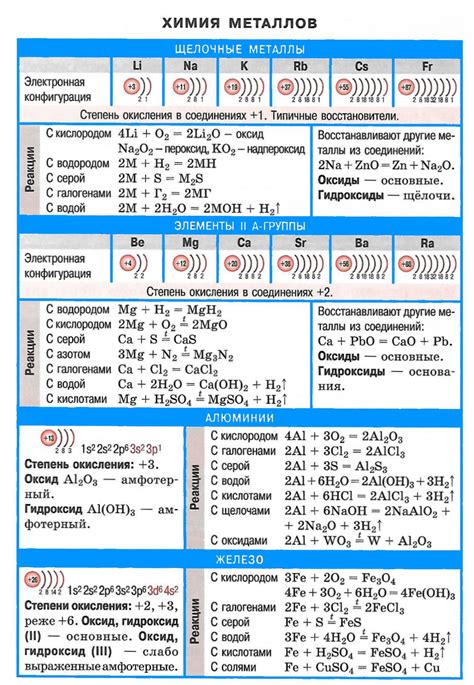
Щелочные металлы - это элементы, которые относятся к первой группе периодической системы, включающейся литий, натрий, калий, рубидий, цезий и франций. Все они обладают общими химическими свойствами, связанными с их активностью и реакционностью.
Первым важным химическим свойством щелочных металлов является их способность к реакции с водой. При контакте с водой они образуют щелочные гидроксиды и выделяются водород. Это обусловлено высокой реакционной способностью щелочных металлов. Реакция с водой является очень интенсивной и сопровождается выделением тепла.
Еще одним химическим свойством щелочных металлов является их способность образовывать соли. Щелочные металлы реагируют с кислотами, образуя соли и выделяя водород. Это происходит из-за их способности отдавать электроны и образовывать ионы с положительным зарядом.
Щелочные металлы также проявляют высокую активность в реакциях с галогенами (фтором, хлором, бромом, иодом) и другими неметаллами. Эти реакции протекают очень быстро и интенсивно, в результате чего образуются соответствующие соединения.
Кроме того, щелочные металлы хорошо растворяются в воде, образуя щелочные растворы. Это связано с их способностью образовывать ионы гидроксидов. В растворах щелочных металлов присутствуют ионы металла и гидроксидионы, которые придают растворам щелочную среду и выводят их за пределы нейтрального pH.
Использование щелочных металлов в промышленности

Щелочные металлы – это группа химических элементов, которые легко реагируют с водой, образуя щелочные растворы. Именно благодаря своим свойствам эти металлы нашли широкое применение в различных сферах промышленности.
Одна из основных областей использования щелочных металлов – производство щелочей. Натрий, калий, литий и другие элементы используются для получения гидроксидов, которые являются основными компонентами щелочей. Гидроксиды натрия и калия находят применение в стекольной, химической и некоторых других отраслях промышленности.
Щелочные металлы также нашли применение в электропромышленности. Калий является важным компонентом электролита, используемого в литий-ионных аккумуляторах, которые широко применяются в современных мобильных устройствах и электромобилях. Калийные соединения также применяются в процессе производства стекла для устранения поверхностных дефектов.
Благодаря своей высокой реактивности, щелочные металлы находят применение в многих химических процессах. Например, натрий используется при производстве металлов, таких как алюминий и титан. Литий, в свою очередь, применяется в производстве легких сплавов и в электрохимических батареях.
Кроме того, щелочные металлы используются в процессах очистки воды. Гидроксиды натрия и калия применяются для регулирования уровня pH в воде и удаления загрязнений. Литий в виде литиевых соединений также может использоваться для очистки воды от различных примесей.
Влияние щелочных металлов на живые организмы
Щелочные металлы, такие как литий, натрий и калий, играют важную роль в функционировании живых организмов. Они участвуют во множестве биохимических процессов, влияют на работу нервной системы и обеспечивают равновесие в организме.
Первым щелочным металлом, роль которого была открыта в организме человека, является калий. Он играет важную роль в поддержании нормального функционирования клеток, особенно мышц и сердечной мышцы. Недостаток калия может привести к нарушению сердечного ритма и мышечной слабости.
Литий является важным микроэлементом, который регулирует активность нервной системы. Он участвует в передаче нервных импульсов и стабилизирует настроение. Недостаток лития может вызвать раздражительность, апатию и депрессию.
Натрий является одним из основных электролитов в организме, играя роль водо-солевого равновесия. Он регулирует объемы внутриклеточной и внеклеточной жидкости, участвует в передаче нервных импульсов и сократительной активности мышц. Недостаток натрия может привести к обезвоживанию и нарушению работы сердечно-сосудистой системы.
Однако, несмотря на важность щелочных металлов для организма, их избыток также может быть опасен. Ежедневное потребление большого количества натрия, например, часто приводит к повышенному давлению и заболеваниям сердца. Поэтому важно поддерживать баланс щелочных металлов в организме и употреблять их в достаточном, но не избыточном количестве.
Итак, щелочные металлы играют важную роль в жизни организмов. Они участвуют в биохимических процессах, регулируют работу нервной системы и поддерживают равновесие в организме. Однако, важно помнить о потребности в достаточном, но не избыточном количестве щелочных металлов для сохранения здоровья.
Значение щелочных металлов в экологии
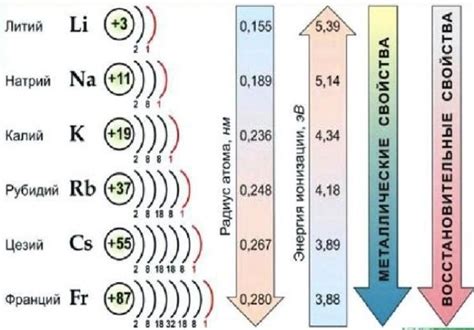
Щелочные металлы в экологии играют значительную роль, так как они являются неотъемлемой частью многих процессов, происходящих в природной среде и оказывают влияние на живые организмы.
Один из основных аспектов значения щелочных металлов в экологии связан с их участием в биохимических реакциях в организмах животных и растений. Например, калий играет важную роль в регуляции водного баланса, участвует в процессе фотосинтеза и синтезе белков. Натрий необходим для нормального функционирования нервной системы и регуляции кровяного давления.
Другим важным аспектом значимости щелочных металлов в экологии является их влияние на экосистему. Например, высокое содержание калия может привести к снижению биоразнообразия в определенных видах экосистем и угрозе для редких видов растений и животных. Также высокая концентрация натрия в почвах может стать причиной солонизации и деградации почвенного покрова.
Кроме того, щелочные металлы имеют важное значение в экологии в контексте предотвращения загрязнения окружающей среды. Они используются в процессе очистки воды и воздуха. Например, гидроксид натрия является ключевым компонентом многих моющих средств и средств для очистки воды, благодаря своим щелочным свойствам.
Изучение значимости щелочных металлов в экологии помогает понять сложные взаимодействия в природных экосистемах и способствует разработке мер, направленных на их сохранение и устойчивое использование.
Перспективы исследований в области щелочных металлов

Щелочные металлы являются одной из ключевых групп элементов в периодической системе химических элементов, и поэтому исследования в области этих металлов имеют большое значение для различных отраслей науки и промышленности.
Первые исследования щелочных металлов были проведены в XIX веке, но до сих пор существуют множество неизученных аспектов и потенциальных применений этих веществ. Одной из перспективных областей исследований является изучение реакций щелочных металлов с различными химическими веществами. Это позволяет расширить нашу базу знаний о реактивных свойствах металлов и найти новые пути их использования.
Еще одной важной областью исследований является изучение структуры и свойств щелочных металлов на молекулярном уровне. С помощью различных физических методов, таких как рентгеновская дифракция и спектроскопия, можно получить информацию о взаимодействии между атомами в молекуле. Это открывает возможности для создания новых материалов с улучшенными свойствами и для разработки новых технологий.
Исследования щелочных металлов также могут быть полезны при решении экологических проблем. Например, исследования по разработке новых методов сжигания отходов с использованием щелочных металлов могут помочь уменьшить негативное воздействие на окружающую среду. Кроме того, изучение возможности использования этих металлов в солнечных батареях и других видов альтернативной энергетики может сделать их более доступными и эффективными.
Наконец, в области медицины исследования щелочных металлов могут привести к разработке новых лекарственных препаратов и методов лечения различных заболеваний. Взаимодействие металлов с организмом человека может иметь важное значение для понимания процессов здоровья и разработки новых способов их поддержания и восстановления.
В целом, исследования в области щелочных металлов имеют большой потенциал и могут привести к созданию новых материалов, разработке новых технологий и решению различных проблем. Это делает их важной областью научных исследований и открывает множество перспектив для будущих открытий и применений.
Вопрос-ответ

Какая формула свойства щелочные металлы?
Формула свойства щелочные металлы можно представить следующим образом: KM, где K - символ щелочного металла, а M - символ второго элемента соединения.
Какие элементы относятся к щелочным металлам?
К щелочным металлам относятся элементы первой группы периодической таблицы: литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Какие основные свойства щелочных металлов?
Основные свойства щелочных металлов включают: высокую реактивность, мягкость и низкую плотность, низкую температуру плавления и кипения, хорошую электропроводность, образование щелочных растворов и гидроксидов, способность образовывать соли с кислотами.
Зачем используются щелочные металлы?
Щелочные металлы широко используются в различных областях, включая промышленность, медицину, электронику и сельское хозяйство. Например, калий используется в удобрениях, натрий - в производстве стекла и мыла, литий - в производстве аккумуляторов.
