Щелочные и щелочноземельные металлы – это группы элементов в периодической системе, которые играют важную роль в химических и физических процессах. Они являются основными металлами и обладают некоторыми общими свойствами, такими как низкая плотность, низкая температура плавления и высокая реакционная способность.
К группе щелочных металлов относятся элементы первой группы периодической системы – литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они отличаются высокой активностью и легкостью образования положительного иона. Щелочные металлы активно реагируют с водой и кислородом, образуя гидроксиды и оксиды.
Группа щелочноземельных металлов состоит из элементов второй группы периодической системы – бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они обладают высокими температурами плавления и кристаллическими структурами. Щелочноземельные металлы меньше реактивны, чем щелочные металлы, но все же могут реагировать с водой и кислородом.
Щелочные и щелочноземельные металлы широко применяются в различных отраслях промышленности, таких как металлургия, электроника и медицина. Они используются в производстве батареек, сплавов, катализаторов, искусственных удобрений и лекарственных препаратов.
Важно отметить, что щелочные и щелочноземельные металлы имеют большое значение для нашей повседневной жизни и научных исследований, и их изучение позволяет лучше понять мир химии и физики. Они представляют собой важные элементы периодической системы и основу для многих химических реакций и процессов.
Щелочные металлы
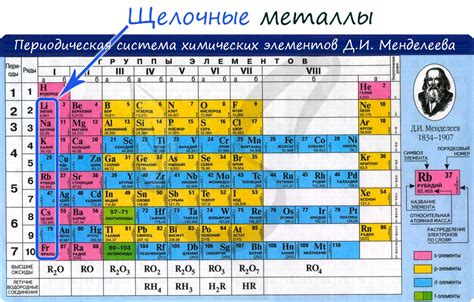
Щелочные металлы - это группа элементов в периодической системе, состоящая из лития (Li), натрия (Na), калия (K), рубидия (Rb), цезия (Cs) и франция (Fr). Они являются первой группой в таблице, металлические элементы, имеющие низкую плотность и низкую температуру плавления.
Щелочные металлы обладают общими характеристиками, такими как мягкость, низкая плотность и низкая температура плавления. Они имеют одну электронную оболочку, что делает их очень реакционными и способными образовывать ионные соединения с другими элементами. Они также обладают хорошей электропроводностью и хорошо растворяются в воде.
Щелочные металлы широко используются в различных областях, включая производство стекла, лекарственных препаратов, батарей и металлургической промышленности. Они также используются в качестве катализаторов для химических реакций и в радиоактивной медицине.
Во всех щелочных металлах проводимость электрического тока очень высокая. Их ионы могут двигаться в металлической решетке, образовывая электрический ток. Кроме того, щелочные металлы известны своими взрывоопасными свойствами. Когда они взаимодействуют с водой, могут образовываться водород и щелочные гидроксиды.
Определение и свойства

Щелочные и щелочноземельные металлы представляют собой группы элементов в периодической системе химических элементов. Щелочные металлы включают литий, натрий, калий, рубидий, цезий и франций. Щелочноземельные металлы включают бериллий, магний, кальций, стронций, барий и радий.
Основным свойством щелочных металлов является их реактивность. Они являются самыми активными металлами и быстро реагируют с водой и кислородом, образуя гидроксиды и оксиды. Щелочные металлы обладают мягкой текстурой и низким плавлением, благодаря чему они легко обрабатываются и используются для создания сплавов.
В отличие от щелочных металлов, щелочноземельные металлы не так реактивны и менее распространены в природе. Щелочноземельные металлы обладают более высокой плотностью и твердостью по сравнению с щелочными металлами. Они также образуют соединения с кислородом и другими элементами, такими как сера и хлор.
Щелочные и щелочноземельные металлы имеют широкое применение в различных отраслях, включая производство аккумуляторов, сплавов, огнестойких материалов и стекла. Они также используются в химической промышленности в качестве катализаторов и в медицине для создания лекарственных препаратов.
Применение в промышленности

Щелочные и щелочноземельные металлы широко применяются в различных отраслях промышленности благодаря своим уникальным свойствам и химической реактивности.
Натрий, который является одним из щелочных металлов, используется в производстве стекла, мыла и моющих средств. Благодаря своим отличным диэлектрическим свойствам, натрий также находит применение в электроэнергетике и производстве батарей.
Калий, также относящийся к щелочным металлам, широко используется в производстве удобрений. Калийные удобрения являются неотъемлемой частью сельского хозяйства, так как способствуют росту растений и увеличению урожайности.
Магний, щелочноземельный металл, имеет широкое применение в автомобильной и авиационной промышленности благодаря своей легкости и прочности. Магниевые сплавы применяются для производства компонентов автомобилей, включая двигатели, трансмиссию и рамы. Кроме того, магний используется в производстве огнеупорных материалов и легких металлоконструкций.
Кальций, также относящийся к щелочноземельным металлам, находит применение в производстве стекла, цемента и стали. Кальцийные соединения используются в качестве добавок в пластике, резине и лаках. Кальций также является важным компонентом диеты человека, необходимым для здоровых костей и зубов.
Щелочноземельные металлы
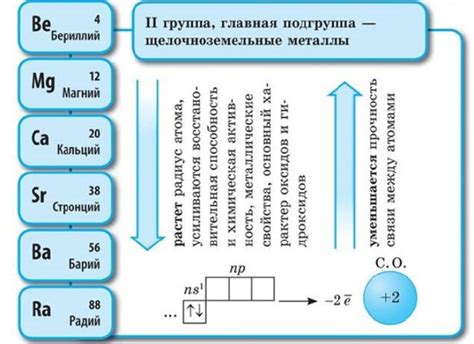
Щелочноземельные металлы - это элементы химической группы 2 периодической системы, расположенные после щелочных металлов. В эту группу входят следующие элементы: бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Щелочноземельные металлы обладают рядом общих химических свойств. Они являются мягкими металлами, силно реактивными и легкими для обработки. Также они имеют низкую плотность и точку плавления, что делает их прекрасными материалами для конструкций, авиации и автомобилестроения.
Однако, щелочноземельные металлы реагируют с водой и влажным воздухом, поэтому их необходимо хранить под слоем масла или в инертной среде. Они могут формировать соединения с различными элементами, такими как кислород, сера и азот, что делает их важными в различных отраслях химической промышленности.
Щелочноземельные металлы также имеют множество применений в быту. Кальций используется для производства строительных материалов, магний применяется в лекарствах и в качестве сплава в автомобильной промышленности, а бериллий является неотъемлемым компонентом в электронике.
Таким образом, щелочноземельные металлы играют важную роль в промышленности и научных исследованиях, а также в повседневной жизни человека.
Определение и свойства

Щелочные металлы - это элементы, которые относятся к первой группе периодической системы. Включают в себя литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они характеризуются высокой активностью и реактивностью.
Основными свойствами щелочных металлов является их низкая плотность, мягкость и низкая температура плавления. Вещества в данной группе обладают высокой электроотрицательностью и способностью образовывать ионы с положительным зарядом.
Щелочные металлы обладают способностью активно реагировать с водой, образуя щелочные растворы. Они также способны гореть в контакте с воздухом, образуя пламя и образцаючие яркое пламя.
Щелочноземельные металлы - это элементы, которые относятся ко второй группе периодической системы. Включают в себя бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они характеризуются большей плотностью и температурой плавления по сравнению со щелочными металлами.
Щелочноземельные металлы также обладают высокой электроотрицательностью и активностью. Они могут образовывать ионы с положительным зарядом и легко реагировать с другими элементами. Они используются в различных отраслях промышленности, в том числе в производстве стекла, алюминия и стали.
Щелочные и щелочноземельные металлы являются важными элементами в периодической системе, которые имеют большое значение для нашей повседневной жизни и различных областей науки и промышленности.
Распространение в природе
Щелочные и щелочноземельные металлы широко распространены в природе и встречаются как в минералах, так и в органических и неорганических соединениях. Они являются важными компонентами земной коры и играют ключевую роль во многих процессах в природе.
Минералы, содержащие щелочные металлы, часто называются «шпатами». Например, сильвин – это калийный шпат, а нефелин – натриевый шпат. Эти минералы образуются в результате геологических процессов, таких как кристаллизация магмы или метаморфизм. Они часто встречаются в гранитах, пегматитах и горных породах, и используются в строительстве и производстве стекла и керамики.
Щелочноземельные металлы, такие как магний, кальций и стронций, также находятся в различных минералах. Кальцит – основной источник кальция, а стронцианит – основной источник стронция. Эти минералы образуются в осадочных породах или образуются в ходе метаморфических процессов. Они широко используются в производстве цемента, стали и стекла, а также в сельском хозяйстве и медицине.
В органических соединениях щелочные и щелочноземельные металлы также играют важную роль. Например, калий необходим для нормального функционирования растений, и его соединения используются в удобрениях. Кальций и магний являются неотъемлемыми компонентами костей и зубов животных и человека.
Распространение щелочных и щелочноземельных металлов в природе является неотъемлемой частью геохимии и геологии. Их важность для жизни на Земле и широкое использование в различных отраслях промышленности делает изучение этих элементов актуальным и интересным.
Применение в технике и медицине

Щелочные и щелочноземельные металлы широко применяются в различных областях техники и медицины благодаря своим уникальным свойствам.
В технике щелочные и щелочноземельные металлы используются для производства батарей и аккумуляторов. Их высокая электропроводность и энергетическая плотность делает их идеальными для использования в устройствах, где нужна долгая автономность работы. Кроме того, некоторые из этих металлов, такие как литий и калий, используются в процессе производства электроники, например, в качестве компонентов батарей для мобильных устройств и ноутбуков.
В медицине щелочные и щелочноземельные металлы также применяются в целом ряде областей. Например, натрий используется для регулирования водно-солевого баланса в организме и в инфузионных растворах при недостатке электролитов. Калий играет важную роль в регуляции сердечного ритма и сокращений мышц, поэтому его соли используются при лечении сердечных заболеваний. Кальций является основным компонентом костей и зубов и используется в лечении остеопороза и нарушений обмена кальция в организме.
В дентистрии щелочные и щелочноземельные металлы используются для создания сплавов, которые применяются в процессе изготовления зубных протезов и индивидуальных реставраций. Эти сплавы обладают высокой прочностью и долговечностью, что позволяет создавать качественные и долговечные изделия.
Таким образом, щелочные и щелочноземельные металлы являются важными компонентами в технике и медицине благодаря своим уникальным свойствам и широкому спектру применения. Их электропроводность, энергетическая плотность и возможность регулировать баланс электролитов делают их незаменимыми в электронике, производстве батарей и аккумуляторов, а также в лечении различных заболеваний.
Сходства и различия
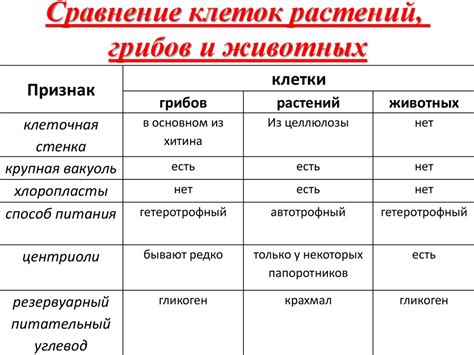
Сходства между щелочными и щелочноземельными металлами:
- Щелочные и щелочноземельные металлы оба относятся к группам элементов в периодической системе.
- Они оба обладают активными химическими свойствами и легко вступают в реакции с другими веществами.
- Оба класса металлов обычно образуют положительные ионы, отдавая электроны при реакциях.
Различия между щелочными и щелочноземельными металлами:
- Одно из основных различий между ними заключается в их положении в периодической системе веществ. Щелочные металлы находятся в первой группе, а щелочноземельные металлы - во второй группе.
- Щелочные металлы имеют одну валентную электронную оболочку, в то время как щелочноземельные металлы имеют две валентные электронные оболочки.
- Щелочные металлы имеют более низкие температуры плавления и кипения, чем щелочноземельные металлы.
- Щелочные металлы, такие как литий и натрий, более реактивны, чем щелочноземельные металлы, такие как магний и кальций.
Таким образом, щелочные и щелочноземельные металлы имеют некоторые сходства в своих химических свойствах, но одновременно отличаются по ряду важных признаков, включая положение в периодической системе, количество валентных электронных оболочек и уровень реактивности.
Химические свойства

Щелочные и щелочноземельные металлы обладают различными химическими свойствами, которые определяют их роль в периодической системе и применение в различных областях.
Щелочные металлы (литий, натрий, калий, рубидий, цезий и франций) являются очень реактивными элементами. Они легко образуют положительные ионы, обладающие однозначным зарядом +1. Щелочные металлы обладают низкой плотностью и низкой температурой плавления, что делает их мягкими и легко расплавляемыми.
Щелочноземельные металлы (бериллий, магний, кальций, стронций, барий и радий) также обладают высокой реактивностью, но они менее реактивны, чем щелочные металлы. Они имеют заряд +2 и также легко образуют положительные ионы. Щелочноземельные металлы имеют высокую плотность и высокую температуру плавления, что делает их прочными и устойчивыми к высоким температурам.
Оба типа металлов обладают способностью реагировать с кислородом из воздуха, образуя оксиды. Щелочные металлы образуют щелочные оксиды, которые обладают базичными свойствами и растворяются в воде, образуя гидроксиды. Щелочноземельные металлы образуют щелочноземельные оксиды, которые также обладают базичными свойствами, но слабее растворяются в воде.
Щелочные и щелочноземельные металлы также образуют соли с различными кислотами. Эти соли имеют множество применений в различных отраслях химии, медицине, пищевой промышленности и технологии.
Вопрос-ответ

Какие элементы входят в группу щелочных металлов в периодической системе?
В группу щелочных металлов входят литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Какие элементы входят в группу щелочноземельных металлов?
В группу щелочноземельных металлов входят бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra).
Каковы основные свойства щелочных металлов?
Основные свойства щелочных металлов включают высокую реактивность, низкую плотность, низкую температуру плавления и кипения, легкость образования оксидов и гидроксидов, а также образование ярких пламенных испарений при горении.
Какую роль играют щелочные и щелочноземельные металлы в живой природе?
Щелочные и щелочноземельные металлы играют важную роль в живой природе. Например, биологически активные формы калия, натрия, магния и кальция необходимы для работы многих ферментов и участвуют в передаче нервных импульсов. Также щелочные металлы необходимы для образования ионов, регулирующих уровень pH в организмах живых организмов.
