Взаимодействие различных металлических материалов может привести к возникновению электрохимической коррозии. Этот процесс является одной из основных причин деградации и разрушения металлических конструкций в различных отраслях промышленности и строительства.
Электрохимическая коррозия возникает при контакте двух материалов, различающихся в своих электрохимических свойствах, таких как потенциал окисления и скорость коррозионных процессов. В результате этого контакта образуется гальваническая пара, в которой один металл выступает в роли анода, а другой – в роли катода.
Электрохимическая коррозия может приводить к различным негативным последствиям, таким как потеря механических свойств металлических конструкций, изменение их внешнего вида, уменьшение срока службы и даже полное разрушение. Для предотвращения электрохимической коррозии необходимо применять различные методы защиты, такие как нанесение защитных покрытий, использование антикоррозионных добавок и правильный выбор соединительных деталей.
Электрохимическая коррозия: проблемы и решения
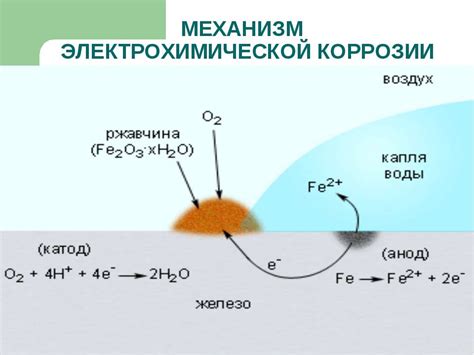
Электрохимическая коррозия является одной из основных проблем, с которыми сталкиваются металлические материалы в различных средах. Коррозия может привести к потере прочности материала, изменениям его внешнего вида и значительному ухудшению эксплуатационных свойств.
Одним из основных факторов, влияющих на электрохимическую коррозию, является наличие различных металлов в контакте друг с другом. При наличии электролитической среды, в которой металлы являются анодом и катодом, возникает гальваническая пара, что приводит к процессу коррозии.
Для решения проблемы электрохимической коррозии существует несколько подходов. Во-первых, можно использовать специальные антикоррозийные покрытия на металлических поверхностях. Эти покрытия создают защитный слой, который препятствует взаимодействию металлов с окружающей средой.
Во-вторых, для предотвращения электрохимической коррозии можно применять методы катодной защиты. Они базируются на создании электрического поля, которое подавляет коррозионный процесс и защищает металл от анодного растворения. Катодная защита может быть осуществлена путем подключения катодов или использования специальных анодов-культиваторов.
Также для борьбы с электрохимической коррозией можно применять адгезионные антикоррозийные покрытия, которые создаются путем нанесения на металлическую поверхность слоя состоящего из полимеров. Этот слой препятствует проникновению влаги и кислорода до металла, что снижает вероятность возникновения коррозии.
В целом, решение проблемы электрохимической коррозии требует комплексного подхода, включающего применение антикоррозийных покрытий, использование методов катодной защиты и предотвращение взаимодействия различных металлов в агрессивной среде. Только таким образом можно обеспечить долговечность и надежность металлических конструкций!
Взаимодействие двух металлических материалов: особенности и факторы

Электрохимическая коррозия является одним из основных способов разрушения металлических материалов и является результатом их взаимодействия. Коррозия может возникать при контакте двух разных металлов в присутствии электролита или при воздействии влаги и атмосферных условий.
Особенностью взаимодействия двух металлических материалов является возникновение гальванической пары. При этом один металл, выступая в роли анода, начинает активно окисляться, а второй металл, выступая в роли катода, становится объектом коррозии. Такое взаимодействие зависит от различных факторов, включая композицию металлов, их электрохимические свойства и температуру окружающей среды.
Один из важных факторов, влияющих на взаимодействие двух металлических материалов, - это разница в их электрохимическом потенциале. Чем больше разница в потенциалах между металлами, тем больше вероятность возникновения гальванической пары и разрушения материалов.
Кроме того, взаимодействие металлов может зависеть от их состояния поверхности. Наличие механических дефектов, микротрещин и других повреждений может способствовать ускоренной коррозии и распространению ее процесса.
Правильный выбор металлических материалов, предотвращение контакта между разными металлами и использование защитных покрытий - все это важные меры для минимизации электрохимической коррозии и сохранности металлических конструкций.
Роль окружающей среды в процессе электрохимической коррозии
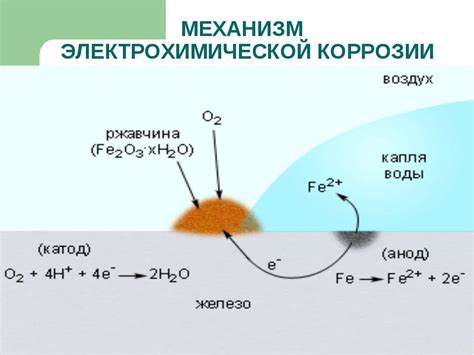
Окружающая среда играет важную роль в процессе электрохимической коррозии металлов. Несмотря на то, что металлы обладают высокой прочностью и стабильностью, они подвержены воздействию неблагоприятных условий окружающей среды, таких как влага, кислоты, соли и другие химически активные вещества. В результате взаимодействия металлов и окружающей среды возникают электрохимические процессы, приводящие к их коррозии.
Одним из факторов, влияющих на электрохимическую коррозию, является влажность окружающей среды. При высокой влажности воздуха увеличивается активность коррозионных процессов, так как вода действует как электролит, проводящий электрический ток между анодом и катодом. Также влага может содержать растворенные в ней соли и другие химически активные вещества, которые усиливают коррозию металлов.
Кроме влажности, важную роль в процессе электрохимической коррозии играют кислоты. Кислотное окружение оказывает разрушительное воздействие на металлы, ускоряя коррозию. Кислоты могут быть как природного происхождения (например, кислотные осадки), так и промышленного (например, кислотные выбросы). Кислотное воздействие в сочетании с другими факторами окружающей среды, такими как влага и соли, может привести к быстрой деградации металлических материалов.
Кроме того, соли являются одним из основных причин электрохимической коррозии. В окружающей среде содержится большое количество различных солей, как естественного, так и искусственного происхождения. Соли могут растворяться в воде и образовывать электролиты, способствующие проведению электрического тока в процессе коррозии металлов. Более того, соли могут вызывать электролитическую коррозию, когда один металл выступает в роли анода, а другой – в роли катода.
Таким образом, окружающая среда имеет существенное влияние на процесс электрохимической коррозии металлов. Высокая влажность, наличие кислот, солей и других химически активных веществ способствуют активации коррозионных процессов и вызывают повреждение металлических материалов. Изучение и контроль этих и других факторов окружающей среды помогут предотвратить или замедлить процесс коррозии, что важно для обеспечения долговечности и надежности металлических конструкций и изделий.
Методы прогнозирования и предотвращения электрохимической коррозии
Электрохимическая коррозия является одним из основных видов повреждений металлических материалов, вызываемых химическими реакциями с окружающей средой. Для предотвращения электрохимической коррозии необходимо применять методы прогнозирования и принимать соответствующие меры.
Методы прогнозирования электрохимической коррозии
Один из методов прогнозирования электрохимической коррозии - это проведение экспериментов в лаборатории с использованием специализированного оборудования. В ходе таких экспериментов можно изучать взаимодействие двух металлических материалов в различных условиях, включая температуру, влажность и наличие различных химических соединений. Это позволяет определить вероятность возникновения электрохимической коррозии и ее скорость в реальных условиях эксплуатации.
Еще одним методом прогнозирования электрохимической коррозии является использование математических моделей. При создании таких моделей учитываются различные факторы, влияющие на электрохимическую коррозию, такие как состав металла, его структура, взаимодействие с окружающей средой и другие параметры. Математические модели позволяют симулировать взаимодействие металлов и предсказывать вероятность возникновения коррозии в различных условиях.
Методы предотвращения электрохимической коррозии
Для предотвращения электрохимической коррозии могут использоваться различные методы. Один из самых эффективных способов - это нанесение на поверхность металлических материалов защитных покрытий. Такие покрытия могут быть выполнены из специальных антикоррозийных покрытий, которые создают защитный барьер между металлом и окружающей средой. Также могут применяться методы катодной защиты, при которых создается электрический потенциал, который подавляет коррозийные процессы.
Другим методом предотвращения электрохимической коррозии является использование антикоррозийных добавок в материалах или окружающей среде. Такие добавки могут изменять хемический состав окружающей среды или взаимодействие металлов, что препятствует возникновению электрохимической коррозии.
В заключение, методы прогнозирования и предотвращения электрохимической коррозии являются важными для сохранения долговечности металлических материалов и обеспечения их безопасной эксплуатации. Применение таких методов позволяет снизить риск повреждения металлов и увеличить их срок службы.
Влияние покрытий и покрытий на возникновение и развитие коррозии
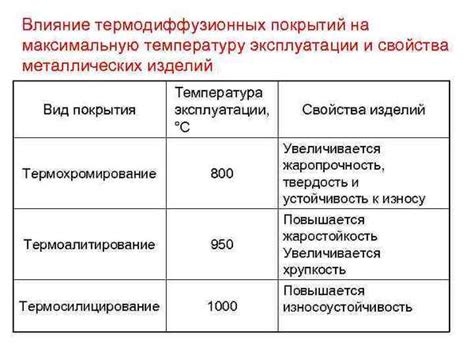
Покрытия и покрытия на металлических материалах играют важную роль в защите от коррозии. Они могут предотвратить контакт металлической поверхности с коррозионно-активной средой, создать барьер, который блокирует доступ влаги, кислорода и других веществ к металлу.
Одним из наиболее распространенных типов покрытий является органическое покрытие, также известное как краска или эмаль. Оно образует защитный слой на поверхности металла, предотвращая проникновение влаги, кислорода и агрессивных веществ. Органические покрытия могут быть применены на металлических поверхностях различных форм и размеров, обеспечивая надежную защиту от коррозии.
Кроме органических покрытий, существуют и другие типы покрытий, такие как металлические пленки и нанопокрытия. Металлические пленки могут быть нанесены на поверхность металла путем нанесения тонкого слоя коррозионно-устойчивого металла, такого как цинк или алюминий. Эти пленки образуют защитный барьер, который предотвращает контакт металла с окружающей средой. Нанопокрытия, в свою очередь, состоят из наночастиц, которые образуют тонкий слой на поверхности металла. Они обладают высокой адгезией и устойчивостью к коррозии.
Выбор подходящего покрытия или покрытия зависит от многих факторов, таких как тип металла, окружающая среда и условия эксплуатации. Неправильный выбор покрытия или его низкое качество может привести к ускоренной коррозии, что приведет к потере функциональности и долговечности металлических конструкций и изделий. Поэтому важно учитывать все эти факторы при выборе покрытий и покрытий, чтобы обеспечить надежную защиту от коррозии и продлить срок службы металлических материалов.
Примеры применения защитных покрытий в промышленности

В промышленности защитные покрытия широко используются для предотвращения электрохимической коррозии при контакте металлических материалов. Они образуют защитную плёнку на поверхности изделий, которая предотвращает взаимодействие с окружающей средой и уменьшает возникновение коррозии.
Примером применения защитных покрытий является автомобильная промышленность. Кузовы автомобилей защищены от коррозии покрытием, которое защищает металлическую поверхность от воздействия атмосферных осадков и химических веществ на дорогах. Защитные покрытия также применяются на деталях автомобильных двигателей, чтобы предотвратить взаимодействие металлов и жидкостей, таких как масло или антифриз.
В строительной промышленности защитные покрытия используются для защиты металлических конструкций от коррозии. Например, металлические решётки и ограждения, установленные на улицах, покрываются специальным покрытием, чтобы предотвратить их разрушение под воздействием атмосферных условий. Защитные покрытия также применяются на металлических конструкциях зданий, чтобы предотвратить их коррозию при контакте с воздухом и другими химическими веществами.
Защитные покрытия также широко применяются в промышленности, где используются агрессивные химические вещества. Например, в химической промышленности защитные покрытия применяются на резервуарах, трубопроводах и оборудовании, чтобы предотвратить их коррозию от контакта с химическими веществами. Такие покрытия способны выдерживать агрессивные условия и предотвращать утечку и повреждение оборудования, что является критическим для безопасности и эффективности процессов в химической промышленности.
В общем, защитные покрытия играют важную роль в промышленности, обеспечивая защиту металлических материалов от электрохимической коррозии и повышая их долговечность и стойкость к агрессивным воздействиям окружающей среды.
Перспективы исследований в области электрохимической коррозии
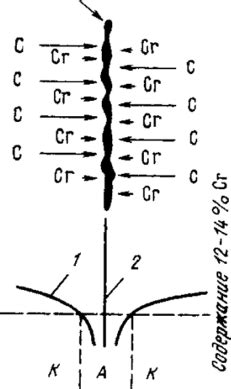
Электрохимическая коррозия является серьезной проблемой во многих индустриальных секторах, таких как металлургия, строительство, энергетика и автомобильная промышленность. Изучение и понимание механизмов, приводящих к коррозии металлических материалов, является ключевым для разработки эффективных методов предотвращения и защиты.
Одной из перспективных областей исследований является разработка новых материалов с улучшенной устойчивостью к электрохимической коррозии. На сегодняшний день уже существуют некоторые материалы, которые обладают высокой коррозионной стойкостью, например, нержавеющие стали и алюминиевые сплавы. Однако постоянно возникают новые вызовы, связанные с более агрессивными средами эксплуатации или необходимостью повышенной прочности материалов. Поэтому необходимо проводить исследования, направленные на поиск новых материалов и оптимизацию их химического состава и структуры.
Другой направлением исследований является разработка новых методов защиты от коррозии. Существует несколько методов, таких как покрытия, антикоррозионные покрытия, пассивация и катодная защита, которые используются для защиты металлов от электрохимической коррозии. Однако большинство из них имеет свои ограничения и недостатки. Поэтому важным направлением исследований является разработка новых и более эффективных методов исключения контакта разнородных металлов и обеспечения защиты от коррозии.
Также перспективными могут быть исследования направленные на разработку новых методов контроля и мониторинга коррозии. Разработка новых датчиков и сенсоров, способных регистрировать и измерять электрохимические процессы на поверхности металлов, может значительно улучшить возможности прогнозирования коррозионных процессов и предотвращения их развития.
В целом, исследования в области электрохимической коррозии играют важную роль в развитии новых материалов и методов защиты от коррозии. Перспективы исследований в этой области связаны с разработкой новых материалов, оптимизацией методов защиты и разработкой новых методов контроля и мониторинга коррозии, что может значительно повысить эффективность и надежность применения материалов в различных индустриальных отраслях.
Вопрос-ответ

Какую роль играют электрохимические процессы в коррозии металлов?
Электрохимические процессы играют важную роль в коррозии металлов, поскольку они являются основным механизмом разрушения металлических материалов в контакте с окружающей средой. Взаимодействие металла с окружающей средой приводит к образованию электрохимических элементов, таких как аноды и катоды, что приводит к коррозии металла.
Что такое анод и катод в контексте электрохимической коррозии?
Анод и катод - это две основные части электрохимической ячейки, которые образуются при взаимодействии металлических материалов с окружающей средой. Анод - это область металла, где происходит окисление и образование ионов металла, а катод - это область металла, где происходит восстановление ионов металла.
Каковы основные факторы, влияющие на скорость электрохимической коррозии металлов?
Скорость электрохимической коррозии металлов зависит от нескольких факторов, включая химическую активность металла, свойства окружающей среды, температуру, наличие кислорода, концентрацию электролита и другие. Оптимальные условия для коррозии металла могут существовать при определенной комбинации этих факторов.
Каковы методы предотвращения электрохимической коррозии металлов?
Существуют различные методы предотвращения электрохимической коррозии металлов, включая использование защитных покрытий и покрытий, применение антикоррозионных покрытий, установку анодной защиты, контроль окружающей среды и поддержание подходящих температурных и химических условий.
