Электрохимическая коррозия является одной из наиболее распространенных и разрушительных форм коррозии металлов. Она возникает при взаимодействии металла с окружающей средой, под воздействием электролита и различных химических реагентов.
В основе электрохимической коррозии лежит электрохимический процесс, в ходе которого металл подвергается окислению и выделению электронов. Эти процессы приводят к разрушению металлической структуры и образованию коррозионных продуктов.
Электрохимическая коррозия металлов является результатом нескольких факторов, включая влажность, температуру, кислотность окружающей среды, а также наличие других металлов и ионов в окружающем растворе. Например, вода является одним из наиболее распространенных электролитов, способных вызывать коррозию металлов.
Понимание основ электрохимической коррозии металлов позволяет разрабатывать методы защиты от коррозии, а также эффективные способы ремонта поврежденных металлических конструкций. Оно также позволяет внести вклад в развитие новых материалов и технологий, с целью улучшения стойкости металлов к коррозии и повышения их срока службы.
Что такое электрохимическая коррозия?

Электрохимическая коррозия - это процесс разрушения металла, вызванный его взаимодействием с окружающей средой при наличии электролита. Она является одной из наиболее распространенных и разрушительных форм коррозии.
Процесс электрохимической коррозии основан на принципах химической реакции, происходящей на поверхности металла в присутствии влаги или других электролитов. В результате взаимодействия металла с окружающей средой образуются электрохимические элементы, так называемые гальванические элементы, в которых происходят анодные и катодные процессы.
Анодный процесс - это окисление металла, при котором металлические ионы переходят в раствор. Катодный процесс - это восстановление металла, при котором электроны из раствора переходят на поверхность металла. Таким образом, на поверхности металла формируются участки, где происходит потеря металла (анодные) и участки, где происходит сохранение металла или его накопление (катодные).
Электрохимическая коррозия приводит к постепенному разрушению металла, формированию коррозионных подпалин, изменению его физико-химических свойств, потере прочности и структурных изменений. Она может возникнуть при различных условиях, таких как влажность, высокая температура, наличие агрессивных химических веществ и других факторов.
Понятие электрохимической коррозии
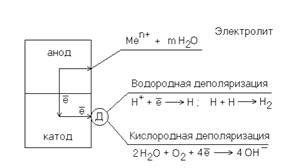
Электрохимическая коррозия - это процесс разрушения металлов под воздействием окружающей среды, происходящий в результате электрохимических реакций. Вследствие этих реакций металлы подвергаются окислению и их поверхность разрушается, что приводит к потере металла и снижению его прочности.
Этот процесс возникает при наличии трех основных компонентов: металла, электролита и кислорода. Когда металл оказывается в контакте с электролитом, начинаются реакции окисления-восстановления, приводящие к образованию электрохимической ячейки. В этой ячейке происходит передача электронов, что приводит к электродной реакции на поверхности металла.
Процесс электрохимической коррозии имеет несколько стадий. Сначала на поверхности металла образуется анодная и катодная области, где происходит окисление и восстановление соответственно. Затем происходит миграция ионов металла в электролит, а также формирование окисленного слоя на поверхности металла.
Электрохимическая коррозия является распространенной проблемой в различных отраслях, таких как строительство, авиация, нефтегазовая промышленность и другие. Процесс коррозии может не только привести к физическому разрушению металлических конструкций, но и вызвать потерю эффективности и безопасности систем и оборудования.
Основные причины электрохимической коррозии

Электрохимическая коррозия – это процесс разрушения материала под воздействием реакций окисления и восстановления в присутствии влаги и электролитов. Этому процессу могут способствовать различные факторы. Рассмотрим основные причины электрохимической коррозии:
- Агрессивная среда: присутствие солей, кислот, щелочей и других химически активных веществ может вызывать разрушение металла путем проведения электрических токов через его поверхность.
- Гальваническая пара: при наличии двух или нескольких металлов, которые находятся в контакте и погружены в электролит, возникает гальваническая пара, что приводит к активной коррозии менее благородного металла.
- Оксидирующие среды: присутствие кислорода в воздухе или воде способствует образованию оксидных пленок на поверхности металла, которые могут обесцвечивать и разрушать его.
- Механические факторы: присутствие трещин, царапин или других повреждений на поверхности металла может способствовать ускоренной электрохимической коррозии.
Понимание основных причин электрохимической коррозии позволяет разработать эффективные методы предотвращения и защиты металлических конструкций от разрушения. Знание взаимодействия между различными металлами, окружающей средой и условиями эксплуатации является важным для технических специалистов, занимающихся проблемами коррозии.
Последствия электрохимической коррозии
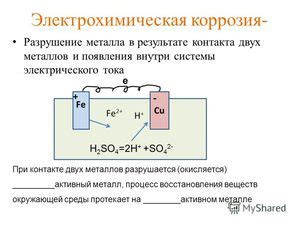
Электрохимическая коррозия металлов является серьезной проблемой, которая может иметь широкий спектр негативных последствий. Она может привести к деградации материала и снижению его механических свойств, что может стать причиной разрушения конструкций и оборудования.
Одним из основных последствий электрохимической коррозии является потеря функциональности металла. Коррозия может привести к появлению трещин, дырок и пятен на поверхности металла, что приводит к его деформации и потере прочности. Это может быть особенно опасно, если коррозия происходит на критически важных деталях, таких как мосты, авиационное оборудование или нефтяные трубопроводы.
Другим негативным последствием электрохимической коррозии является увеличение затрат на обслуживание и ремонт. Поврежденные металлические конструкции требуют дорогостоящего восстановления или замены, что может значительно увеличить бюджеты компаний и организаций. Кроме того, если коррозия происходит на оборудовании, это может привести к простою производства и потере доходов.
Еще одним последствием электрохимической коррозии является угроза окружающей среде и здоровью людей. Коррозия металлов может привести к выделению токсичных веществ в окружающую среду, таких как тяжелые металлы и химические соединения. Это может негативно сказаться на качестве воды, почвы и воздуха, а также привести к развитию различных заболеваний у людей и животных.
Ущерб, причиняемый коррозией

Коррозия металлов – процесс, который может привести к значительному ущербу различным объектам, включая сооружения, транспортные средства, оборудование и даже человеческое здоровье. Она может причинить значительные финансовые потери и вызвать опасные ситуации.
Электрохимическая коррозия металлов поражает их поверхность, приводя к ее разрушению и потере свойств. Данный процесс происходит из-за воздействия влажной среды, являющейся проводником электричества, на металлы. В результате коррозии возникают трещины, отслойки, облупливания и прочие повреждения, которые могут привести к серьезным последствиям.
Поэтому коррозионная защита является важной задачей в различных сферах деятельности. В масштабах производства, коррозия может вызвать аварию, привести к прекращению работы оборудования или снижению качества продукции. В строительстве и инфраструктуре коррозия может привести к разрушению сооружений и необходимости в ремонте или замене. Коррозия также может иметь нежелательное влияние на окружающую среду, загрязняя почву и воду.
Поэтому важно разрабатывать эффективные методы предотвращения коррозии и использовать специальные материалы и покрытия, которые обеспечат надежную защиту от вредного воздействия электрохимической коррозии. Также необходимо осуществлять регулярное обслуживание и контроль состояния металлических объектов, чтобы вовремя выявить и устранить возможные повреждения и предотвратить серьезные последствия.
Способы предотвращения электрохимической коррозии

Электрохимическая коррозия металлов может приводить к серьезным повреждениям и снижению срока службы металлических конструкций. Для предотвращения коррозии существуют различные методы и технологии.
1. Покрытие металла защитным слоем. Нанесение покрытия на металлическую поверхность предотвращает взаимодействие с окружающей средой и образование коррозионных реакций. Популярными методами покрытия являются гальваническое покрытие, гидроизоляционное покрытие и порошковая окраска.
2. Использование антикоррозионных добавок. В процессе изготовления металлических изделий и конструкций можно добавлять специальные вещества, которые замедляют или полностью подавляют процессы коррозии. Это могут быть антиоксиданты, ингибиторы коррозии или водоотталкивающие добавки.
3. Защита электроизоляцией. Если металлическая конструкция находится в условиях, где может происходить контакт с влагой или агрессивными средами, ее можно защитить электроизоляционными материалами. Например, применение специальных покрытий или обмотка мест контакта с другими материалами изоляционными лентами или проводами.
4. Катодная и анодная защита. Для предотвращения коррозии можно использовать специальные системы катодной и анодной защиты. Катодная защита основана на подключении внешнего источника тока к металложидкостному интерфейсу с целью создания отрицательного потенциала на металлической поверхности, что препятствует возникновению коррозионных процессов. Анодная защита, наоборот, предполагает использование положительного потенциала для защиты металла.
5. Регулярное обслуживание и мониторинг состояния Если металлическая конструкция подвержена воздействию влаги, химических веществ или других агрессивных факторов, важно проводить регулярное обслуживание и контролировать состояние поверхностей. Это позволяет своевременно выявить возможные повреждения или признаки коррозии и принять меры по их устранению.
Выбор конкретных методов предотвращения электрохимической коррозии зависит от условий эксплуатации, типа металла и требований к долговечности и надежности конструкции. Использование сочетания нескольких методов может быть наиболее эффективным способом защиты.
Вопрос-ответ

Что такое электрохимическая коррозия?
Электрохимическая коррозия — это процесс разрушения металла, вызванный химическими реакциями между металлом, водой и другими веществами при наличии электрической проводимости.
Какие металлы подвержены электрохимической коррозии?
Подвержены электрохимической коррозии многие металлы, включая железо, алюминий, цинк, медь и т. д. Однако разные металлы имеют разную степень стойкости к коррозии в различных условиях.
Как происходит электрохимическая коррозия?
Электрохимическая коррозия происходит из-за переноса электронов и ионов между металлом и окружающей его средой. В результате этого процесса металл постепенно разрушается и образуются оксидные или соляные отложения на его поверхности.
Как можно защитить металл от электрохимической коррозии?
Существуют различные методы защиты металлов от электрохимической коррозии, например, применение покрытий (как органических, так и металлических), использование антикоррозионных покрытий, применение специальных составов или добавок к металлу, контроль параметров окружающей среды и др.
