Электрохимическая коррозия металлов является серьезной проблемой в промышленности и сельском хозяйстве. Она вызывает повреждения и разрушения металлических конструкций, что приводит к значительным экономическим потерям. В данной статье рассмотрим механизмы электрохимической коррозии, факторы, влияющие на ее развитие, а также способы предотвращения данного процесса.
Электрохимическая коррозия происходит в результате химических реакций между металлом, окружающей средой и электролитом. В результате этих реакций происходит перенос электронов от металла к окружающей среде, что приводит к образованию окислов и солей металла. При этом на поверхности металла образуются коррозионные электроды, а происходящие химические реакции вызывают разрушение материала.
Факторы, влияющие на развитие электрохимической коррозии, включают такие параметры, как влажность, кислотность или щелочность среды, наличие примесей и температура. Влажная среда способствует образованию электролита, кислотность или щелочность окружающей среды повышает активность химических реакций, а примеси и высокая температура создают процессы полимеризации и окисления металла.
Существует ряд способов предотвращения электрохимической коррозии металлов. Один из них - использование специальных реактивов и покрытий, которые создают защитный слой на поверхности металла и препятствуют взаимодействию с окружающей средой. Другой способ - применение антикоррозионных покрытий, таких как краска или лак, которые создают барьер между металлом и окружающей средой. Также эффективным способом является использование специальных сплавов, которые обладают повышенной стойкостью к коррозии.
Электрохимическая коррозия металлов: проблема и способы предотвращения

Электрохимическая коррозия металлов является серьезной проблемой, с которой сталкиваются многие отрасли промышленности. Она возникает при контакте металла с окружающей средой, особенно в присутствии влаги или агрессивных химических веществ. Коррозия приводит к постепенному разрушению металла, что может привести к дорогостоящим повреждениям и аварийным ситуациям.
Для предотвращения электрохимической коррозии металлов применяются различные методы и технологии. Один из основных способов - использование защитных покрытий на поверхности металла. Такие покрытия могут быть нанесены с помощью гальванического осаждения, порошкового покрытия или покрытия с использованием специальных составов. Они создают защитную барьерную пленку, которая предотвращает проникновение влаги и вредных веществ на поверхность металла.
Другой способ предотвращения коррозии - использование антикоррозионных добавок. Эти добавки добавляются в различные материалы, например, в краски, покрытия, антикоррозионные образующие. Они обладают особыми свойствами, которые позволяют создать защиту от коррозии даже при наличии влаги или химически агрессивных сред.
Также для предотвращения электрохимической коррозии металлов, особенно в условиях высоких температур и агрессивной среды, используются специальные сплавы и материалы. Они имеют повышенную стойкость к коррозии и специальные химические свойства, которые помогают сохранить целостность и надежность металлических конструкций.
В целом, предотвращение электрохимической коррозии металлов требует комплексного подхода и применения различных технологий и материалов. Это позволяет увеличить срок службы металлических изделий, защитить их от коррозии и обеспечить надежное функционирование в технических и промышленных системах.
Что такое электрохимическая коррозия металлов?

Электрохимическая коррозия металлов - это процесс разрушения металлических материалов под воздействием электрохимических реакций, возникающих в контакте с окружающей средой. В результате электрохимической коррозии металлов происходит изменение их структуры и свойств, что может привести к снижению прочности и долговечности металлических конструкций и изделий.
Одной из основных причин электрохимической коррозии металлов является образование гальванических пар. При наличии электролита (обычно это влажная среда или растворы солей), разные металлические материалы, находящиеся в контакте, могут образовывать гальваническую пару. В такой паре один металл выступает в роли анода, а другой – в роли катода. По мере прохождения электрического тока через пару, анод начинает растворяться, а на катоде откладываются продукты коррозии.
Электрохимическую коррозию можно условно разделить на два типа: непосредственную и индуктивную коррозию. Непосредственная коррозия происходит при прямом контакте металла с агрессивной средой, например, когда металлическая поверхность погружена в воду или раствор солей. Индуктивная коррозия возникает, когда анод и катод находятся на разных участках металлической конструкции, и между ними проходит электролитическая связь.
Для предотвращения электрохимической коррозии металлов применяют различные методы защиты, включая использование защитных покрытий (например, покраска или гальваническое покрытие), использование антикоррозионных добавок или специальных растворов. Также можно использовать методы электрохимической защиты, такие как катодная и анодная защита, которые основаны на применении внешнего электрического тока для подавления коррозионных процессов.
Влияние электрохимической коррозии на металлы
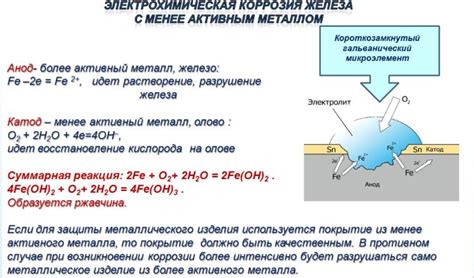
Электрохимическая коррозия является одной из основных проблем для металлических материалов, так как она может привести к их разрушению и деградации. Электрохимическая коррозия возникает при контакте металла с электролитом, что приводит к образованию электродов и возникновению электрохимических реакций. Такой процесс обуславливается разности потенциалов между различными частями металла, а также присутствием кислорода, влаги и других коррозионно-активных веществ.
Одним из наиболее распространенных примеров электрохимической коррозии является ржавчина, которая приводит к окислению и разрушению структуры металла. Коррозия может приводить к образованию трещин, поверхностных дефектов и питтинга, что сокращает прочность и долговечность металлических конструкций и изделий.
Электрохимическая коррозия может иметь серьезные последствия для различных отраслей промышленности, таких как судостроение, аэрокосмическая, нефтегазовая и другие. В результате коррозии могут происходить аварии, снижение эффективности работы оборудования и увеличение затрат на его ремонт и замену.
Для предотвращения электрохимической коррозии применяются различные методы и способы. Одним из них является применение покрытий и защитных слоев на поверхности металла, которые могут уменьшить воздействие электролита и влаги. Также применяются методы катодной и анодной защиты, которые основаны на изменении потенциала металла или применении внешнего источника тока.
Способы предотвращения электрохимической коррозии

Для предотвращения электрохимической коррозии металлов применяются различные методы и технологии. Один из наиболее эффективных способов защиты от коррозии - использование покрытий, которые создают защитный барьер между металлом и агрессивной средой.
Нанесение антикоррозионных покрытий на металлические поверхности позволяет защитить их от контакта с влагой, кислотами, солями и другими агрессивными веществами. Такие покрытия могут быть органическими или неорганическими и наносятся методом нанесения путем покраски, гальванического осаждения или физического напыления.
Один из методов предотвращения коррозии - использование катодной защиты. Этот метод основан на создании на металлической поверхности постоянного электрозащитного потенциала путем подключения внешнего источника электрического тока. Катодная защита применяется в случаях, когда невозможно или невыгодно использовать другие методы предотвращения коррозии.
Для предотвращения электрохимической коррозии металлов также можно применять метод активной и пассивной защиты. Активная защита включает в себя использование различных анодных и катодных материалов, а также наличие комплексного анодно-катодного элемента. Пассивная защита, в свою очередь, основана на образовании на поверхности металла пассивной пленки, которая защищает его от коррозии.
Для предотвращения электрохимической коррозии широко применяются также специальные добавки и ингибиторы коррозии. Эти вещества предотвращают разрушение металлической поверхности путем образования защитной пленки или реагирования с агрессивными веществами, блокируя коррозионные реакции.
Вопрос-ответ

Как возникает электрохимическая коррозия металлов?
Электрохимическая коррозия металлов возникает при наличии влаги и кислорода, а также в результате химических реакций с окружающей средой. Когда металл находится в контакте с электролитом (обычно влагой), возникает электрохимическая реакция, которая разлагает металл на ионы и электроны. Этот процесс может привести к разрушению металлической поверхности и потере его механических свойств.
Какие металлы подвержены электрохимической коррозии?
Большинство металлов подвержены электрохимической коррозии, особенно если они находятся в контакте с влагой или агрессивными химическими средами. Некоторые из самых подверженных коррозии металлов включают сталь, железо, алюминий, медь, цинк, свинец, никель и магний. Однако существуют и сплавы, которые обладают высокой стойкостью к коррозии, например, нержавеющая сталь или алюминиевые сплавы с добавкой магния.
Каковы способы предотвращения электрохимической коррозии металлов?
Существует несколько способов предотвращения электрохимической коррозии металлов. Один из них - использование защитных покрытий, таких как краска, эмаль, порошковое напыление или гальваническое покрытие. Эти покрытия создают барьер между металлом и окружающей средой, предотвращая контакт с водой или агрессивными химическими веществами. Еще одним способом является использование антикоррозионных добавок или ингибиторов, которые могут уменьшить активность химических реакций, происходящих на поверхности металла. Также возможно использование анодной защиты, при которой металл превращается в анод и защищается от коррозии посредством подключения к внешнему источнику тока.
