При изучении элементов и их свойств в химии мы наталкиваемся на понятие электроотрицательности, которое играет важную роль в объяснении химических реакций и соединений. Одним из ключевых различий между неметаллами и металлами является их электроотрицательность.
Электроотрицательность – это способность атома притягивать электроны к себе при образовании химических связей. Неметаллы, такие как кислород, азот, сера и хлор, обладают электроотрицательностью ниже двух. Это означает, что они имеют склонность притягивать электроны и образовывать отрицательные ионы. В свою очередь, металлы, такие как натрий, железо и алюминий, имеют электроотрицательность выше двух, что делает их склонными отдавать электроны и образовывать положительные ионы.
Различие в электроотрицательности обусловлено особенностями строения атомов неметаллов и металлов. Атомы неметаллов обладают высокой электронной плотностью и малым размером, что делает их более электроотрицательными. В металлах же электронная плотность низкая, а размер атомов большой, что ослабляет их способность притягивать электроны.
Таким образом, неметаллы и металлы различаются по своей электроотрицательности. Неметаллы притягивают электроны, образуя отрицательные ионы, в то время как металлы отдают электроны, образуя положительные ионы.
Обобщение про электроотрицательность

Электроотрицательность является важной характеристикой элементов в химии. Она указывает на способность атома притягивать к себе электроны в химической связи. Неметаллы обычно имеют электроотрицательность ниже двух, в то время как у металлов она всегда выше двух.
Высокая электроотрицательность у металлов связана с их способностью отдавать электроны в химических реакциях. Металлы стремятся образовывать положительные ионы, отдавая свои валентные электроны. Это объясняет их свойство быть хорошими проводниками электричества и тепла.
Неметаллы, с другой стороны, имеют более низкую электроотрицательность и обычно стремятся получить или разделить электроны других атомов. Они образуют отрицательные ионы или делят свои электроны с другими элементами, чтобы достичь устойчивости.
Электроотрицательность является основой для определения полярности химических связей и молекул. Когда два атома с разной электроотрицательностью образуют связь, возникают дипольные моменты и отрицательные и положительные заряды. Это делает такие связи полярными, что важно для понимания свойств и реакций соединений.
Единицей измерения электроотрицательности является шкала Полинга. На этой шкале самая высокая электроотрицательность имеет флуор, значения которого равны 4.0. Самая низкая электроотрицательность у франция, которой принимается значение 0.7.
Понимание электроотрицательности и ее роли в химических связях помогает химикам предсказывать свойства и реактивность веществ. Эта характеристика позволяет определить, какие элементы будут склонны образовывать ионные и ковалентные связи, а также понять, как разные элементы могут взаимодействовать друг с другом.
Неметаллы с электроотрицательностью ниже двух

Неметаллы - это элементы, которые в их чистом состоянии не обладают металлическими свойствами. Их электроотрицательность, то есть способность притягивать электроны, обычно ниже значения два.
Электроотрицательность является важной характеристикой элемента, определяющей его химическую активность и способность образовывать химические связи с другими элементами. Неметаллы с низкой электроотрицательностью имеют тенденцию притягивать электроны слабее, чем металлы и другие неметаллы с более высокой электроотрицательностью.
Примеры неметаллов с электроотрицательностью ниже двух включают в себя элементы, такие как водород, углерод, нитроген, кислород и фтор. Водород, наименьший и самый легкий элемент в периодической системе, имеет электроотрицательность 2,2. Углерод, играющий важную роль в органической химии, имеет электроотрицательность 2,55. Группа элементов, известных как галогены, такие как фтор с электроотрицательностью 3,98, также относятся к неметаллам с низкой электроотрицательностью.
Неметаллы с низкой электроотрицательностью играют важную роль в химических реакциях и образовании соединений. Они часто образуют ковалентные связи, в которых электроны между атомами разделяются равномерно или более равномерно, что позволяет образовать молекулярные соединения и сложные структуры.
- Водород, углерод, нитроген, кислород и фтор - примеры неметаллов с электроотрицательностью ниже двух.
- Неметаллы с низкой электроотрицательностью обычно образуют ковалентные связи и сложные структуры.
- Их способность притягивать электроны слабее, чем у металлов и других неметаллов с более высокой электроотрицательностью.
- Неметаллы с низкой электроотрицательностью играют важную роль в химических реакциях и органической химии.
Металлы с электроотрицательностью выше двух

Металлы, в отличие от неметаллов, обладают электроотрицательностью, которая всегда превышает значение двух. Это одно из ключевых отличий между металлами и неметаллами и определяет их химические свойства и способы взаимодействия с другими элементами.
Высокая электроотрицательность металлов обусловлена их структурой и расположением элементов в периодической системе. Металлы находятся слева от линии разделения в периодической системе, а неметаллы - справа. С ростом электроотрицательности элемент прогрессивно приближается к правой стороне периодической системы. Поэтому металлы имеют более низкую электроотрицательность.
Коэффициент электроотрицательности позволяет оценить способность атома притягивать электроны в химической связи. У металлов электроотрицательность обычно находится в диапазоне от 1,5 до 2,8. Это значительно меньше, чем у неметаллов, чья электроотрицательность может достигать значений выше четырех.
Металлы с высокой электроотрицательностью обладают способностью образовывать ионные соединения с неметаллами, перенося электроны на неметаллы в химической реакции. Таким образом, металлы играют важную роль во многих процессах, включая коррозию, образование растворов и окисление.
Важно отметить, что электроотрицательность является лишь одним из показателей химической активности элементов. Она определяет, как элемент будет вступать в химические реакции, но не может полностью описать его всю химическую сущность. Металлы с высокой электроотрицательностью могут быть как активными, так и менее активными в зависимости от других факторов, таких как размер атома, структура решётки и особенности химической связи.
Реакции неметаллов и металлов
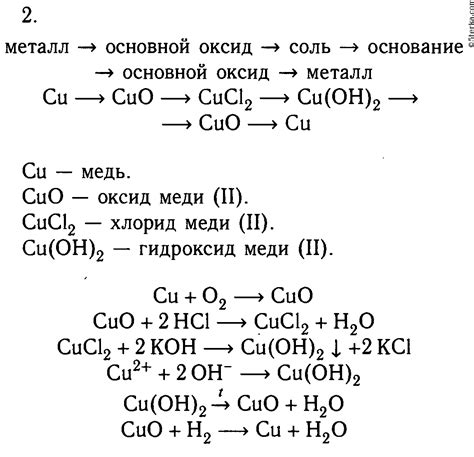
Неметаллы - это группа элементов, характеризующаяся электроотрицательностью ниже двух. Они обладают большими валентностями и образуют соединения с металлами и другими неметаллами. Реакции неметаллов могут быть очень разнообразными и иметь различную степень активности.
Одним из наиболее известных неметаллов является кислород. Он образует множество соединений с металлами, так как является сильным окислителем. Реакции кислорода с металлами могут протекать с образованием оксидов, пероксидов или гидроксидов в зависимости от условий.
Ещё одним неметаллом является сера. Она также способна образовывать соединения с металлами, например, серные соединения. Реакции серы с металлами могут протекать с образованием сульфидов или тионатов.
Металлы, в отличие от неметаллов, обладают электроотрицательностью выше двух. Они обычно являются хорошими проводниками электричества и тепла, а также могут дать электроны сравнительно легко.
Реакции металлов с неметаллами могут быть различного характера. Например, металлы могут реагировать с кислородом, образуя оксиды. Также они могут реагировать с несколькими неметаллами одновременно и образовывать сложные соединения.
Важно отметить, что электроотрицательность неметаллов и металлов является ключевым фактором при определении их способности образовывать соединения друг с другом. Эта разница в электроотрицательности определяет направленность электронного переноса и химическую активность веществ.
Физические свойства неметаллов и металлов
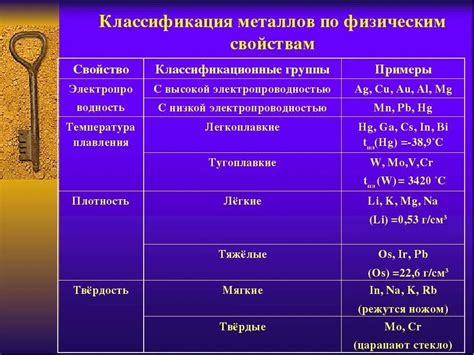
Неметаллы – это группа элементов, обладающих несколькими характерными физическими свойствами. Одно из таких свойств – низкая электроотрицательность, которая означает слабую способность притягивать электроны. Это обусловлено строением и составом атомов неметаллов. Однако у каждого неметалла есть своя определенная электроотрицательность, которая может меняться в зависимости от конкретного элемента.
Примеры неметаллов:
- Кислород (O) – один из самых распространенных элементов в природе. Он обладает высокой электроотрицательностью и легко вступает в реакции с металлами.
- Углерод (C) – ключевой элемент органических соединений. Он имеет способность образовывать длинные цепочки и разнообразные структуры, что позволяет создавать различные материалы.
- Азот (N) – важный элемент в составе белков и нуклеиновых кислот, играет роль в метаболических процессах организмов.
Металлы, в отличие от неметаллов, обладают высокой электроотрицательностью. Это связано с их способностью легко отдавать электроны, что обусловлено строением атомов металлов и наличием свободных электронов в их внешнем энергетическом уровне.
Примеры металлов:
- Железо (Fe) – один из наиболее распространенных и важных металлов. Он обладает высокой прочностью, хорошей проводимостью электричества и тепла, что делает его идеальным материалом для различных конструкций и оборудования.
- Алюминий (Al) – легкий и прочный металл, широко используемый в промышленности и строительстве. Он обладает хорошей коррозионной стойкостью и является отличным проводником тепла и электричества.
- Медь (Cu) – мягкий и пластичный металл, который отличается высокой электропроводностью. Он используется в производстве электроники, проводов и различных изделий.
Таким образом, различия в электроотрицательности между неметаллами и металлами являются основным физическим свойством, отличающим эти две группы элементов. Это свойство определяет способность этих элементов вступать в химические реакции и образовывать соединения с другими элементами.
Использование неметаллов и металлов в промышленности

Неметаллы и металлы играют важную роль в различных отраслях промышленности. Неметаллы, благодаря своим особым свойствам, нашли применение в производстве электроники, космической техники, стекла и других материалов.
Один из самых важных неметаллов, который широко используется в промышленности, это кремний. Кремний является основным материалом для производства полупроводников, которые необходимы в современной электронике. Кремний также используется для создания солнечных батарей, стекла и других материалов с высокой прочностью и стабильностью.
В то же время, металлы имеют широкое применение в различных отраслях промышленности. Металлы, такие как железо, алюминий и медь, используются для создания конструкций, машин и различных изделий. Железо, благодаря своей прочности и устойчивости к коррозии, является основным материалом в строительстве зданий, производстве автомобилей и многих других промышленных отраслях.
Кроме того, металлы применяются в производстве электрических проводов и контактов благодаря своей хорошей электропроводности. Медь, например, является одним из наиболее использованных металлов в производстве электрических проводов.
Таким образом, неметаллы и металлы имеют ключевое значение в промышленности. Они предоставляют нам различные материалы и изделия, необходимые для повседневной жизни и развития технологий. Благодаря своим уникальным свойствам, они помогают создавать устойчивые и функциональные материалы, которые находят широкое применение в различных отраслях промышленности.
Вопрос-ответ

Что такое электроотрицательность и зачем она нужна?
Электроотрицательность - это способность атома притягивать электроны к себе. Она нужна для описания химических свойств веществ и определения их типа - металлов или неметаллов.
Почему неметаллы имеют электроотрицательность ниже двух?
Неметаллы характеризуются низкой электроотрицательностью, так как они имеют большую связывающую силу между электронами и ядрами. Это связано с особенностями электронной структуры атомов неметаллов.
Почему у металлов электроотрицательность всегда выше двух?
Металлы обладают высокой электроотрицательностью, так как они имеют малую связывающую силу между электронами и ядрами. В результате, металлы легко отдают электроны, образуя положительно заряженные ионы.
Как электроотрицательность влияет на свойства веществ?
Электроотрицательность влияет на химические свойства веществ. Неметаллы с высокой электроотрицательностью обычно образуют ковалентные связи и проявляют неметаллические свойства, такие как нежность, хрупкость, низкую температуру плавления и кипения. Металлы же, с низкой электроотрицательностью, имеют металлическую связь и обладают металлическими свойствами, такими как хорошая проводимость тепла и электричества, гибкость и блеск.
