Электронная конфигурация переходных металлов определяет их химические свойства и способность образовывать соединения. Внешняя оболочка переходного металла содержит электроны, которые участвуют в химических реакциях и определяют его атомные и молекулярные свойства. Знание электронной конфигурации переходных металлов является ключевым вопросом для всех студентов и специалистов в области химии.
Пройти тест на знание электронной конфигурации внешней оболочки переходного металла поможет вам систематизировать знания и проверить уровень понимания этой важной темы. Тест состоит из нескольких вопросов, которые охватывают основные аспекты электронной конфигурации переходных металлов, такие как количество электронов в внешней оболочке, квантовые числа, электронные конфигурационные правила и распределение электронов в орбиталях.
Правильные ответы помогут расширить вашу базу знаний и улучшить понимание электронной конфигурации переходных металлов. Тест также может быть полезен для подготовки к экзаменам или освежения знаний перед выполнением лабораторных работ или научных исследований.
Электронная конфигурация внешней оболочки переходного металла и зачем она нужна?
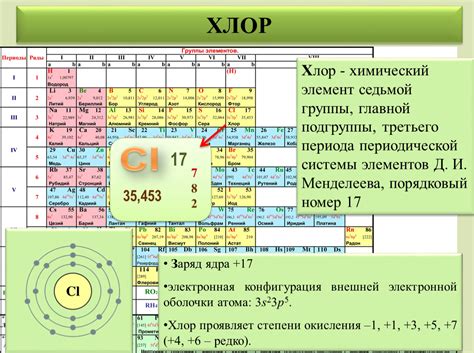
Электронная конфигурация внешней оболочки переходного металла определяет, сколько электронов находится во внешнем энергетическом уровне атома металла. Такая конфигурация играет особую роль в химических и физических свойствах переходных металлов.
Внешняя оболочка переходного металла состоит из d- и f-орбиталей, которые могут быть заполнены различным количеством электронов. Электроны в этих орбиталях способны участвовать в химических реакциях и создавать разнообразные соединения с другими элементами.
Электронная конфигурация внешней оболочки переходного металла определяет его химическую активность, способность образовывать соединения и проявлять свои уникальные каталитические свойства. Кроме того, электронная конфигурация внешней оболочки определяет положение переходного металла в таблице элементов и его химические свойства.
Знание электронной конфигурации внешней оболочки переходного металла позволяет установить его положение в периодической системе элементов, предсказать его способность формировать различные типы соединений, а также понять, почему переходные металлы обладают уникальными свойствами, которые делают их полезными в различных областях науки и техники.
Принципы построения электронной конфигурации

Электронная конфигурация внешней оболочки переходного металла определяется принципами построения, основанными на энергетической структуре атомов. Внешняя оболочка переходного металла состоит из s- и d-орбиталей, которые характеризуются разными энергетическими уровнями и заполняются по определенным правилам.
Основные принципы построения электронной конфигурации внешней оболочки переходного металла включают принцип заполнения по возрастанию энергии, принцип исключения Паули и принцип Хунда. Принцип заполнения по возрастанию энергии означает, что электроны в поперечных орбиталях заполняются сначала в орбиталь с более низкой энергией, а затем в орбитал с более высокой энергией.
Принцип исключения Паули гласит, что каждому электрону в атоме должно соответствовать уникальное квантовое состояние, то есть два электрона не могут иметь одинаковые квантовые числа. Это означает, что каждая орбиталь может содержать не более двух электронов с разными спинами.
Принцип Хунда определяет, что электроны заполняют орбитали одного энергетического уровня по отдельности сначала в орбитали одного спина, а затем в орбитали другого спина. Этот принцип обусловлен энергетическими условиями и минимизацией энергии.
При построении электронной конфигурации внешней оболочки переходного металла следует учитывать эти принципы, чтобы определить количество электронов, их распределение по орбиталям и спиновые состояния.
Как понять электронную конфигурацию внешней оболочки переходного металла?
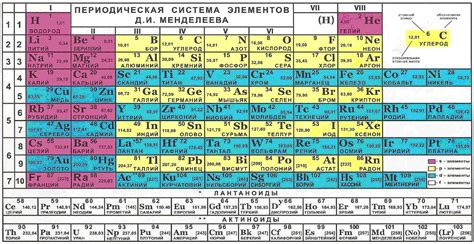
Электронная конфигурация внешней оболочки переходного металла определяет его свойства и реактивность в химических реакциях. Понимание электронной конфигурации помогает понять, какие электроны доступны для участия в химических связях и реакциях.
Внешняя оболочка переходного металла обычно состоит из d-электронов, которые находятся на уровне энергии выше заполненных s- и p-оболочек. Для определения электронной конфигурации можно использовать таблицу Менделеева и знания о расположении элементов в периодической системе.
Например, для определения электронной конфигурации меди (Cu), можно найти его положение в таблице Менделеева и узнать, что у него атомный номер 29. Это означает, что в атоме меди имеется 29 электронов.
Также можно использовать принцип заполнения орбиталей, который позволяет определить порядок заполнения электронов в атоме. Переходные металлы имеют сложную электронную конфигурацию из-за особенностей энергетических уровней d-орбиталей.
Понимание электронной конфигурации внешней оболочки переходного металла важно для понимания его свойств и способности образовывать химические связи. Оно помогает предсказывать его реактивность и взаимодействия с другими веществами.
Как правильно пройти тест на электронную конфигурацию внешней оболочки переходного металла?
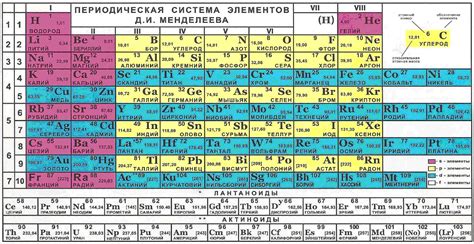
Тест на электронную конфигурацию внешней оболочки переходного металла включает в себя вопросы о расположении электронов внешней оболочки атомов данных металлов. Чтобы успешно пройти тест, необходимо иметь хорошие знания о распределении электронов и особенностях переходных металлов в таблице Менделеева.
Во-первых, рекомендуется внимательно изучить таблицу Менделеева и запомнить электронную конфигурацию внешней оболочки каждого переходного металла. Особое внимание следует обратить на номер элемента и количество электронов в атоме.
Во-вторых, полезно упражняться в записи электронной конфигурации переходных металлов. При этом можно использовать сокращенную нотацию для упрощения записи. Например, вместо полной записи "1s2 2s2 2p6 3s2 3p6 4s2 3d10" для атома циркония (Zr), можно использовать сокращенную запись "[Kr] 5s2 4d2".
Также рекомендуется осуществлять практику с решением задач на определение электронной конфигурации переходного металла. Для этого можно использовать онлайн-ресурсы, учебники или тренировочные задания, которые помогут закрепить полученные знания и научиться правильно определять распределение электронов во внешней оболочке атомов переходных металлов.
Важно также внимательно читать вопросы теста, чтобы понять, что именно требуется. Ответы на вопросы могут быть представлены в различных форматах, например, в виде чисел, символов элементов, сокращенной нотации или других обозначений. Необходимо быть готовым к различным вариантам ответов.
Итак, чтобы правильно пройти тест на электронную конфигурацию внешней оболочки переходного металла, необходимо иметь хорошие знания об электронной конфигурации переходных металлов, уметь записывать их сокращенно, регулярно практиковаться в решении задач и внимательно читать вопросы теста. Удачи!
Вопрос-ответ

Что такое электронная конфигурация внешней оболочки переходного металла?
Электронная конфигурация внешней оболочки переходного металла описывает расположение электронов на самом внешнем энергетическом уровне атома этого металла. Она определяет его химические свойства и способность образовывать химические связи.
Каким образом можно определить электронную конфигурацию внешней оболочки переходного металла?
Электронную конфигурацию внешней оболочки переходного металла можно определить, зная порядковый номер элемента в периодической системе. Она соответствует количеству электронов на последнем энергетическом уровне этого элемента. Например, для железа (Fe) с порядковым номером 26 конфигурация внешней оболочки будет 3d6 4s2.
Какая роль электронной конфигурации внешней оболочки переходного металла в его химических свойствах?
Электронная конфигурация внешней оболочки переходного металла определяет его химические свойства. Наличие неполной оболочки электронов (так называемые незаполненные d-подуровни) позволяет переходным металлам образовывать разнообразные химические связи и проявлять свою валентность. Такие металлы обладают высокой реакционной активностью и могут участвовать во многих химических реакциях.
