Электрокоррозия металла – это процесс разрушения и разложения металлических материалов вследствие химической реакции между металлом и окружающей средой при наличии электрического тока. Этот процесс является одной из наиболее распространенных причин разрушения металлических конструкций и поверхностей.
При электрокоррозии металл подвергается окислительным процессам, которые вызывают разрушение его структуры и образование коррозионных осадков. Изначально электрокоррозия ведет к образованию микроскопических дефектов на поверхности металла, которые затем увеличиваются и приводят к образованию пузырьков, трещин и пятен коррозии.
Бороться с электрокоррозией металла можно различными способами. Одним из основных методов является использование антикоррозионных покрытий, которые препятствуют взаимодействию металла с окружающей средой. Другим способом является использование анодной защиты, при которой металл обменивается на другое вещество, предотвращая его коррозию. Также можно применять катодную защиту, при которой металл превращается в катод и не подвергается электрокоррозии.
Электрокоррозия металла: проблема с повреждением
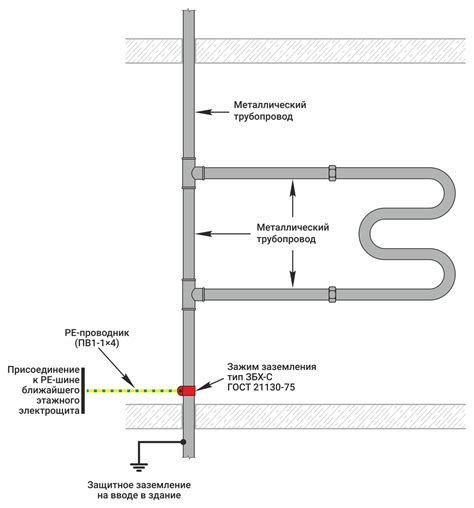
Электрокоррозия металла представляет собой серьезную проблему, которая может привести к повреждению различных конструкций и оборудования. Она возникает из-за химических реакций, происходящих между металлическими поверхностями и электролитами, такими как вода или влажный воздух.
В результате электрокоррозии металла происходит процесс разрушения металлической поверхности, что может привести к образованию выбоин, трещин или ослаблению конструкций. Это особенно проблематично в случае использования металла в строительстве или в промышленности, где надежность и долговечность материалов играют важную роль.
Чтобы бороться с проблемой электрокоррозии металла, необходимо применять различные защитные меры. Например, можно использовать специальные покрытия, такие как краска или порошковое покрытие, которые создадут защитный барьер между металлической поверхностью и окружающей средой.
Также электрокоррозию можно предотвратить путем использования таких методов, как катодная защита или анодирование. При катодной защите на металлическую поверхность наносится слой активного материала, который выступает в качестве катода и принимает на себя все электрические токи, предотвращая тем самым коррозию металла.
Анодирование, в свою очередь, заключается в процессе оксидации металла в анодных условиях. Это создает защитный слой оксида на поверхности металла, который предотвращает его коррозию.
Что такое электрокоррозия металла

Электрокоррозия металла является одной из основных причин разрушения металлических конструкций и изделий. Это электрохимический процесс, при котором металл под действием внешнего электрического поля переходит в состояние коррозии.
Основным механизмом электрокоррозии является передача электрических зарядов через электролит - среду, в которой находится металл. Электролитом может служить вода, почва, атмосферный воздух и другие среды, содержащие ионы.
При наличии разности потенциалов между различными участками поверхности металла, возникают гальванические элементы, которые активируют процесс коррозии. Этот процесс приводит к образованию окисных пленок на поверхности металла и последующему разрушению материала.
Особенно чувствительными к электрокоррозии являются металлы с различной электрохимической активностью, такие как железо, алюминий и оцинкованная сталь. Более активный металл оказывает защитное воздействие на менее активный металл, приводя к его разрушению.
Контроль и предотвращение электрокоррозии металла включает в себя применение защитных покрытий (например, красок или эмалей), установку анодных защитных систем, использование антикоррозионных ингибиторов и более активного металла, а также правильную эксплуатацию и обслуживание металлических конструкций.
Влияние влажности и кислотности на электрокоррозию

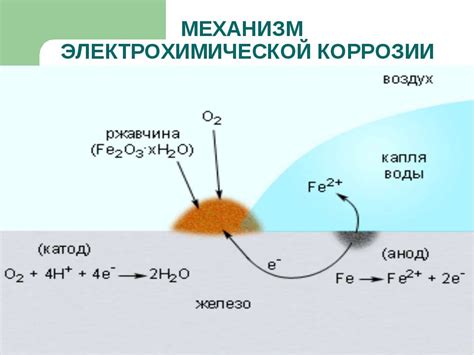
Влажность и кислотность в окружающей среде существенно влияют на процесс электрокоррозии металла. Влага является одним из основных факторов, способствующих возникновению и развитию коррозии. Когда металл находится в присутствии влаги, образуется электролит, который служит проводником для электрического тока между анодом и катодом. В результате происходит электрохимическая реакция, которая приводит к разрушению металла.
Компоненты, содержащиеся в воде, такие как растворенные соли и газы, могут дополнительно ускорять процесс электрокоррозии. Вода, обогащенная солями, например, становится электролитом более высокой концентрации, что приводит к более интенсивному разложению металла. Кроме того, наличие кислых компонентов в воде может вызывать коррозию катодов, что также способствует ускорению электрокоррозии.
Кислотность окружающей среды также является значимым фактором, влияющим на электрокоррозию металла. Кислый раствор, обладающий низким pH, образует агрессивную среду, которая ускоряет разложение металла. Кислотная среда способна разрушить защитные покрытия на поверхности металла и обнажить его, что приводит к дальнейшей электрокоррозии.
Для борьбы с электрокоррозией, необходимо обеспечить защиту металла от воздействия влаги и кислотности. В качестве методов защиты используются покрытия, пассивационные слои, антикоррозионные покрытия и специальные добавки, которые придают металлу защитные свойства. Важно также поддерживать оптимальную влажность и избегать воздействия кислых сред, чтобы предотвратить разрушение металлических конструкций и предметов.
Основные причины электрокоррозии металла:

1. Гальваническая пара: Одна из главных причин электрокоррозии металла - образование гальванической пары. Это происходит, когда два различных металла соприкасаются во влажной среде. В таком случае, более активный металл (анод) начинает выделять электроны, которые переносятся на менее активный металл (катод), что приводит к разрушению анода.
2. Электролиты: Наличие электролитов, таких как вода с солями или кислотами, сильно увеличивает скорость электрокоррозии металла. Электролиты обеспечивают участие в химических реакциях, необходимых для образования и распространения коррозии.
3. Неравномерное покрытие: Если металлическое покрытие на поверхности изделия неравномерно, то это может создать условия для возникновения электрокоррозии. Недостатки в покрытии могут привести к накоплению электролитического раствора, что приводит к образованию коррозионных очагов.
4. Механическое повреждение: Механическое повреждение металлической поверхности, такое как царапины или трещины, может привести к нарушению защитного покрытия и выявить металл на действие коррозии. При наличии влаги или электролитов, электрокоррозия начнется с места повреждения и продолжится по всей поверхности металла.
5. Воздействие окружающих условий: Электрокоррозию металла могут существенно ускорять факторы внешней среды, такие как высокая влажность, серная пыль, морская среда, кислотные дожди и т. д. Эти условия способствуют более активному выделению электронов и увеличению скорости коррозии.
Последствия электрокоррозии для металлических изделий

Электрокоррозия – это процесс разрушения металлических изделий, вызванный воздействием электрического тока и коррозивной среды. Несмотря на свою невидимость, электрокоррозия может иметь серьезные последствия для металлических конструкций.
Первым и наиболее очевидным последствием электрокоррозии является потеря эстетического вида и повреждение внешней поверхности металла. Появление пятен, ржавчины, шероховатости и коррозионных пузырей сделает металлическую поверхность непригодной для использования в декоративных целях или придания эстетического вида здания или изделия.
Кроме того, электрокоррозия способна привести к разрушению металлических конструкций. Коррозия ослабляет структуру металла, делая его более хрупким и подверженным механическим повреждениям. Это может привести к обрушению здания или поломке металлических устройств и механизмов.
Другими негативными последствиями электрокоррозии является снижение эффективности металлических устройств и систем. Зачастую, за счет воздействия коррозии на проводимость электрического тока, происходит ухудшение контакта и повышение сопротивления в металлических соединениях. Это может привести к значительному снижению производительности и эффективности электрических систем.
Также стоит отметить, что электрокоррозия может вызвать утечку или контаминирование хранящихся в металлических емкостях или трубопроводах жидкостей или газов. Ржавые трубы или оборудование, подверженное коррозии, могут стать источником отравления или загрязнения воды, пищевых продуктов или других сред.
Методы борьбы с электрокоррозией металла
1. Покрытие металла
Один из наиболее эффективных способов борьбы с электрокоррозией металла - покрытие его защитными материалами.
Покрытие может быть нанесено с помощью различных методов, таких как покраска, гальванизация или нанесение покрытий методом плазменного напыления.
Защитные покрытия создают барьер между металлом и окружающей средой, предотвращая проникновение влаги и агрессивных химических веществ на поверхность металла, что снижает риск электрокоррозии.
2. Изоляция металла
Другим методом борьбы с электрокоррозией металла является его изоляция.
Изоляция может быть достигнута с помощью различных материалов, таких как пластик, резина или эпоксидная смола.
Эти материалы предотвращают прямой контакт металла с окружающей средой, создавая электрическую изоляцию и позволяя избежать протекания электрического тока и последующей коррозии.
3. Использование анодной защиты
Анодная защита - это метод, который основан на введении в систему зажигания металла второго металлического элемента, который будет подвергаться коррозии вместо основного металла.
Это осуществляется путем подключения специального источника тока, который делает "анод" положительным и защищаемый металл - "катод" отрицательным.
Это позволяет снизить скорость коррозии основного металла, за счет того, что второй металлический элемент принимает на себя роль жертвенного анода.
4. Модификация окружающей среды
Изменение окружающей среды также является важным аспектом борьбы с электрокоррозией металла.
Контроль влажности, температуры и содержания агрессивных химических веществ вокруг металла может значительно снизить риск коррозии.
Использование осушителей воздуха, теплоизоляционных материалов и применение добавок, которые уменьшают концентрацию вредных веществ, помогут защитить металл от электрокоррозии.
Профилактика электрокоррозии металлических поверхностей

Для предотвращения электрокоррозии металлических поверхностей необходимо принять несколько мер. Во-первых, важно правильно подготовить поверхность перед ее эксплуатацией. Это включает в себя удаление грязи, ржавчины, старой краски или защитного покрытия.
Во-вторых, следует нанести на металлическую поверхность антикоррозийное покрытие. Оно защитит металл от воздействия влаги, кислот и щелочей. При выборе покрытия нужно учитывать конкретные условия эксплуатации и свойства металла.
Важным этапом профилактики электрокоррозии является применение катодной защиты. Катодный защитный слой наносится на поверхность металла и препятствует коррозии путем создания электрической гальванической ячейки, где металл выступает в роли катода. Это позволяет значительно продлить срок службы металлических конструкций.
Для эффективной профилактики электрокоррозии металла можно также использовать систему катодной защиты на основе анодов. Аноды размещаются вблизи металлической поверхности и компенсируют потери электронов, что способствует сохранению целостности металла.
Кроме того, существует возможность применения двухслойных покрытий, где один слой является активным, а второй – защитным. Активный слой называют анодным, он позволяет замедлить или полностью остановить процесс коррозии, а защитный слой обеспечивает долговременную защиту металла от внешней среды.
Вопрос-ответ

Что такое электрокоррозия и как она возникает?
Электрокоррозия - это процесс разрушения металла под воздействием электрического тока. Она возникает при взаимодействии различных металлических элементов, когда один из них работает как анод, а другой - как катод. При этом происходит анодное окисление, что приводит к разрушению металла.
Какие металлические изделия подвержены электрокоррозии?
Подвержены электрокоррозии различные металлические изделия, такие как трубы, баки, судовое оборудование и другие конструкции, находящиеся в контакте с водой или почвой. Также металлы с разной химической активностью, находящиеся вблизи друг друга, могут стать источником электрокоррозии.
Какие меры предпринять для предотвращения электрокоррозии?
Для предотвращения электрокоррозии можно применять различные меры. Важно выбрать правильный материал для конструкции, учитывая его химическую активность и свойства. Также можно использовать специальные защитные покрытия на металлических изделиях, такие как краска или антикоррозийные покрытия. Дополнительно можно устанавливать так называемые "жертвенные аноды", которые будут работать как аноды и защищать основные металлические элементы от коррозии.
Какую роль играет температура и влажность в процессе электрокоррозии?
Температура и влажность являются важными факторами в процессе электрокоррозии. Высокая температура ускоряет процесс коррозии, поскольку ускоряет реакции окисления металла. Высокая влажность создает благоприятные условия для электрокоррозии, поскольку вода является хорошим проводником электрического тока.
Как можно контролировать электрокоррозию в промышленных объектах?
Для контроля электрокоррозии в промышленных объектах используются различные методы. Это включает системы мониторинга и контроля, регулярную проверку и обслуживание оборудования, а также применение антикоррозийных покрытий и защитных систем. Также проводятся специальные обследования и анализы для определения уровня коррозии и принятия соответствующих мер.
