Оксиды и основания являются важными компонентами химии, и их взаимодействие может привести к различным химическим реакциям. Действие оксида на основание происходит при контакте двух веществ, которые могут проявлять свои химические свойства.
Оксиды - это химические соединения, состоящие из кислорода и другого элемента. Они могут иметь разные степени окисления, что влияет на их реакционную способность. Основания, с другой стороны, являются веществами, которые обладают щелочными свойствами и способны выделять гидроксиды ионов.
Когда оксид контактирует с основанием, происходит химическая реакция, в результате которой образуется соль и вода. При этом оксид обладает кислотными свойствами и образует кислотный оксид. Эта реакция является высокоэкзотермической и может сопровождаться выделением тепла или света.
Примерами реакций действия оксида на основание могут быть реакция между оксидом кальция (CaO) и водой (H2O), в результате которой образуется гидроксид кальция (Ca(OH)2). Еще одним примером является реакция между оксидом алюминия (Al2O3) и щелочью NaOH, в результате которой образуется натрий алюминат (NaAlO2).
Определение оксида и основания

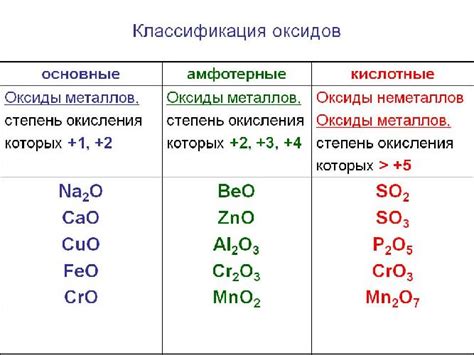
Оксид - это химическое вещество, составленное из металлического элемента и кислорода. Оксиды могут быть основными, кислотными или амфотерными в зависимости от того, какое химическое действие они проявляют.
Основание - это химическое вещество, которое может реагировать с кислотами, образуя соль и воду. Основания обычно содержат гидроксидный ион (OH-), который является донором гидроксильной группы.
Оксиды и основания играют важную роль в химических реакциях, так как они могут образовывать соли и воду при взаимодействии между собой. Например, когда оксид металла вступает в реакцию с основанием, образуется соль и вода.
Оксиды и основания также находят применение в различных областях науки и промышленности. Например, оксиды металлов используются в качестве катализаторов при производстве химических веществ, в производстве стекла и керамики, а также в электроэнергетике.
Таким образом, понимание определений оксида и основания является важным для понимания химических реакций и их применений в различных областях науки и промышленности.
Взаимодействие оксида с основанием
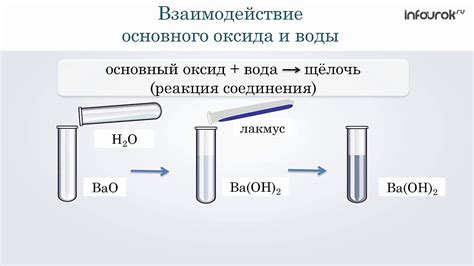
Взаимодействие оксида с основанием является одной из основных реакций в химии. В результате этого взаимодействия происходит образование соли и воды. Оксиды представляют собой химические соединения, состоящие из кислорода и другого элемента. Они могут быть кислотными, щелочными или амфотерными.
Оксиды взаимодействуют с основаниями, которые представляют собой соединения, содержащие гидроксильные группы. При взаимодействии оксида с основанием происходит реакция нейтрализации. Кислотные оксиды реагируют с основаниями, образуя соль и воду. Щелочные оксиды также образуют соль и воду, но при этом происходит образование гидроксида металла.
Реакция взаимодействия оксида с основанием может быть представлена следующим уравнением: Оксид + Основание → Cоль + Вода. Например, взаимодействие кислотных оксидов с основаниями приводит к образованию солей с общей формулой M(OH)2, где M - металл. Щелочные оксиды, такие как оксид натрия или оксид калия, при реакции с водой образуют гидроксиды NaOH или KOH соответственно.
Примеры реакций оксида с основанием
1. Реакция между оксидом кальция и водой:
Оксид кальция (CaO), химически известный как известь, вступает в реакцию с водой, образуя гидроксид кальция (Ca(OH)2). Реакция происходит с выделением тепла и называется гашением извести.
2. Реакция между оксидом алюминия и натриевым гидроксидом:
Оксид алюминия (Al2O3), известный как глина или красная глина, реагирует с натриевым гидроксидом (NaOH) при нагревании, образуя натрия солянокислый алюминат (Na3Al(OH)6). Эта реакция используется для получения гидроксида алюминия, который широко применяется в производстве бумаги и кожи.
3. Реакция между оксидом железа и калиевым гидроксидом:
Оксид железа (Fe2O3), известный как ржавчина, реагирует с калиевым гидроксидом (KOH), образуя калий феррит (KFeO2). Эта реакция используется для получения калий-железных аккумуляторов, которые широко применяются в электротехнике.
4. Реакция между оксидом серы и калиевым гидроксидом:
Оксид серы (SO2), образующийся при сжигании серы, реагирует с калиевым гидроксидом (KOH), образуя калий сульфит (K2SO3) и воду. Эта реакция используется для очистки дымовых газов от сернистого газа.
5. Реакция между оксидом азота и аммиаком:
Оксид азота (NO), образующийся при сгорании азота, вступает в реакцию с аммиаком (NH3), образуя азотную кислоту (HNO3) и азоту оксид (N2O). Эта реакция используется для получения азотной кислоты, которая широко применяется в производстве удобрений и взрывчатых веществ.
Таким образом, реакции между оксидом и основанием являются важными химическими процессами, которые находят применение в различных отраслях промышленности и научных исследованиях.
Образование соли при взаимодействии оксида с основанием
Оксиды и основания – это классы химических соединений, обладающих различными свойствами и реакционной способностью. Однако они могут вступать во взаимодействие друг с другом, приводя к образованию солей.
Взаимодействие оксида с основанием происходит с образованием промежуточного соединения - гидроксида металла. Далее этот гидроксид может реагировать с кислотой, образуя соль и воду.
Примером реакции образования соли при взаимодействии оксида с основанием может служить реакция образования сернокислого натрия (Na2SO4):
| Оксид | Основание | Соль |
| SO2 | NaOH | Na2SO4 |
Также, в результате взаимодействия оксидов с основаниями могут образовываться другие соли, например:
- Fe2O3 + 6NaOH → 2Na3FeO3 + 3H2O
- CaO + 2NaOH → Ca(OH)2 + Na2O
Выводящая продукт из этих реакций – соль – имеет совершенно иные свойства, чем исходные вещества. Таким образом, образование солей при взаимодействии оксида с основанием является важным процессом в химии.
Базовые свойства реакций оксида с основанием

Реакции оксида с основанием являются одним из важнейших типов химических реакций, которые происходят между кислотными и основными соединениями. Особенностью этих реакций является образование соли и воды в результате обменных взаимодействий.
Действие оксида на основание происходит с выделением тепла. Основные известные примеры реакций включают реакцию оксида меди (II) с гидроксидом натрия:
- CuO + 2NaOH → Na2CuO2 + H2O
Другой пример - это реакция оксида железа (III) с гидроксидом аммония:
- Fe2O3 + 6NH4OH → 2Fe(OH)3 + 6NH3
Важно отметить, что при реакции оксида с основанием происходит образование соли и воды. Вода образуется в результате специфичесного переноса водорода между оксидом и основанием. Это явление называется гидратацией или гидрированием.
Реакции оксида с основанием имеют широкое применение в различных областях, включая химическую промышленность, пищевую промышленность и многие другие. Понимание основных свойств и химических реакций оксида с основанием является фундаментальным для изучения химии и применения ее в разных сферах деятельности.
Применение реакций оксида с основанием в промышленности

Реакции между оксидами и основаниями имеют широкое применение в промышленности. Они используются для получения различных продуктов и материалов, а также для очистки и обработки различных веществ. Одним из примеров такого применения является производство стекла.
Стекло - это аморфное вещество, получаемое путем плавления смеси оксидов металлов с основаниями. Обычно используется силикат натрия (Na2SiO3) в качестве основания. Реакция между оксидом кремния (SiO2) и основанием приводит к образованию кремний-натриевого стекла.
Реакция происходит следующим образом: кремнийоксид распадается на кремний и кислород, и кремний вступает в реакцию с основанием, образуя стеклообразную массу. В процессе плавления можно добавлять различные добавки для придания стеклу определенных свойств, таких как прозрачность или цвет.
Еще одним примером применения реакций оксида с основанием является производство мыла. Оксид калия (K2O) реагирует с жирами, содержащими кислоты, образуя соли жирных кислот - мыло. Реакция основания с жирами называется щелочным гидролизом.
Реакция происходит следующим образом: оксид калия распадается на калий и кислород, и калий вступает в реакцию с кислотными группами в молекулах жиров, образуя мыло и воду. Этот процесс используется в промышленности для производства мыла различного назначения.
Таким образом, реакции оксида с основанием играют важную роль в промышленности. Они используются для получения различных продуктов, таких как стекло и мыло, которые широко применяются в повседневной жизни.
Важность изучения реакций оксида с основанием для химической промышленности

Изучение реакций оксида с основанием является важным аспектом в химической промышленности. Эти реакции являются основой для производства различных продуктов и материалов, которые имеют широкое применение в различных отраслях экономики.
Одним из важных примеров реакции оксида с основанием является нейтрализация, при которой оксид и основание образуют соль и воду. Эта реакция используется для производства солей, которые находят применение в пищевой промышленности, фармацевтике, сельском хозяйстве и других отраслях промышленности.
Кроме того, реакция оксида с основанием может привести к образованию новых соединений, которые имеют специфические свойства и применяются в различных сферах. Например, реакция оксида железа с основанием может привести к образованию оксида железа(III), который является важным компонентом в производстве стали и других металлов. Также реакции оксида с основанием могут быть использованы для получения катализаторов, которые используются в различных процессах химического производства.
Изучение реакций оксида с основанием помогает развивать новые технологии и улучшать существующие процессы в химической промышленности. Понимание химических реакций позволяет оптимизировать производственные процессы, улучшать эффективность и качество продукции, а также разрабатывать новые материалы и продукты с улучшенными свойствами. Это способствует развитию экономики и повышению конкурентоспособности предприятий на мировом рынке.
Вопрос-ответ

Какое действие происходит между оксидом и основанием?
Между оксидом и основанием происходит химическая реакция, которая называется нейтрализацией. В результате этой реакции образуется соль и вода.
Какие химические реакции возникают при действии оксида на основание?
При действии оксида на основание возникает химическая реакция нейтрализации. В результате образуются соль и вода. Например, при действии оксида кальция на основание щелочи (гидроксид натрия), получается соль - кальция натрия, и вода.
Какой пример такой реакции можно привести?
Примером такой реакции может служить реакция между оксидом магния и гидроксидом калия. При их взаимодействии образуются соль - магния калия, и вода.
Какие еще реакции нейтрализации происходят при действии оксида на основание?
Помимо образования солей, при действии оксида на основание может образовываться и другой продукт - амфотерные оксиды. Например, при действии оксида алюминия на основание (гидроксид натрия), образуется соль - алюминия натрия и вода.
Возможны ли другие реакции, кроме нейтрализации, при действии оксида на основание?
Да, возможны и другие реакции при действии оксида на основание. Например, при действии оксида железа на основание (гидроксид натрия), образуется сложный ионный комплекс, а также вода.
