Металлы – это класс химических элементов, которые обладают определенными свойствами и имеют специфическую структуру. Их основные характеристики включают высокую тепло- и электропроводность, а также блеск и способность быть деформированными без разрушения. Кроме того, металлы обычно имеют высокую плотность и плавятся при относительно высоких температурах.
Структура металлов основана на решетчатом упорядочении атомов, главным образом кубической или гексагональной симметрии. Атомы в металлах тесно упакованы друг к другу, образуя кристаллическую решетку. Эта решетка обеспечивает металлам их основные свойства и исключительную прочность.
Особенности химического элемента металлов также связаны с его электронной структурой. Металлы обычно имеют малое количество валентных электронов, что делает их хорошими проводниками тепла и электричества. Валентные электроны свободно передвигаются по решетке и создают электронное облако, что обуславливает специфическую электропроводность металлов.
Другие химические свойства металлов включают их активность в реакциях с другими веществами. Многие металлы имеют тенденцию образовывать катионы, позволяя им образовывать ионные связи с отрицательно заряженными атомами. Золото, серебро и платина являются хорошими примерами малоактивных металлов, которые имеют низкую реакционную способность и сохраняют свою благородность даже в агрессивных условиях.
Структура и свойства металлов
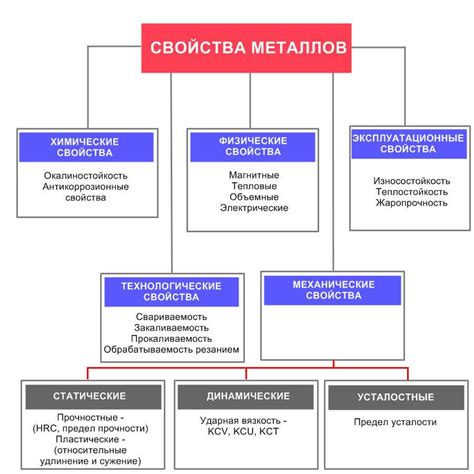
Металлы - это группа химических элементов с характерными свойствами, такими как блеск, высокая проводимость тепла и электричества, пластичность и прочность.
Структура металлов основана на сетке атомов, называемой кристаллической решеткой. В этой решетке атомы металла имеют регулярное расположение, образуя ряды и плоскости.
Основные свойства металлов определяются их электронной структурой.
Металлы легко проводят тепло и электричество благодаря наличию свободных электронов, которые могут свободно двигаться по решетке. Это делает их отличными проводниками электричества и тепла.
Благодаря пластичности металлов они могут быть легко переработаны и сформированы в различные формы. Это объясняется способностью атомов металлов сдвигаться друг относительно друга без нарушения кристаллической структуры.
Прочность металлов связана с их механическими свойствами. Атомы в решетке металлов образуют связи, которые придают материалу силу и жесткость.
Химический элемент и его особенности
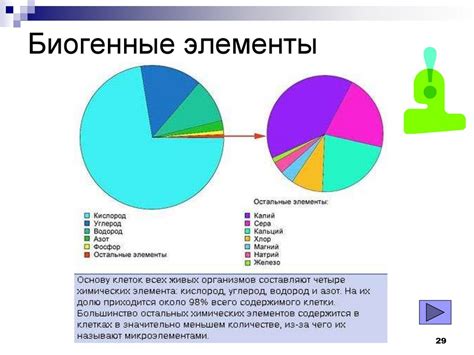
Химический элемент - это вещество, состоящее только из одного типа атомов, которые имеют одинаковое число протонов в ядре. Количество протонов определяет химические и физические свойства элемента и называется атомным номером.
Каждый химический элемент имеет свою уникальную химическую символику, которая состоит из одной или двух букв. Некоторые химические элементы названы в честь известных ученых или открытий, например, натрий (Na) по имени города Наумбург в Германии.
У химического элемента может быть несколько изотопов, различающихся числом нейтронов в ядре. Изотопы могут иметь различные степени стабильности и использоваться как радиоизотопы в науке и медицине.
Каждый химический элемент обладает характерными физическими и химическими свойствами. Физические свойства включают точку плавления, точку кипения, плотность и твердость элемента. Химические свойства включают способность элемента вступать в химические реакции, образование химических соединений и изменение окраски при взаимодействии с другими веществами.
Химические элементы строются в таблицу Менделеева, где они упорядочены по возрастанию атомного номера. В таблице указывается их химическая символика, атомный номер, относительная атомная масса и групповая принадлежность. По горизонтали находятся элементы с одинаковым количеством электронных оболочек, а по вертикали - с одинаковым числом электронов на внешней оболочке.
Изучение свойств и характеристик химических элементов позволяет понять и объяснить многочисленные явления в природе, создать новые материалы, а также применять их в различных отраслях науки и промышленности.
Строение металлической решетки
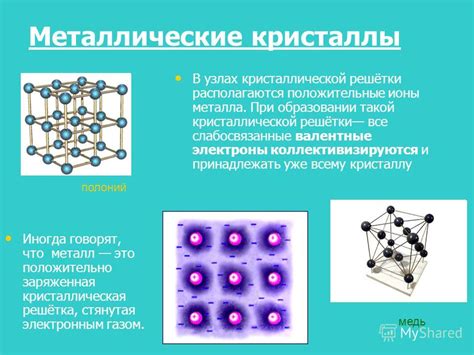
Металлы отличаются от других элементов своим уникальным строением - металлической решеткой. Это особое атомное строение, которое придает металлам их характерные свойства. Строение металлической решетки состоит из кристаллической решетки и межатомных связей.
Кристаллическая решетка металлов представляет собой трехмерную сетку, состоящую из положительно заряженных атомных ядер, окруженных электронными облаками. Атомная решетка обладает регулярной структурой, где атомы расположены в определенном порядке. Эта структура делает металлы прочными и твердыми, а также обеспечивает устойчивость и форму металлических предметов.
Межатомные связи в металлах образуются за счет деликатного взаимодействия свободных электронов с атомами. Свободные электроны создают электронное облако, которое поддерживает связь между атомами и придает металлам их уникальные электропроводящие и теплопроводные свойства. Благодаря этим связям, металлы обладают высокой пластичностью и способностью принимать различные формы.
Строение металлической решетки не только определяет физические и механические свойства металлов, но и влияет на их химическую реактивность. Электронность и высокое тепловое движение свободных электронов в металле обуславливают его реакционную способность и способность образовывать сплавы с другими элементами.
Основные физические и химические свойства металлов

Физические свойства:
- Металлы обладают высокой теплопроводностью и электропроводностью. Благодаря этому они широко применяются в электротехнике и строительстве.
- У металлов высокая пластичность и податливость. Они легко поддаются обработке и формовке, что позволяет создавать различные изделия и конструкции.
- Металлы обладают высокой плотностью, что делает их тяжелыми материалами. Они отлично подходят для изготовления структурных элементов.
- Металлы имеют обычно серебристо-серый цвет. Некоторые металлы, такие как медь и золото, обладают характерными яркими оттенками.
- Металлы обладают высокой твердостью, хотя есть и исключения, такие как натрий и калий, которые мягкие и могут быть нарезаны ножом.
- Металлы имеют высокую плавность и кипение. Некоторые металлы, такие как железо и алюминий, имеют высокую температуру плавления и применяются для производства стали и алюминиевых сплавов.
- Металлы могут быть магнитными, такими, как железо, никель и кобальт, или немагнитными, такими, как алюминий и медь.
Химические свойства:
- Металлы обычно образуют катионы, отдавая электроны другим элементам. Они активны в химических реакциях и способны образовывать соединения с не металлами.
- Металлы часто реагируют с водой, выделяя водородный газ. Некоторые металлы, такие как натрий и калий, реагируют с водой очень активно и могут вспыхивать.
- Металлы образуют оксиды при взаимодействии с кислородом. Оксиды металлов часто обладают щелочными или основными свойствами.
- Металлы обычно реагируют с кислотами, образуя соль и выделяяся водородный газ.
- Металлы могут формировать сплавы и специальные соединения с другими металлами и не металлами, что значительно расширяет их применение.
Вопрос-ответ

Каково строение металлов?
Строение металлов характеризуется наличием регулярно расположенных атомных решеток, которые образуют кристаллическую структуру.
Какие свойства металлов обусловлены их строением?
Строение металлов определяет такие их свойства как высокая термическая и электрическая проводимость, пластичность и металлический блеск.
Какие элементы характеризуются металлическим строением?
Металлическим строением характеризуются большинство элементов в таблице периодических элементов, например, железо, алюминий, медь, олово и др.
Что представляет собой атомная решетка металлов?
Атомная решетка металлов представляет собой трехмерную сетку атомов, в которой каждый атом окружен несколькими соседними атомами и имеет определенную позицию в решетке.
Почему металлы проводят электричество?
Металлы проводят электричество из-за наличия свободных электронов, которые могут легко перемещаться внутри металлической решетки и образовывать электрический ток.
