Металлы – это набор элементов, имеющих особые свойства, среди которых высокая электропроводность. Электропроводность металлов определяется их способностью отдавать электроны другим атомам. Именно это свойство делает металлы незаменимыми в различных областях науки и промышленности.
Существует много металлов, которые известны своей высокой готовностью отдавать электроны. Одним из таких металлов является литий. Литий – самый легкий из металлов и обладает высокой реактивностью. Он легко отдает свои электроны, что делает его незаменимым компонентом в различных типах аккумуляторов.
Еще одним металлом, готовым отдавать электроны, является натрий. Натрий имеет высокую электропроводность и широко используется в производстве различных электронных устройств. Он способен быстро отдавать свои электроны, что обеспечивает стабильную работу множества электронных систем.
Калий – еще один металл, готовый отдать свои электроны. Он обладает высокими электропроводностью и реактивностью. Это свойство делает калий не только важным компонентом в различных электронных устройствах, но и необходимым элементом для нормального функционирования организма человека.
Ртуть – это металл, который всегда готов отдать свои электроны. Он обладает очень высокой электропроводностью и реактивностью. Ртуть активно используется в различных электротехнических устройствах и приборах из-за своей высокой способности отдавать электроны.
Другим металлом, готовым отдавать электроны, является алюминий. Он обладает высокой электропроводностью и реактивностью. Алюминий широко используется в производстве проводов и кабелей, а также в электронике, благодаря своей готовности отдавать электроны.
Цезий – это еще один металл, готовый отдать свои электроны. Он обладает очень высокой электропроводностью и реактивностью, что делает цезий незаменимым в различных электронных устройствах и приборах.
Стронций – это металл, который всегда готов отдать свои электроны. Он обладает высокой электропроводностью и реактивностью. Стронций активно используется в производстве различных электронных компонентов и деталей, так как способен быстро отдавать свои электроны.
Таким образом, металлы, которые всегда готовы отдавать свои электроны, являются важными компонентами в различных областях науки и промышленности. Их высокая электропроводность и готовность отдавать электроны делают эти металлы незаменимыми в создании электронных устройств и приборов.
Металлы, готовые отдать свои электроны:
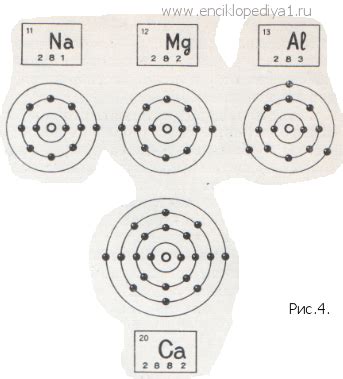
В химии существует особая группа металлов, которые отличаются от других своей способностью отдавать электроны. Это позволяет им быть активными химическими элементами и участвовать во многих реакциях.
Первым в списке металлов, готовых отдать свои электроны, находится литий. Это мягкий и легкий металл, который легко реагирует с водой и кислородом. Литий используется в производстве аккумуляторов и является важным компонентом в электротехнике.
Еще одним металлом, готовым отдать свои электроны, является натрий. Он также имеет активные химические свойства и активно реагирует с водой и кислородом. Натрий широко используется в пищевой промышленности и в производстве стекла.
Алюминий – еще один металл, готовый отдать свои электроны. Он одновременно и легкий, и прочный, что делает его идеальным материалом для конструкций, авиации и упаковки. Алюминий также активно применяется в производстве проводов, кабелей и других электронных устройств.
Цинк – металл, готовый отдать свои электроны с относительно низкой реактивностью. В основном он используется для гальванического покрытия других металлов, таких как железо и сталь, чтобы защитить их от коррозии. Цинк также используется в производстве батареек и других электрохимических устройств.
Медь – металл, готовый отдать свои электроны и обладающий высокой электропроводностью. Именно поэтому медь широко используется в электротехнике и производстве проводников. Она также применяется для создания украшений благодаря своей привлекательной цветовой гамме и устойчивости к коррозии.
Серебро – металл, готовый отдать свои электроны и обладающий высокой электропроводностью и термической проводимостью. Оно широко используется в электротехнике, производстве зеркал и фотографии благодаря своей способности отражать свет.
Золото – металл, готовый отдать свои электроны и известный своей устойчивостью к коррозии и химической инертностью. Золото используется в ювелирном искусстве, электротехнике и в производстве электроники.
Платина – металл, готовый отдать свои электроны и известный своей химической инертностью и высокой устойчивостью к коррозии. Платина используется в катализаторах, ювелирных изделиях и производстве биомедицинских устройств.
Таким образом, эти восемь металлов являются прекрасными проводниками электричества и активно участвуют в различных химических реакциях, делая их неотъемлемой частью современной технологии и промышленности.
Алюминий

Алюминий – это легкий, прочный и хорошо поддающийся обработке металл. Он является третьим по распространенности металлом на Земле после кислорода и кремния.
Алюминий обладает высокой теплопроводностью и отлично проводит электричество. Он широко используется в электротехнике и производстве проводов.
Необычайная легкость алюминия делает его незаменимым материалом для производства легких и прочных конструкций, таких как авиационные и автомобильные детали, корпуса космических ракет и спутников.
Вывод алюминия из руды происходит с помощью электролиза – процесса, при котором алюминий отдает свои электроны и становится положительно заряженным ионом.
Алюминий является одним из самых экологически чистых и устойчивых материалов к воздействию окружающей среды. Он можно полностью переработать множество раз без потери качества и свойств. Поэтому алюминий часто используется в упаковке, так как его можно легко переработать и использовать повторно.
Цинк

Цинк – химический элемент с атомным номером 30 в периодической системе. Он относится к группе металлов и является одним из самых распространенных элементов в Земной коре. Цинк обладает серебристым блеском и хорошо реагирует с кислородом, образуя оксид цинка (ZnO).
Цинк является важным сплавным элементом и используется в производстве многих материалов. Например, цинковые сплавы широко используются в автомобильной, строительной и электротехнической промышленности. Они обладают хорошими механическими свойствами и устойчивостью к коррозии.
Однако особенностью цинка является его способность легко отдавать электроны. Благодаря этому свойству, цинк широко используется в гальванических элементах и батареях. Он является одним из основных компонентов анизотропных аккумуляторных батарей и может обеспечить высокую энергетическую плотность и длительное время работы устройств.
Цинк также используется в производстве некоторых видов пищевых добавок и лекарственных препаратов. Он играет важную роль в поддержании иммунной системы и обеспечении нормального роста и развития организма.
Натрий

Натрий – это химический элемент с атомным номером 11 и символом Na. Он относится к категории щелочных металлов и является светлым и мягким металлом. Натрий входит в состав множества соединений и находит применение в различных отраслях промышленности и науки.
Одной из основных особенностей натрия является его высокая реактивность. Натрий всегда готов отдать свои электроны. Это связано с его строением атома и особенностями электронной оболочки. Благодаря этой особенности натрий активно взаимодействует с другими веществами и обладает множеством химических и физических свойств.
Натрий широко используется в производстве стекла, щелочей, соды и различных химических соединений. Он также находит применение в пищевой промышленности, где используется в качестве добавки в пищевые продукты. Натрий играет важную роль в работе нашего организма, поскольку участвует в регуляции водного баланса и нервной активности.
Несмотря на все свои полезные свойства, натрий также может быть опасным в больших количествах. Перерасход натрия может вызвать дефицит калия и других электролитов, что может привести к нарушению работы организма. Поэтому важно умеренно употреблять продукты, богатые натрием, и следить за его потреблением.
Литий

Литий – это химический элемент из группы щелочных металлов, который всегда готов отдать свои электроны. Он имеет атомный номер 3 и обозначается символом Li. Литий обладает низкой плотностью и малой твердостью, что делает его одним из самых легких металлов.
Литий является очень реактивным металлом и легко вступает в химические соединения. Он обладает высокой электроотрицательностью, что делает его отличным веществом для использования в батареях и аккумуляторах. Благодаря своей низкой плотности, литий-ионные аккумуляторы обеспечивают высокую энергоемкость и могут быть использованы в различных электронных устройствах – от мобильных телефонов до электрических автомобилей.
Литий также широко используется в лечении психических расстройств, таких как биполярное расстройство и маниакально-депрессивное состояние. Литийные препараты помогают стабилизировать настроение и предотвращают возникновение маниакальных или депрессивных эпизодов.
Кроме того, литий применяется в ядерной энергетике, производстве стекла и керамики, а также в производстве алюминия и лития для авиационной и автомобильной промышленности. Его сплавы обладают высокой прочностью и легкостью, что делает их идеальным материалом для строительства легких и прочных конструкций.
Магний

Магний – химический элемент с атомным номером 12 в периодической таблице Менделеева. Этот металл является одним из самых распространенных в земной коре и обладает рядом уникальных свойств.
Вещество магния обладает серебристым цветом и характерной мягкостью. Магний является активным металлом, который легко реагирует с кислородом и в больших количествах образует окисленные соединения. Это свойство делает магний отличным компонентом для создания сплавов, особенно в авиационной и автомобильной промышленности.
Магний также обладает высокими теплоотводящими свойствами, что делает его незаменимым материалом для производства радиаторов и других систем охлаждения. Благодаря своей легкости, магний также используется в производстве легких сплавов для автомобильных деталей, таких как диски и кузов.
Кроме того, магний имеет полезные биологические свойства. Он является необходимым элементом для здоровья человека и животных. Магний участвует в большом количестве биохимических процессов в организме, таких как синтез белка, активацию ферментов и регуляцию нервной системы.
Вывод: магний - это универсальный металл, который находит применение в самых различных областях человеческой деятельности. Он является не только важным строительным элементом для создания различных материалов, но и незаменимым веществом для поддержания здоровья и жизнедеятельности организмов.
Потассий

Потассий – химический элемент периодической системы с атомным номером 19 и символом K. Он относится к щелочным металлам, обладает серебристо-белым цветом и мягкой текстурой. Потассий имеет низкую плотность и кипит при относительно низкой температуре — 759 градусов по Цельсию.
Потассий является очень активным химическим элементом и образует множество соединений. Он вступает в реакции с водой, кислородом и многими другими веществами. Потассий играет важную роль в организмах живых организмов, так как является необходимым элементом для работы нервной системы и мышц. Он также участвует в регуляции водного баланса в организме и поддержании здоровья сердца.
В природе потассий в основном встречается в виде солей, таких как хлорид потассия и сульфат потассия. Он широко используется в химической промышленности для производства удобрений, стекла, мыла и других продуктов. Потассий также используется в металлургии для получения различных сплавов.
Кальций

Кальций - химический элемент из группы щелочноземельных металлов, обладающий атомным номером 20. Он представляет собой мягкий серебристо-белый металл, который легко окисляется на воздухе.
Кальций является одним из самых распространенных элементов в земной коре и составляет около 3% ее массы. Он входит в состав многих минералов, таких как известняк, мрамор и гипс.
Одной из ключевых ролей кальция в организме человека является участие в образовании и поддержании здоровья костей и зубов. Кальций также играет важную роль в нервной системе, мышцах и сердце, участвует в сокращении мышц и передаче нервных импульсов.
Одним из наиболее известных соединений кальция является известь (оксид кальция), которая широко используется в строительстве для производства строительных материалов, таких как цемент и извести. Кальций также используется в производстве стекла, керамики и сплавов.
В природе кальций обычно встречается в виде ионов Ca2+, которые являются одними из наиболее распространенных положительно заряженных ионов в земной гидросфере. Кальций входит в состав многих важных минералов и биологических структур, таких как раковины морских животных и зубы у человека.
Рубидий

Рубидий – химический элемент с атомным номером 37 и символом Rb. Он относится к группе щелочных металлов и является одним из восьми металлов, которые всегда готовы отдать свои электроны. Рубидий довольно редкий элемент в земной коре, однако его находят в некоторых минералах, таких как лепидолит и селенит.
Рубидий обладает мягкими физическими свойствами, он имеет серебристо-белый цвет и является хорошим проводником тепла и электричества. Он обладает низкой плотностью, что делает его легким и удобным для использования в различных технологических процессах и приборах.
Из-за своей высокой реактивности рубидий часто используется в научных исследованиях и в производстве электронных устройств. Его применяют в процессе создания фоточувствительных элементов и фотоэлементов. Рубидиевый атом также используется в атомных часах для измерения времени с высокой точностью.
Кроме того, рубидий является важным металлом для некоторых процессов в ядерной энергетике и в медицинской диагностике. Он применяется в нейтронных ионных материалах, используемых в ядерных реакторах, а также в некоторых методах радиоизотопной диагностики для получения изображений органов и тканей человека.
Вопрос-ответ

Какие металлы готовы отдать свои электроны?
В статье упоминаются 8 металлов, которые всегда готовы отдать свои электроны. Это натрий, калий, цезий, барий, стронций, кальций, радий и франций.
Почему эти металлы готовы отдать свои электроны?
Эти металлы находятся в первой группе периодической системы элементов и имеют всего один электрон в внешней оболочке. Из-за такой конфигурации электронов, им отдаление одного электрона довольно выгодно, так как они тем самым приходят к стабильной конфигурации с полностью заполненной оболочкой.
Какие свойства имеют эти металлы?
Металлы этой группы обладают свойством легко отдавать электроны и образовывать положительные ионы. Они также имеют низкую электроотрицательность и высокую реактивность. Также эти металлы обладают хорошей проводимостью электричества и тепла.
