Оксид металла – это химическое соединение, состоящее из металла и кислорода. Оксиды металлов встречаются в природе в виде минералов и имеют широкий спектр свойств и применений. Они образуются при взаимодействии металла с воздухом или в результате окисления металлов при контакте с водой или другими веществами.
Оксиды металлов часто имеют характерные цвета, например, оксид железа имеет красно-коричневый цвет, оксид меди – зеленый, оксид алюминия – белый. Кроме того, оксиды металлов обладают различными физическими и химическими свойствами. Например, они могут быть твердыми, полупроводниковыми или жидкими веществами, а также иметь высокую температуру плавления и кипения.
Примеры оксидов металлов включают оксиды кальция, магния, железа, алюминия, свинца и других элементов. Они широко применяются в различных отраслях промышленности. Например, оксид алюминия используется в производстве керамики, стекла, аэрокосмической и электронной промышленности. Оксид железа является основным составляющим пигментов и используется в производстве красок и косметики. Оксид кальция играет ключевую роль в производстве цемента и стекла.
Оксиды металлов в большинстве случаев обладают высокой химической стабильностью и не растворяются в воде. Некоторые из них также обладают кислотными или щелочными свойствами. Например, оксид алюминия является амфотерным веществом и может взаимодействовать как с кислотами, так и с щелочами.
Оксиды металлов имеют важное значение не только в промышленности, но и в природе. Они являются неотъемлемой частью геохимических циклов и влияют на химические процессы в почвах, воде и атмосфере. Кроме того, оксиды металлов играют важную роль в катализаторах, батареях и других технологиях.
Определение и состав
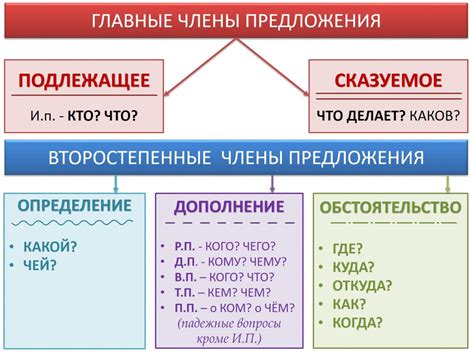
Оксиды металлов представляют собой химические соединения, состоящие из металлического элемента и кислорода. Оксиды металлов широко распространены в природе и имеют множество применений в различных отраслях промышленности.
Состав оксидов металлов определяется их химической формулой, которая указывает на количество атомов каждого элемента в соединении. Например, оксид алюминия имеет формулу Al2O3, что означает наличие двух атомов алюминия и трех атомов кислорода.
Оксиды металлов могут быть одноатомными или многоатомными соединениями. Одноатомные оксиды содержат только один металлический элемент, например, оксид железа(II) - FeO. Многоатомные оксиды содержат несколько металлических элементов, например, оксид бария и алюминия - BaAl2O4.
Примеры оксидов металлов
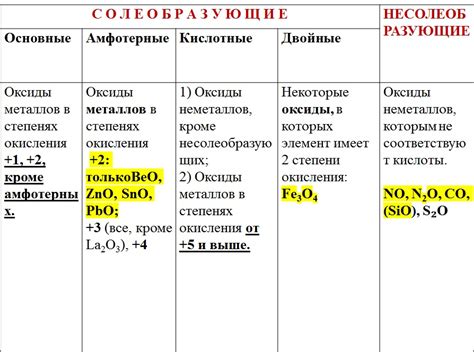
Оксиды металлов - это химические соединения, состоящие из металлического элемента и кислорода. Они являются наиболее распространенными классами соединений металлов.
Некоторые из наиболее известных примеров оксидов металлов включают:
- Оксид алюминия (Al2O3) - прочный, твердый и немагнитный материал, используемый, например, в производстве керамики и алюминиевых сплавов.
- Оксид железа (Fe2O3) - также известный как оксид гематита, это красное соединение, которое является одним из основных компонентов ржавчины и используется в производстве красок и косметики.
- Оксид цинка (ZnO) - это белый порошок с широким спектром применений, включая использование в солнцезащитных кремах, керамике и лекарствах.
Другие примеры включают оксиды металлов, такие как оксид меди (Cu2O), оксид свинца (PbO), оксид магния (MgO) и оксид кобальта (CoO). Каждый из этих оксидов имеет свои уникальные свойства и применения в различных отраслях промышленности и научных исследованиях.
Свойства оксидов металлов
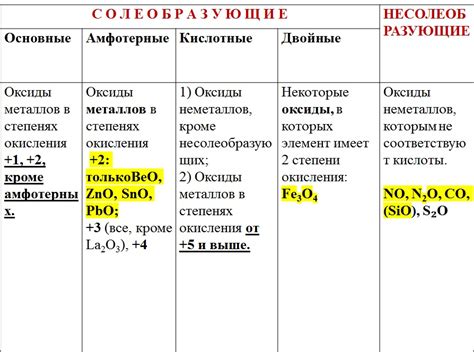
Оксиды металлов – это соединения металлов с кислородом. У этих соединений есть несколько общих свойств:
- Оксиды металлов обычно имеют высокую температуру плавления и кипения. Некоторые из них обладают свойством быть твердыми при комнатной температуре, например, оксиды алюминия и железа.
- Большинство оксидов металлов обладают хорошей электропроводностью. Это связано с наличием свободных электронов, которые могут перемещаться по структуре оксида.
- Оксиды могут иметь различную степень окисления металла. Это обуславливает их разнообразные свойства и способность взаимодействовать с другими веществами.
- Некоторые оксиды металлов обладают кислотными свойствами и могут реагировать с основаниями, образуя соли. Например, оксид цинка взаимодействует с кислотой и образует соль цинка.
- Оксиды металлов могут быть использованы в качестве катализаторов для различных химических реакций. Их поверхностная активность и гетерогенность позволяют ускорить процесс протекания реакции.
Также оксиды металлов могут использоваться в различных отраслях промышленности, например, в качестве пигментов для красок и лаков, в производстве стекла, в медицине и электронике.
Вопрос-ответ

Что такое оксид металла?
Оксид металла - это химический соединение, состоящее из металла и кислорода. Оксиды металлов являются одним из наиболее распространенных классов неорганических соединений. Они образуются путем реакции металла с кислородом, как в атмосфере, так и в реакциях с другими веществами.
Какие примеры оксидов металлов существуют?
Существует огромное количество оксидов металлов. Некоторые из них включают оксид алюминия, оксид железа, оксид меди, оксид цинка и оксид свинца. Каждый из этих оксидов обладает уникальными физическими и химическими свойствами, что делает их полезными в различных промышленных и научных приложениях.
Какие свойства обладают оксиды металлов?
Оксиды металлов обладают различными свойствами в зависимости от конкретного соединения. Однако, в целом, оксиды металлов обладают высоким плавлением и кипением, тугоплавкими, хорошей проводимостью тепла и электричества, а также отличаются различной степенью растворимости в воде и других растворителях.
Какие применения имеют оксиды металлов?
Оксиды металлов имеют широкое применение в различных областях. Например, оксид алюминия используется в производстве абразивов и керамики, оксид железа применяется в изготовлении магнитов и красителей, оксид цинка используется в производстве резиновых изделий и косметических продуктов. Кроме того, оксиды металлов играют важную роль в химической промышленности и катализе реакций.
