Металлы - это элементы химической таблицы, обладающие отличительными свойствами, такими как высокая плавкость, тугоплавкость, хорошая электропроводность и теплопроводность. Однако мало кто знает, что каждый металл может иметь различные изотопы, которые играют важную роль в научных и промышленных исследованиях.
Изотопы - это атомы одного и того же элемента, но с различным количеством нейтронов в ядре. Например, у металла железа существуют такие изотопы, как Fe-54 с 54 нейтронами в ядре и Fe-56 с 56 нейтронами. Похожие изотопы могут иметь различные физические и химические свойства, что делает их неотъемлемой частью исследований в различных областях науки и промышленности.
Особенности изотопов металла определяются их атомным весом и стабильностью. Атомный вес изотопа зависит от суммарного количества протонов и нейтронов в ядре атома, а стабильность - от соотношения протонов и нейтронов. Некоторые изотопы металлов являются стабильными и не подвержены распаду, в то время как другие могут быть радиоактивными и иметь ограниченную жизнь.
Что такое изотопы металла?
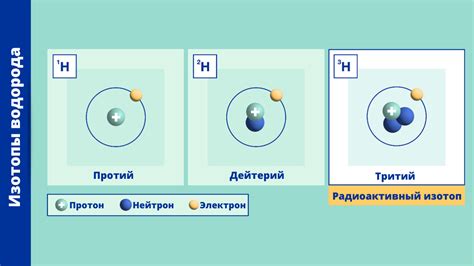
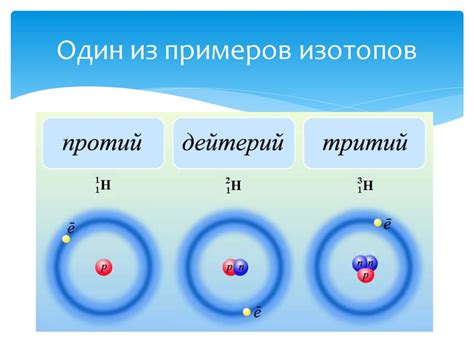
Изотопы металла – это разновидности атомов одного элемента, отличающиеся числом нейтронов в ядре. Все изотопы одного элемента имеют одинаковое количество протонов, но разное количество нейтронов. Например, углерод может иметь изотопы с числом нейтронов 12, 13 и 14. Изотопы металла имеют свои уникальные свойства, которые определяют их химические и физические параметры.
Присутствие изотопов металла может влиять на его физические свойства, такие как плотность, теплопроводность и электропроводность. Некоторые изотопы металла могут быть стабильными, то есть они не подвержены радиоактивному распаду, в то время как другие изотопы могут быть радиоактивными и иметь свойство распадаться со временем.
Изотопы металла широко используются в научных исследованиях и практических приложениях. Например, изотопы железа используются для изучения процессов образования крови и диагностики некоторых заболеваний. Также изотопы металла могут использоваться для маркировки и трассировки веществ, анализа минералов и атомных структур.
Изотопы металла могут быть разделены и изучены с использованием различных методов, таких как масс-спектрометрия и диффузия газа через мембраны. Изотопы металла являются важным объектом исследования для ученых и имеют широкий спектр применений в различных областях науки и технологий.
Определение изотопов металла
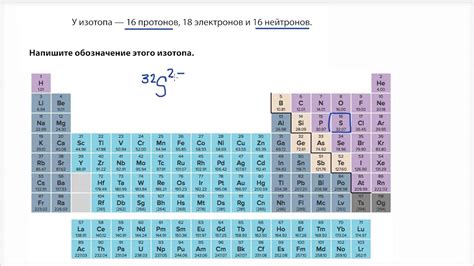
Изотопы металла – это атомы этого металла, в которых число нейтронов в ядре отличается от обычного (наиболее распространенного) изотопа этого элемента. Все металлы имеют несколько изотопов, отличающихся друг от друга по числу нейтронов в ядре. Изотопы обладают одинаковым количеством протонов в ядре, то есть имеют одинаковый атомный номер, но отличаются атомной массой.
Изотопы металла могут иметь различные свойства и характеристики. Например, некоторые изотопы металла могут быть радиоактивными и иметь больший или меньший период полураспада, чем стабильные изотопы. Также изотопы металла могут образовывать соединения с разными степенями окисления, что влияет на их химическую активность и способность вступать в реакции.
Знание о различных изотопах металла является важным для таких областей, как радиоизотопная диагностика, анализ материалов и исследование происхождения и свойств различных металлургических и природных материалов. Кроме того, изотопы металла используются в ядерных и радиоизотопных технологиях, таких как ионообменная хроматография, медицинская диагностика и радиоизотопная терапия.
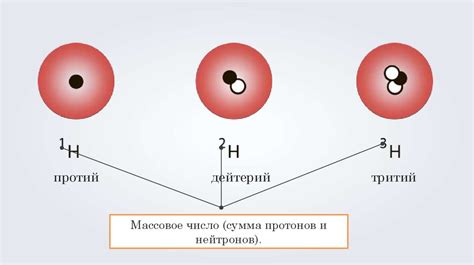
Для удобства классификации и идентификации изотопов металла используются специальные обозначения, включающие атомный номер и массовое число изотопа. Например, вода с атомами кислорода-18 и кислорода-16 имеет обозначение H2O-18 и H2O-16 соответственно. Массовое число указывается в верхнем индексе справа от символа химического элемента.
Изотопы металла могут иметь разные степени стабильности и время жизни. Некоторые изотопы металла могут быть очень стабильными и иметь длительное время жизни, в то время как другие могут быть нестабильными и быстро распадаться. Это свойство изотопов металла может быть использовано для их идентификации и анализа методами масс-спектрометрии и спектроскопии.
Как определить изотопы металла?
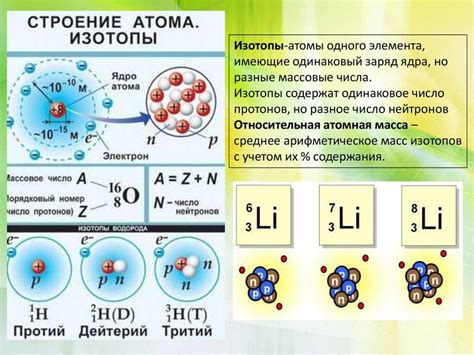
Изотопы металла – это атомы этого металла с одинаковым числом протонов в ядре, но разным числом нейтронов. Определение изотопов металла может осуществляться различными методами, в зависимости от его свойств и химической структуры.
Один из методов определения изотопов металла – это масс-спектрометрия. В ходе данного метода атомы металла разлагаются на ионы и проходят через магнитное поле, которое изгибает их траекторию в зависимости от их массы-заряда соотношения. Таким образом, можно разделить изотопы металла по массе и определить их количество.
Другой метод – это использование ядерно-магнитного резонанса (ЯМР). ЯМР позволяет изучать различия в химическом окружении атомов металла и их соседей. Поэтому, если изотопы металла имеют различную химическую активность или химическое окружение, их можно определить с помощью ЯМР.
Также для определения изотопов металла может быть использовано окислительно-восстановительное растворение. При данном методе можно определить изотопы металла, изучив изменения во времени или изменения в окружающей среде после введения вещества, содержащего металл.
В целом, определение изотопов металла является важной задачей в химических исследованиях. Различные методы позволяют узнать состав и химические свойства изотопов металла, что открывает новые возможности для их использования в различных областях науки и промышленности.
Изотопы металла в природе
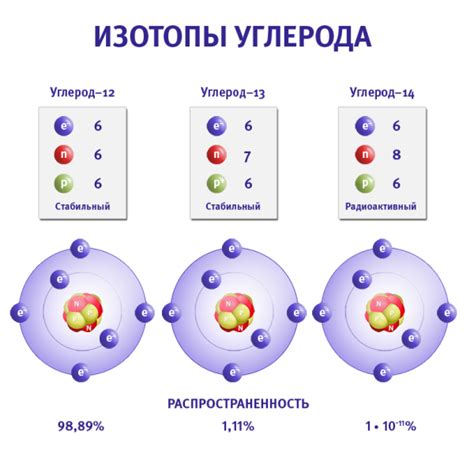
Изотопы металла — это разновидности атомов данного металла, имеющие одинаковое количество протонов в ядре, но различающиеся по количеству нейтронов. Отличие в количестве нейтронов влияет на массу атома, а следовательно, на его свойства.
В природе находится несколько изотопов каждого металла. Например, у железа существует четыре основных изотопа: %Fe-54%, %Fe-56%, %Fe-57% и %Fe-58%. Изотоп %Fe-56% является наиболее распространенным и встречается в природе с частотой около 91,75%. Остальные изотопы железа встречаются в природе в небольших количествах.
Как правило, изотопы металла имеют примерно одинаковые химические свойства, однако их физические свойства, такие как плотность и температура плавления, могут незначительно различаться.
Изотопы металла могут иметь практическое применение. Например, уран-235 является основным изотопом урана и используется в ядерной энергетике. Другой изотоп урана, уран-238, используется в производстве покрытий для ламп и керамических изделий.
В целом, изотопы металла играют важную роль в науке и промышленности. Изучение и использование различных изотопов помогает расширить наши знания об элементах и позволяет создавать новые материалы и технологии.
Распространенность изотопов металла
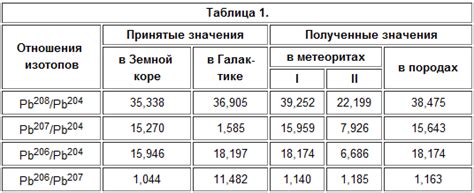
Каждый металл обычно имеет несколько изотопов, которые отличаются по числу нейтронов в ядре. Распространенность изотопов металла зависит от его происхождения и способа получения.
Например, натуральный медь (Cu) состоит из двух стабильных изотопов: медь-63 (63Cu) и медь-65 (65Cu). Их распространенность в природе примерно одинакова, причем медь-63 встречается немного чаще.
Алюминий (Al), в свою очередь, имеет три стабильных изотопа: алюминий-27 (27Al), алюминий-26 (26Al) и алюминий-28 (28Al). Распространенность этих изотопов различается и зависит от их стабильности и способа образования.
Некоторые металлы также имеют радиоактивные изотопы, которые образуются через процессы ядерного распада. Например, уран (U) имеет несколько радиоактивных изотопов, таких как уран-235 (235U) и уран-238 (238U).
Распространенность изотопов металла может играть важную роль в его использовании в различных областях, таких как электроника, металлургия и ядерная промышленность.
Особенности изотопов металла

Изотопы металла - это разновидности атомов данного металла, отличающиеся числом нейтронов в ядре. Они имеют одинаковое количество протонов в ядре, но разное число нейтронов. Это приводит к тому, что изотопы металла могут иметь различные физические и химические свойства.
Одна из особенностей изотопов металла заключается в их стабильности или нестабильности. Некоторые изотопы металла являются стабильными и не подвержены радиоактивному распаду. Однако другие изотопы металла являются радиоактивными и имеют способность распадаться со временем.
Кроме того, изотопы металла могут иметь различный массовый номер. Массовый номер является суммой числа протонов и нейтронов в ядре атома. Изменение массового номера может влиять на плотность и физические свойства металла.
Изотопы металла также могут использоваться для различных целей. Некоторые изотопы металла являются источниками радиационного излучения и могут использоваться в медицине для лечения опухолей. Другие изотопы металла могут использоваться в промышленности для обозначения материалов и контроля качества.
Изотопы металла могут быть представлены в виде таблицы, где указывается массовый номер и химический символ изотопа. В таблице также могут быть указаны другие характеристики изотопа, такие как период полураспада для радиоактивных изотопов и применение для различных изотопов.
Физические и химические свойства изотопов металла
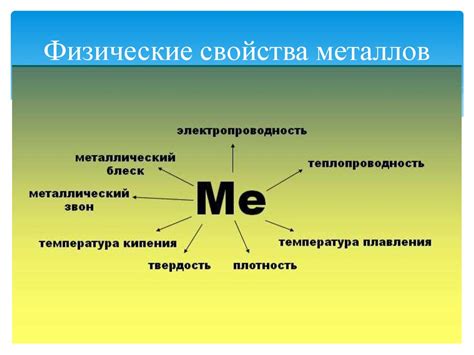
Изотопы металла отличаются друг от друга в своих физических и химических свойствах, так как имеют разное количество нейтронов в ядре. В результате этого, свойства изотопов металла, включая его плотность, точку плавления и кипения, могут отличаться.
Плотность изотопов металла может быть разной из-за различного уровня компактности атомов в кристаллической решетке. Так, некоторые изотопы металла могут быть более плотными, что делает их полезными в различных промышленных приложениях.
Точка плавления и кипения изотопов металла также могут отличаться, что приводит к различным физическим свойствам этих изотопов. Например, некоторые изотопы металла могут иметь более низкую точку плавления, что делает их идеальными для использования в процессах, требующих высокой температуры.
Химические свойства изотопов металла также могут быть разными. Некоторые изотопы металла могут обладать более активной реакционной способностью, что делает их полезными в химической промышленности. Они могут использоваться в качестве катализаторов или добавок в различных химических процессах.
В целом, изотопы металла предлагают разнообразие свойств, которые можно использовать в различных отраслях промышленности и науки. Изучение и понимание их физических и химических свойств помогает нам использовать их в нашей пользе и улучшить наши технологические процессы.
Применение изотопов металла
Изотопы металла находят широкое применение в различных отраслях науки и промышленности благодаря своим особенностям.
1. Медицина:
- Изотопы металла используются для создания радиоактивных препаратов, которые применяются в диагностике и лечении различных заболеваний, включая рак.
- Они также являются важными компонентами в процессе радиотерапии, для уничтожения злокачественных опухолей.
2. Энергетика:
- Изотопы металла применяются в ядерных реакторах для производства электрической энергии. Они играют роль топлива, которое подвергается расщеплению, выделяя огромное количество тепла.
- Изотопы также используются в ядерных исследованиях и тестировании ядерных взрывов.
3. Индустрия:
- Изотопы металла применяются в процессе маркировки и трассировки материалов, что помогает контролировать качество продукции и предотвращать подделку.
- Они также используются в процессе радиографии и испытаниях материалов для определения их структуры и свойств.
4. Наука:
- Изотопы металла играют важную роль в исследованиях геологии, позволяя определить возраст горных пород и их происхождение.
- Они также применяются в археологии, помогая определить возраст и происхождение артефактов и древних предметов.
Таким образом, изотопы металла имеют множество применений в различных областях и являются неотъемлемой частью современных технологий и исследований.
Области применения изотопов металла
Изотопы металла широко используются в различных областях научных и промышленных исследований. Одной из таких областей является ядерная энергетика. Изотопы металла, такие как уран или плутоний, используются в ядерных реакторах для производства электроэнергии. Благодаря своей ядерной активности, изотопы металла способны генерировать большое количество энергии и обеспечивать работу электростанций.
Еще одной областью применения изотопов металла является медицина. Некоторые изотопы металла используются в радионуклидной терапии и диагностике различных заболеваний. Например, изотопы металла такие как цезий и кобальт используются в лучевой терапии для лечения раковых заболеваний. Они используются для облучения опухолей, что способствует их разрушению.
Изотопы металла также находят применение в археологии и геологии. С помощью метода радиоуглеродного датирования, основанного на превращении изотопа углерода-14, ученые определяют возраст археологических находок и геологических образований. Такой метод позволяет ученым узнать, сколько лет назад произошло событие или образование исторически важных объектов или образований.
Изотопы металла также используются в промышленности, например, в качестве металлографических маркировок. Они позволяют идентифицировать и отслеживать металлы и сплавы в процессе производства, что является очень важным для обеспечения качества и безопасности продукции.
Вопрос-ответ

Что такое изотопы металла?
Изотопы металла - это атомы одного и того же химического элемента с различным числом нейтронов в ядре. Так как число нейтронов может варьироваться, то массовое число изотопов металла будет различаться.
В чем заключается особенность изотопов металла?
Особенностью изотопов металла является различие в их массовом числе и, соответственно, в массе атома. Изотопы металла могут иметь различные физические и химические свойства, однако их основное химическое поведение обычно остается неизменным.
Как можно определить изотопы металла?
Определить изотопы металла можно с помощью специальных аналитических методов, таких как масс-спектрометрия или атомная эмиссионная спектроскопия. Эти методы позволяют идентифицировать изотопы металла и определить их относительное содержание в образце.
Какие металлы могут иметь изотопы?
Изотопы металла могут быть обнаружены у многих химических элементов, включая такие металлы, как железо, медь, свинец, золото и другие. Все эти металлы имеют несколько изотопов с различными массовыми числами.
