Переходные металлы - это элементы, которые находятся в периодической таблице между главными группами элементов. Они обладают свойствами, которые отличают их от других элементов, таких как бледно-желтый цвет соединений, альтернированный магнитный момент и широкий диапазон окислительно-восстановительных состояний. Атомы переходных металлов имеют свободные d-электроны, которые могут давать им уникальные электронные и световые свойства.
Строение атомов переходных металлов
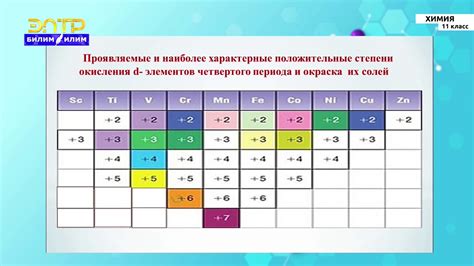
Атомы переходных металлов имеют сложную и уникальную структуру. Они содержат внутренние энергетические уровни, называемые полностью заполненными n-энергетическими уровнями, а также дополнительные d-энергетические уровни. В отличие от атомов элементов главной группы, уровни d-электронов в атомах переходных металлов могут быть частично заполнены. Это позволяет атомам переходных металлов образовывать различные окислительно-восстановительные состояния и обладать необычными электронными свойствами.
Окислительно-восстановительные свойства
Атомы переходных металлов могут менять свое окислительное состояние, что означает изменение числа электронов в их внешней оболочке. Это делает их хорошими катализаторами химических реакций. Экспериментальные данные показывают, что атомы переходных металлов легко вступают в реакции с молекулами, образуя комплексы с различными степенями окисления. Кроме того, они также могут образовывать металлокластеры и наночастицы с уникальными свойствами, которые могут быть использованы в катализе, электрохимии и медицине.
Электронные и световые свойства
Атомы переходных металлов имеют особенности, связанные с д-электронами, которые делают их интересными для исследования электронных и световых свойств. Д-электроны могут поглощать и испускать свет в видимом и ближнем инфракрасном диапазоне, что придает соединениям переходных металлов яркий цвет. Кроме того, д-электроны могут обладать магнитными свойствами, которые проявляются в альтернированном магнитном моменте атомов переходных металлов. Эти свойства делают атомы переходных металлов полезными в приложениях, связанных с радиологией, оптикой и информационными технологиями.
Переходные металлы: особенности и свойства
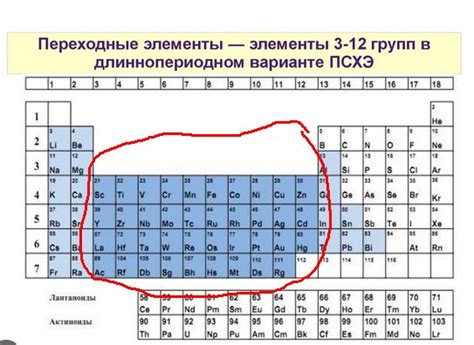
Переходные металлы – это элементы, которые находятся в таблице химических элементов между группами 2 и 13. Они обладают рядом особенностей и уникальных свойств, которые делают их важными в химии и промышленности.
Одной из особенностей переходных металлов является наличие внутренней оболочки электронов, которая защищает внешние электроны от воздействия других атомов. Это делает переходные металлы устойчивыми и позволяет им образовывать стабильные соединения.
Переходные металлы также характеризуются своей способностью образовывать ионы различных зарядов. Это связано с возможностью переходных металлов изменять число валентных электронов в своей внешней оболочке. Благодаря этому они могут образовывать соединения с различными элементами и участвовать во множестве химических реакций.
Важным свойством переходных металлов является их способность каталитического действия. Они могут ускорять химические реакции, не участвуя в них непосредственно. Это делает их полезными в различных промышленных процессах, а также в химической лаборатории.
Среди переходных металлов есть также элементы, обладающие магнитными свойствами. Они способны притягивать и взаимодействовать с магнитным полем. Это делает их важными в применении в магнитных материалах, электронике и многих других областях науки и техники.
В связи со своими особенностями и уникальными свойствами, переходные металлы играют важную роль во многих сферах жизни. Их применение распространено в промышленности, медицине, электронике и других отраслях. Поэтому изучение и понимание переходных металлов имеет большое значение для современной науки и технологий.
Вопрос-ответ

Что такое атом переходного металла?
Атом переходного металла - это атом элемента, который находится в периодической таблице между щелочными металлами и блоком p. Он обладает неполной заполненной внешней электронной оболочкой, что делает его химически активным.
Какие элементы являются переходными металлами?
Переходными металлами являются элементы, которые находятся в блоке d периодической таблицы. К ним относятся такие элементы, как железо, медь, никель, цинк, серебро и другие.
Чем переходные металлы отличаются от других элементов?
Переходные металлы отличаются от других элементов тем, что они имеют переменную степень окисления, образуют комплексные соединения и обладают химической активностью. Они также отличаются своими физическими свойствами, например, высокой плотностью, тугоплавкостью и хорошей проводимостью электричества и тепла.
Какую роль играют переходные металлы в химических реакциях?
Переходные металлы являются важными катализаторами химических реакций, так как они способны активировать молекулы и ускорять химические процессы. Они также широко используются в промышленности и технологии для производства металлов, сплавов и других материалов.
